Clear Sky Science · fr
Réduire la méthylation de la lysine 4 de l’histone 3.3 dans l’éminence ganglionnaire médiale et l’hypothalamus reproduit des phénotypes de troubles du développement neuronal
Comment de minuscules marques chimiques façonnent le cerveau et le corps
Pourquoi certains changements génétiques provoquent-ils à la fois des difficultés d’apprentissage et des modifications de la croissance, comme une très petite taille pendant l’enfance mais une obésité à l’âge adulte ? Cette étude examine de minuscules marques chimiques portées par les protéines qui emballent l’ADN dans le cerveau et montre comment leur perturbation dans seulement deux régions clés peut se répercuter en crises d’épilepsie, comportements anxieux, troubles de la mémoire et changements corporels marqués chez la souris.
Interrupteurs sur les variateurs du génome
Dans chaque cellule cérébrale, l’ADN est enroulé autour de protéines en forme de bobine appelées histones. Des marques chimiques apposées sur ces histones agissent comme des variateurs, augmentant ou diminuant l’activité de groupes de gènes. Une de ces marques, ajoutée sur un site nommé H3K4, est fortement associée à l’activation des gènes. Des études génétiques chez l’humain ont montré que des personnes nées avec des défauts dans les enzymes qui ajoutent ou enlèvent cette marque présentent souvent des troubles du développement neuronal combinant déficience intellectuelle, épilepsie et croissance corporelle anormale. Toutefois, on ignorait quelles cellules cérébrales sont les plus sensibles à cette perturbation et comment leur dysfonction pourrait relier l’excitabilité cérébrale et le métabolisme de l’ensemble du corps.
Ciblage de deux pôles cérébraux critiques
Les chercheurs ont conçu des souris dans lesquelles une version mutante d’une protéine histone (H3.3K4M) était activée uniquement dans les cellules issues de deux régions cérébrales embryonnaires : l’éminence ganglionnaire médiale, qui produit de nombreux neurones « freins » inhibiteurs du cerveau, et l’hypothalamus en développement, qui régule l’appétit, les hormones et l’équilibre énergétique. Cette mutation bloque spécifiquement la méthylation de H3K4 sans supprimer les histones eux‑mêmes. Des tests ont confirmé que la protéine mutante était largement présente dans les zones ciblées et que les marques normales de H3K4 y étaient fortement réduites alors que le niveau global d’histones restait stable. Cette stratégie imite de nombreuses conditions humaines où une seule copie d’un gène lié à H3K4 est défectueuse, plutôt que l’absence totale du gène.
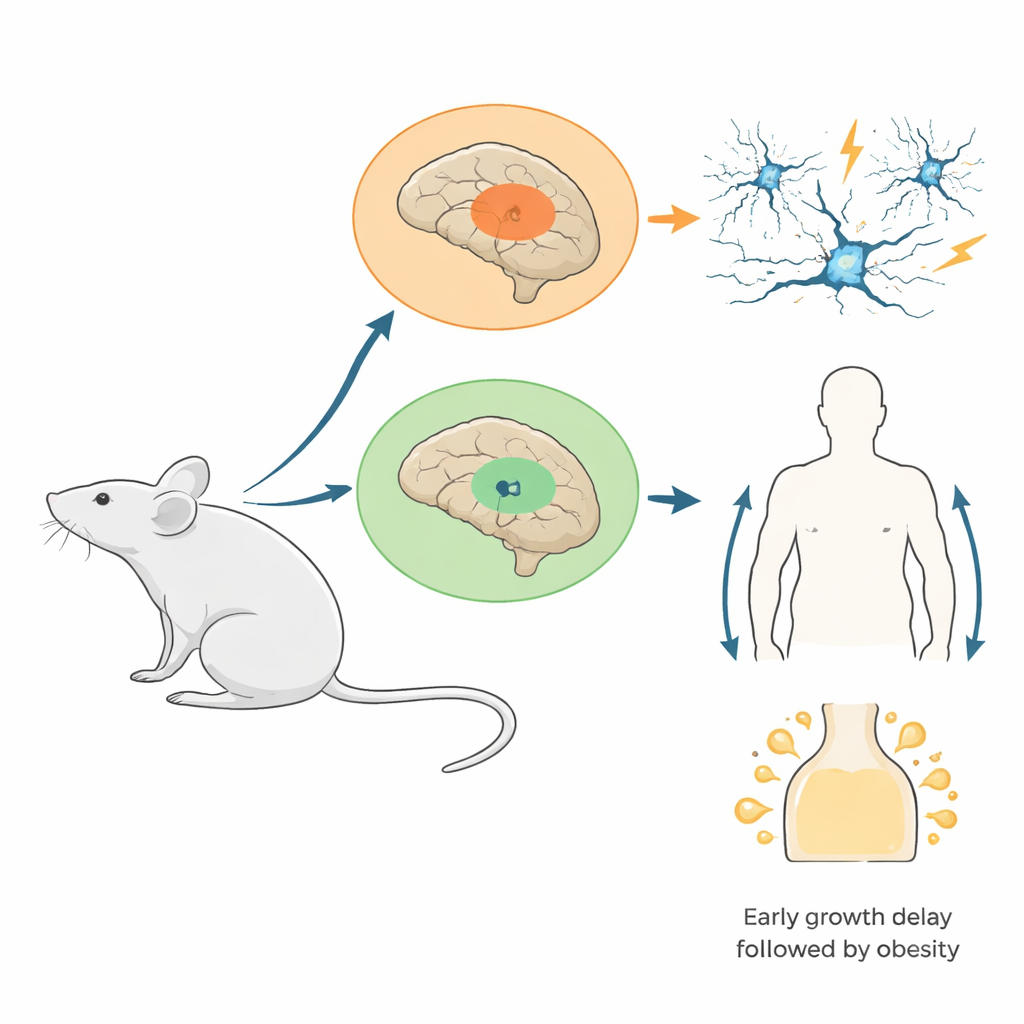
Des neurones freins manquants à des circuits prédisposés aux crises
À mesure que ces souris grandissaient, les conséquences pour les circuits cérébraux sont apparues. Les jeunes mutants avaient moins d’interneurones inhibiteurs dans le cortex et l’hippocampe, en particulier un type à décharge rapide qui maintient normalement le timing des rythmes neuronaux. Des enregistrements détaillés ont montré que les interneurones restants étaient présents mais présentaient une plus grande variabilité dans leurs propriétés électriques, suggérant une maturation perturbée. Lorsque l’hippocampe était stimulé dans des tranches de tissu, les habituelles oscillations « gamma » à haute fréquence — rythmes électriques liés au traitement de l’information — étaient plus faibles et plus lentes, et des événements anormaux en rafales sont apparus. Chez des animaux vivants, beaucoup de mutants, en particulier les femelles, ont développé des crises spontanées et étaient beaucoup plus sensibles aux crises induites par des médicaments. Au début du développement, l’équipe a attribué principalement cette perte cellulaire à une migration insuffisante des interneurones vers le cortex, et non à une augmentation de la mort cellulaire ou à une diminution de la division cellulaire.
Reprogrammation de l’activité génique dans les cellules liées aux crises
Pour relier ces changements physiques au contrôle des gènes, l’équipe a utilisé le séquençage d’un noyau à la fois qui lit à la fois l’activité génique et l’accessibilité de l’ADN dans des cellules individuelles. Dans l’éminence ganglionnaire médiale embryonnaire, la plupart des gènes modifiés chez les mutants étaient réprimés, y compris des régulateurs clés qui orientent les cellules vers des destins inhibiteurs spécifiques. Chez les interneurones adultes, l’équilibre entre sous‑types était altéré et des groupes de gènes impliqués dans la formation des connexions et dans le contrôle des courants potassiques — ces flux qui aident à régler la vitesse de décharge — étaient mal régulés. L’analyse de réseau a mis en évidence une perturbation coordonnée des gènes de canaux potassiques déjà connus pour influencer l’épilepsie et les rythmes cérébraux, fournissant un lien moléculaire direct entre la perte d’une marque histonique, l’altération de l’identité des interneurones et la susceptibilité aux crises.
Déséquilibre hypothalamique et courbe de croissance en deux phases
L’hypothalamus a raconté une histoire complémentaire centrée sur la croissance corporelle. Dès le stade de souriceau, les mutants étaient plus petits et une fraction importante succombait précocement. Les survivants, en revanche, mangeaient plus tard davantage, accumulaient de la graisse et développaient des taux élevés d’hormone leptine, signes d’obésité et probable résistance à la leptine. L’analyse unicellulaire de l’hypothalamus embryonnaire a révélé davantage de cellules progénitrices en division mais moins de cellules destinées aux noyaux clés liés à la prise alimentaire, en particulier des régions qui détectent normalement l’état nutritionnel et régulent l’hormone de croissance. Chez l’adulte, la composition cellulaire de l’hypothalamus était remodelée : les astrocytes augmentaient fortement, les oligodendrocytes diminuaient, et des cellules spécialisées de barrière appelées tanycytes ainsi que les glies voisines perdaient leur organisation ordonnée à l’interface du cerveau avec les hormones et nutriments circulants. Ces changements structuraux et d’expression génique déforment probablement la façon dont le cerveau perçoit les réserves d’énergie et contrôle l’appétit.
Échos comportementaux des troubles neurodéveloppementaux humains
Le comportement des souris faisait écho aux symptômes observés dans de nombreux troubles du développement neuronal. Elles présentaient des comportements anxieux plus marqués, une démarche modifiée, une activité spontanée réduite à domicile et de mauvaises performances dans des tâches évaluant la mémoire, la reconnaissance d’objets et le filtrage de sons surprenants. Certains tests ont révélé une augmentation d’actions de type impulsif. Sur de multiples mesures, les femelles semblaient plus sévèrement affectées que les mâles, suggérant que les systèmes hormonaux et la régulation génique spécifiques au sexe peuvent interagir avec les marques histones pour façonner la vulnérabilité.
Que signifie cela pour la santé humaine
Ensemble, ces résultats montrent qu’affaiblir un ensemble de marques histoniques dans seulement deux pôles embryonnaires du cerveau suffit à reproduire une large constellation de problèmes : moins de « freins » inhibiteurs, réseaux cérébraux instables, crises, circuits de la prise alimentaire perturbés et croissance corporelle anormale. Pour le grand public, le message clé est que les marques épigénétiques comme la méthylation de H3K4 ne sont pas de vagues ajouts, mais des boutons de contrôle précis qui aident les cellules cérébrales en développement à devenir le bon type, au bon endroit et au bon moment. Lorsque ces réglages sont perturbés, comme dans de nombreux syndromes génétiques rares, le résultat peut être une combinaison étroitement liée de symptômes cognitifs, comportementaux et métaboliques. Comprendre ces racines communes pourra finalement guider des thérapies qui corrigent non seulement un symptôme, comme les crises ou l’obésité, mais le système interconnecté qui les engendre.
Citation: Li, J., Tanzillo, A.F., Pizzirusso, G. et al. Reducing methylation of histone 3.3 lysine 4 in the medial ganglionic eminence and hypothalamus recapitulates neurodevelopmental disorder phenotypes. Nat Commun 17, 2984 (2026). https://doi.org/10.1038/s41467-026-69248-9
Mots-clés: épigénétique, interneurones, hypothalamus, convulsions, obésité