Clear Sky Science · fr
Dissocier la séparation de phase et la fibrillisation préserve l’activité des condensats biomoléculaires
Pourquoi cela compte pour la santé du cerveau
De nombreuses maladies cérébrales, dont la maladie d’Alzheimer, impliquent des protéines qui s’agglutinent en enchevêtrements durs et fibreux au fil du temps. Ces mêmes protéines peuvent aussi former à l’intérieur des cellules des structures plus molles, en gouttelettes, qui aident à organiser la chimie cellulaire, un peu comme de minuscules postes de travail liquides. Cette étude pose une question cruciale : peut‑on empêcher la transformation nocive de ces gouttelettes en fibres sans détruire leur fonction utile au quotidien ? Les auteurs montrent qu’un métabolite cellulaire courant, l’acide aminé L‑arginine, peut précisément faire cela pour une protéine clé liée à Alzheimer appelée Tau.
Du protéin libre aux minuscules gouttelettes
À l’intérieur des cellules, certaines protéines ne restent pas toujours uniformément dispersées dans le fluide cytoplasmique. Elles peuvent au contraire se rassembler en gouttelettes, appelées condensats biomoléculaires, qui se comportent comme des gels très mous ou des liquides visqueux. L’équipe s’est concentrée sur Tau, une protéine qui aide normalement à assembler et stabiliser les microtubules—des filaments creux qui font office de voies de transport dans les neurones. Tau est aussi tristement célèbre pour former des fibrilles amyloïdes, les fibres rigides présentes dans les enchevêtrements caractéristiques de nombreuses maladies neurodégénératives. Pour étudier l’évolution des gouttelettes de Tau au fil du temps, les chercheurs ont conçu une version modifiée de la protéine, nommée SynTag‑Tau, qui forme des condensats actifs vieillissant en fibrilles amyloïdes sur une échelle de temps adaptée à l’expérimentation, sans additifs agressifs.
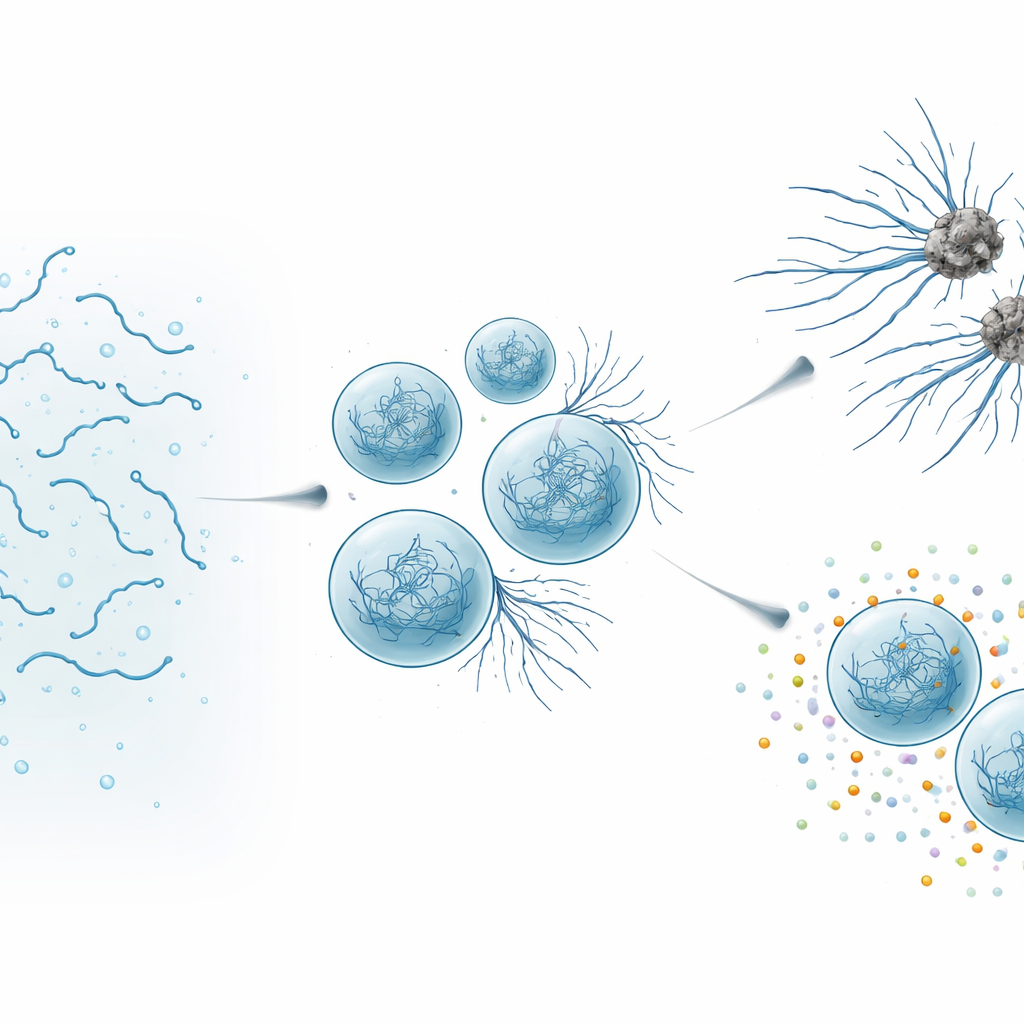
Quand des gouttelettes utiles deviennent nocives
Grâce à la microscopie haute résolution et à des mesures biophysiques, les auteurs ont observé les gouttelettes de SynTag‑Tau évoluer sur plusieurs heures. Les gouttelettes fraîches se comportaient comme des liquides : elles fusionnaient facilement, leurs molécules se déplaçaient rapidement et aucune structure ordonnée n’était visible. Avec le temps, les gouttelettes ralentissaient et se raidissaient, et de fines fibres commençaient à pousser depuis leur surface vers le milieu environnant. Des méthodes optiques sensibles ont montré que ces fibres présentaient l’architecture « cross‑beta » fortement empaquetée typique des amyloïdes. Fait notable, l’interface—la frontière entre la goutte dense et le fluide environnant—agissait comme un point chaud où les fibrilles apparaissaient en premier. À mesure que les gouttelettes vieillissaient et produisaient davantage de fibres, la fonction normale de Tau se détériorait : les condensats perdaient leur capacité à attirer la tubuline, le bloc de construction des microtubules, et finissaient par ne plus soutenir l’assemblage des microtubules du tout.
Petites molécules qui font basculer l’équilibre
Les chercheurs se sont ensuite demandé si des métabolites simples pouvaient ralentir ou empêcher cette transition liquide→fibre tout en laissant les gouttelettes intactes. En testant plusieurs petites molécules naturelles, ils ont trouvé que les acides aminés chargés positivement L‑arginine et L‑lysine retardaient fortement ou bloquaient la formation de fibrilles amyloïdes à partir des gouttelettes de SynTag‑Tau, sans empêcher la formation des gouttelettes à des concentrations réalistes de l’ordre du millimolaire. En revanche, des acides aminés chargés négativement comme le glutamate et l’aspartate accéléraient la formation de fibrilles, et des agents généraux perturbant les protéines échouaient à aider ou perturbaient eux‑mêmes les gouttelettes. Un analogue fluorescent de la L‑arginine a révélé que cette molécule préfère se localiser à l’intérieur des condensats de Tau plutôt qu’à l’extérieur, suggérant qu’elle agit là où elle est le plus nécessaire.
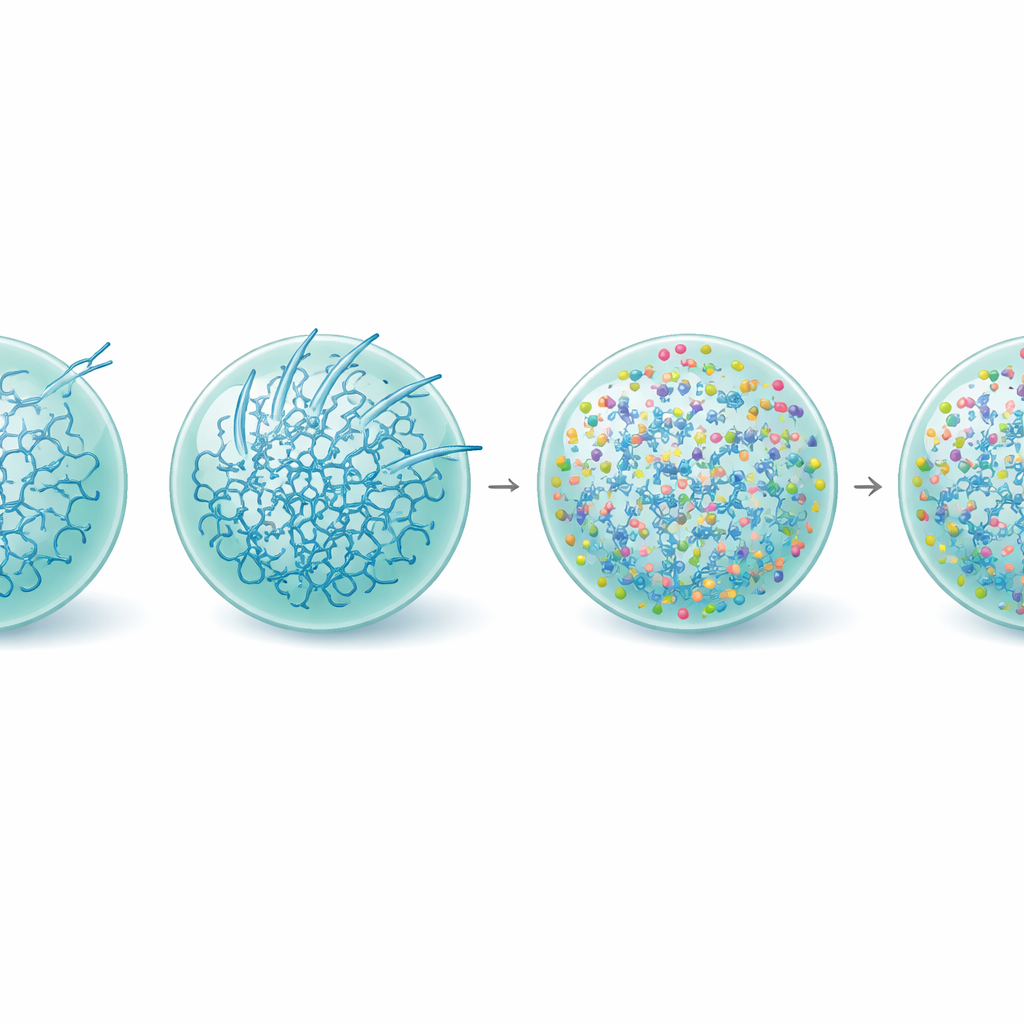
Renforcer la goutte, sauver la fonction
En approfondissant, l’équipe a examiné comment la L‑arginine remodèle la vie interne des gouttelettes de Tau. Des mesures de la structure protéique ont montré qu’en présence de L‑arginine, la fraction de molécules de Tau adoptant les conformations rigides riches en feuillets bêta associées aux amyloïdes était réduite, même dans des gouttelettes vieillies. La nanorhéologie par vidéo—suivi du mouvement de minuscules billes à l’intérieur des condensats—a révélé que la L‑arginine rendait en réalité les gouttelettes de Tau plus viscoélastiques, c’est‑à‑dire que leur réseau interne devenait plus solide et plus interconnecté tout en restant de type fluide. Ce renforcement semble maintenir le système dans un état métastable et fonctionnel et augmente la barrière énergétique à la formation de fibrilles, en particulier à la surface des gouttelettes. Cohérent avec cela, les condensats traités à la L‑arginine continuaient à recruter la tubuline de manière homogène et soutenaient la croissance des microtubules longtemps après que les gouttelettes non traitées étaient devenues inactives.
Ce que cela signifie pour les thérapies futures
Le travail montre que les forces qui favorisent la formation de gouttelettes protéiques et celles qui conduisent à la formation de fibres nocives sont liées mais dissociables. En modulant la chimie à l’intérieur des condensats avec un métabolite tel que la L‑arginine, il est possible de préserver l’état bénéfique et liquide tout en retardant ou en empêchant la transition vers des fibres amyloïdes associées à la maladie. Bien que cette étude utilise un système Tau spécialement conçu in vitro, elle offre une preuve de principe : des petites molécules qui renforcent sélectivement la stabilité des condensats pourraient un jour aider à protéger les cellules de l’accumulation progressive d’agrégats protéiques toxiques sans bloquer les rôles organisateurs normaux des condensats biomoléculaires.
Citation: Mahendran, T.S., Singh, A., Srinivasan, S. et al. Decoupling phase separation and fibrillization preserves activity of biomolecular condensates. Nat Commun 17, 2841 (2026). https://doi.org/10.1038/s41467-026-69244-z
Mots-clés: Protéine Tau, condensats biomoléculaires, fibrilles amyloïdes, L-arginine, neurodégénérescence