Clear Sky Science · fr
Une signature électrophysiologique humaine de la physiopathologie du syndrome de l’X fragile est partagée dans V1 des souris Fmr1-/y
Pourquoi les rythmes cérébraux importent dans l’X fragile
Le syndrome de l’X fragile est une cause héréditaire majeure de déficience intellectuelle et d’autisme. Familles et cliniciens espéraient depuis longtemps que des traitements prometteurs testés chez la souris profiteraient aux personnes, mais de nombreux médicaments efficaces dans les modèles animaux ont échoué en essais cliniques. Cette étude pose une question simple mais cruciale : peut-on identifier un signal cérébral partagé et mesurable chez l’humain et la souris qui rende compte de ce qui dysfonctionne dans l’X fragile, et qui change aussi lorsque des traitements agissent sur le cerveau ?
Les rythmes lents « au ralenti » comme fenêtre sur le cerveau
Nos cerveaux ne sont jamais vraiment au repos. Même au repos, des milliards de neurones génèrent une activité électrique rythmique détectable à la surface du crâne par électroencéphalographie (EEG). L’un des rythmes les plus puissants est l’alpha, une oscillation douce de 8–13 cycles par seconde qui est particulièrement marquée à l’arrière de la tête et aide à réguler le traitement des informations visuelles et auditives. Dans de nombreux troubles cérébraux, y compris l’X fragile, l’autisme, la schizophrénie et d’autres, ce rythme est altéré. Ici, les chercheurs se sont penchés sur la manière dont les rythmes alpha diffèrent chez les hommes présentant l’X fragile par rapport à des pairs en développement typique, et sur l’existence d’un rythme similaire dans le cortex visuel des souris modèles de l’X fragile.
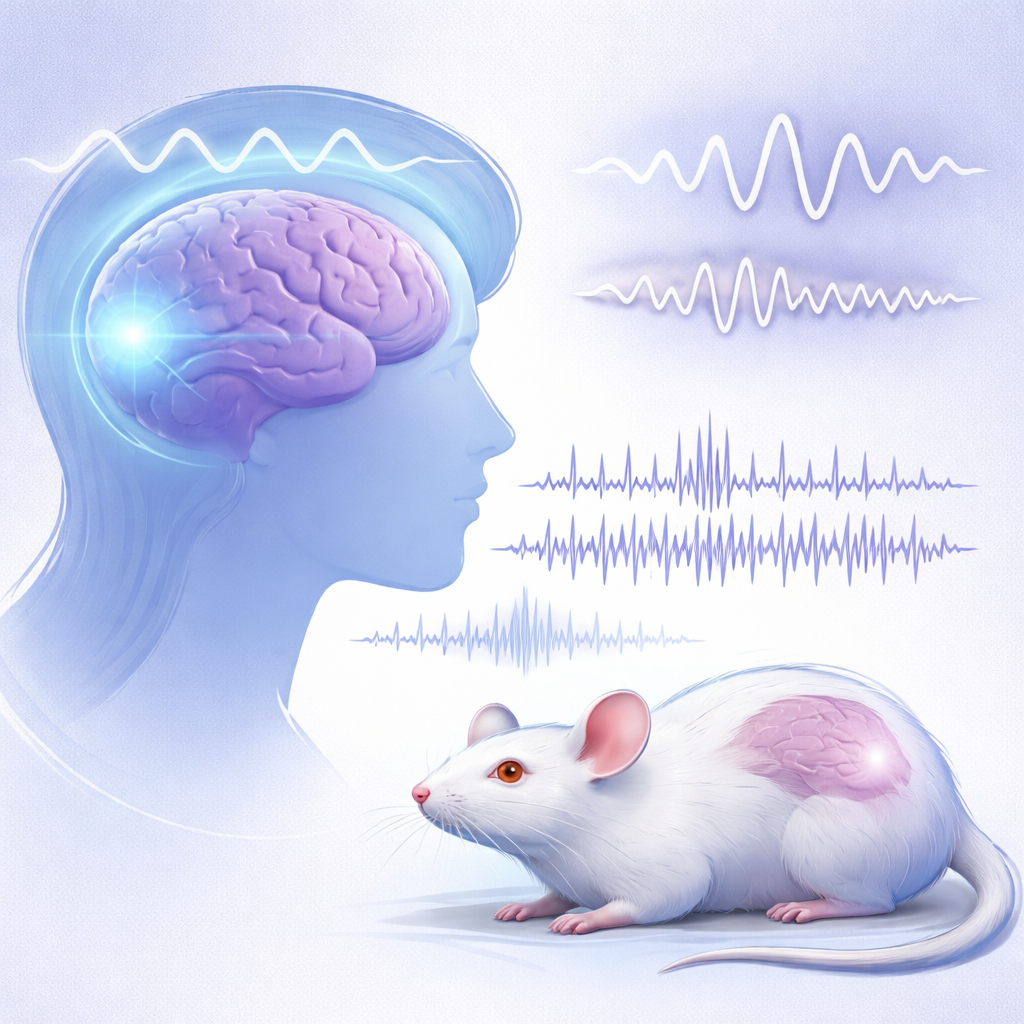
Ce que les chercheurs ont observé chez l’humain
L’équipe a enregistré l’EEG au repos chez des garçons et des hommes atteints de l’X fragile et chez des témoins appariés par âge, en utilisant de nombreux petits électrodes sur le cuir chevelu. Plutôt que de se limiter aux bandes de fréquences classiques, ils ont séparé le signal de chaque personne en un « bruit » de fond lisse et des pics distincts représentant de véritables oscillations rythmiques. Toutes tranches d’âge confondues, les personnes atteintes de l’X fragile présentaient un déplacement constant de leur pic principal basse fréquence — lié à l’alpha — vers des fréquences plus lentes. Chez les enfants, ce pic de type alpha était non seulement plus lent mais aussi plus faible en puissance, tandis que chez les adultes il était clairement plus lent mais de puissance comparable à celle des témoins. La source la plus marquée de ce rythme altéré a été localisée dans les zones visuelles à l’arrière du cerveau, ce qui suggère une cible pertinente pour la comparaison avec les modèles animaux.
Correspondances dans le cortex visuel de la souris
En appliquant la même méthode d’analyse, les chercheurs ont ensuite mesuré l’activité cérébrale dans le cortex visuel de souris mâles modèles de l’X fragile et de leurs congénères sains. Les souris n’ont pas une bande alpha humaine classique, mais elles présentent un rythme proéminent de 3–6 cycles par seconde dans le cortex visuel lorsqu’elles regardent calmement un écran gris ou sont dans l’obscurité. Chez les souris X fragile ce rythme était ralenti, reproduisant ce qui avait été observé chez l’humain. Lorsqu’on a placé de petites électrodes directement dans le cortex visuel, une image encore plus fine est apparue : le principal rythme basse fréquence contenait en fait deux sous-pics. Le plus bas montrait le ralentissement observé dans l’X fragile, tandis que les modifications du sous-pic supérieur ne semblaient présentes qu’à l’état juvénile, faisant écho aux changements spécifiques à l’enfance observés chez l’humain.
Cellules et chimie derrière le rythme
Parce que les expériences chez la souris permettent d’explorer directement les types cellulaires et les médicaments, l’équipe a ensuite cherché quels neurones et quels signaux chimiques façonnent ces rythmes de type alpha. Ils ont constaté que la suppression de la protéine de l’X fragile spécifiquement dans les neurones excitateurs corticaux et les cellules de soutien proches suffisait à recréer les rythmes anormaux, même lorsque les cellules inhibitrices restaient génétiquement intactes. En atténuant sélectivement deux classes majeures d’interneurones inhibiteurs — ceux exprimant la parvalbumine et ceux exprimant la somatostatine — ils ont montré que chaque classe influence un sous-pic différent du rythme. Ils ont ensuite testé un médicament, l’Arbaclofène, qui renforce un type particulier de signal inhibiteur (récepteurs GABA_B). Chez les souris témoins, ce médicament a rendu le rythme basse fréquence plus fort et légèrement plus lent, confirmant que l’oscillation est sensible à une intervention pharmacologique. Chez les souris X fragile, cependant, les mêmes doses eurent un effet plus faible sur le rythme, même si elles réduisaient toujours l’activité excessive aux fréquences plus élevées.
Relier les souris de laboratoire et le traitement humain
Pour les non-spécialistes, le message clé est que cette étude identifie une anomalie rythmique cérébrale spécifique et partagée chez les personnes atteintes de l’X fragile et dans un modèle murin, et montre que ce signal peut être modulé par un médicament de façons qui dépendent de l’âge et du génotype. Le rythme ralenti de type alpha offre un « thermomètre » pratique de la fonction cérébrale mesurable de la même manière chez l’humain et la souris, et qui pourrait mieux suivre l’efficacité des traitements que les ondes cérébrales rapides utilisées auparavant. En reliant ce rythme à des types cellulaires et à des voies inhibitrices particulières, le travail indique aussi des stratégies plus ciblées pour de futurs traitements, tout en aidant à expliquer pourquoi certains essais médicamenteux antérieurs n’ont pas été transposables de la souris à l’humain.
Citation: Kornfeld-Sylla, S.S., Gelegen, C., Norris, J.E. et al. A human electrophysiological signature of Fragile X pathophysiology is shared in V1 of Fmr1-/y mice. Nat Commun 17, 1497 (2026). https://doi.org/10.1038/s41467-026-69243-0
Mots-clés: Syndrome de l’X fragile, rythmes cérébraux, oscillations alpha, cortex visuel, inhibition GABA