Clear Sky Science · fr
Des variantes de FOXJ3 associées à l’épilepsie relient un programme transcriptionnel de la voie PTEN-mTOR à la spécification neuronale et à la lamination corticale
Quand le câblage du cerveau dévie légèrement
L’épilepsie débute souvent pendant l’enfance, mais chez de nombreux jeunes patients les examens cérébraux ne révèlent rien d’évident. Cette étude explore une cause cachée : de petites variations d’un gène nommé FOXJ3 qui modifient en silence la façon dont la couche externe du cerveau, le cortex, se construit. En suivant l’action de ce gène dans des familles atteintes d’épilepsie focale et dans des cerveaux de souris en développement, les auteurs montrent comment des erreurs précoces dans la naissance, le déplacement et la stratification des cellules peuvent finalement conduire à des crises.
Une malformation discrète derrière des crises difficiles à traiter
De nombreux enfants atteints d’épilepsie focale résistante aux médicaments présentent une dysplasie corticale focale (DCF), dans laquelle des régions du cortex sont malformées. Ces zones contiennent des neurones mal placés et anormalement volumineux et constituent une cause fréquente de l’échec des traitements médicamenteux. Pourtant, la cause moléculaire de la DCF est souvent inconnue, et l’IRM standard peut manquer des défauts petits ou superficiels. Les auteurs ont commencé par une famille dans laquelle plusieurs membres souffraient d’épilepsie focale avec des signes de DCF. Une analyse génomique attentive a mis en évidence des variantes rares de FOXJ3, un gène qui n’avait pas été lié auparavant à l’épilepsie. D’autres cas, issus de larges bases de données génétiques, ont révélé davantage d’individus porteurs de variantes inhabituelles de FOXJ3 et de crises focales, suggérant que ce gène pourrait jouer un rôle récurrent dans ces troubles.
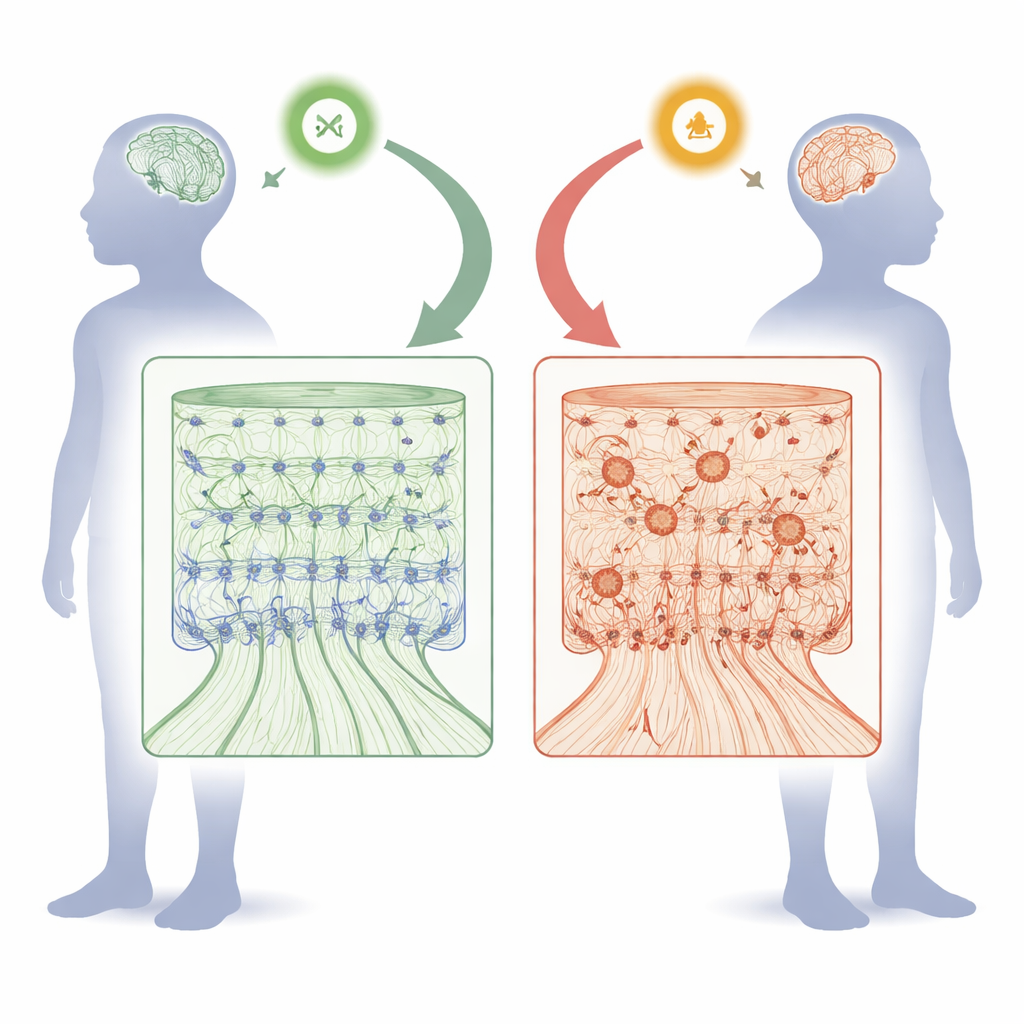
Comment FOXJ3 contribue à façonner la surface pensante du cerveau
Pendant le développement fœtal, le cortex se construit comme un immeuble à plusieurs étages. Des cellules souches bordant la surface interne du cerveau se divisent, puis envoient des neurones nouveaux vers l’extérieur le long de « échafaudages » radiaux pour former six couches ordonnées. L’équipe a constaté que FOXJ3 est actif à la fois dans ces progéniteurs de type souche et dans les jeunes neurones, mais son activité dans les progéniteurs diminue naturellement après un point précis au milieu de la gestation. En réduisant les niveaux de Foxj3 à différents stades chez des embryons de souris à l’aide d’outils d’inhibition génique, les chercheurs ont observé les conséquences. Une perte précoce de Foxj3 a ralenti la migration des nouveaux neurones et entraîné leur installation dans de mauvaises couches. Des cellules qui devaient devenir des neurones des couches profondes ont plutôt adopté des identités typiques des couches supérieures, et un excès de neurones projecteurs callosaux, qui relient les deux hémisphères, a été produit. En revanche, une réduction de Foxj3 plus tardive a eu des effets beaucoup plus modérés, montrant que son rôle dépend fortement du moment où il intervient.
Maintenir l’équilibre entre division cellulaire et croissance
Pour comprendre pourquoi FOXJ3 a une telle influence, les auteurs ont combiné plusieurs approches à grande échelle. Ils ont cartographié où FOXJ3 se lie sur l’ADN et quels gènes sont actifs dans des milliers de cellules corticales individuelles. Cela a fortement pointé vers des gènes qui régulent le cycle cellulaire et la croissance cérébrale, en particulier PTEN, un frein majeur d’une voie de croissance connue sous le nom de mTOR. Dans les cellules progénitrices, la liaison de FOXJ3 augmentait l’activité de PTEN, ce qui aidait les cellules à quitter le cycle de division, à se transformer en neurones et à migrer vers l’extérieur de manière ordonnée. Lorsque Foxj3 était réduit, davantage de progéniteurs restaient en division, moins de cellules quittaient le cycle au bon moment et la migration s’arrêtait dans des zones intermédiaires. De façon cruciale, restaurer les niveaux de PTEN dans des cerveaux déficients en Foxj3 a largement renversé les problèmes de migration, de lamination et de destin cellulaire, tandis que l’augmentation d’un autre régulateur de croissance, TSC1, ne l’a pas fait. Cela place PTEN au centre du contrôle exercé par FOXJ3 sur la construction corticale.
De voies mal régulées à des neurones hypertrophiés
L’équipe s’est ensuite intéressée au comportement des variantes de FOXJ3 observées chez des patients. Une version associée à la maladie n’a pas réussi à augmenter les niveaux de PTEN et a permis à la voie mTOR de devenir hyperactive, comme le montre une phosphorylation accrue d’une protéine clé liée à la croissance. Chez des souris adolescentes génétiquement modifiées pour exprimer cette forme mutante dans le cortex en développement, les neurones sont apparus plus tard visiblement gonflés, avec des corps et des périmètres cellulaires plus grands, imitant les cellules dysmorphiques observées dans la DCF humaine. Pourtant la protéine mutante atteignait correctement le noyau, ce qui indique que le problème réside dans une régulation génique défectueuse et non dans une mauvaise localisation. Ensemble, ces résultats relient les mutations de FOXJ3 à une cascade d’événements — moins de PTEN, plus de signalisation mTOR, sortie retardée du cycle cellulaire, migration désordonnée et neurones hypertrophiés — qui peuvent préparer le terrain à des réseaux épileptiques.
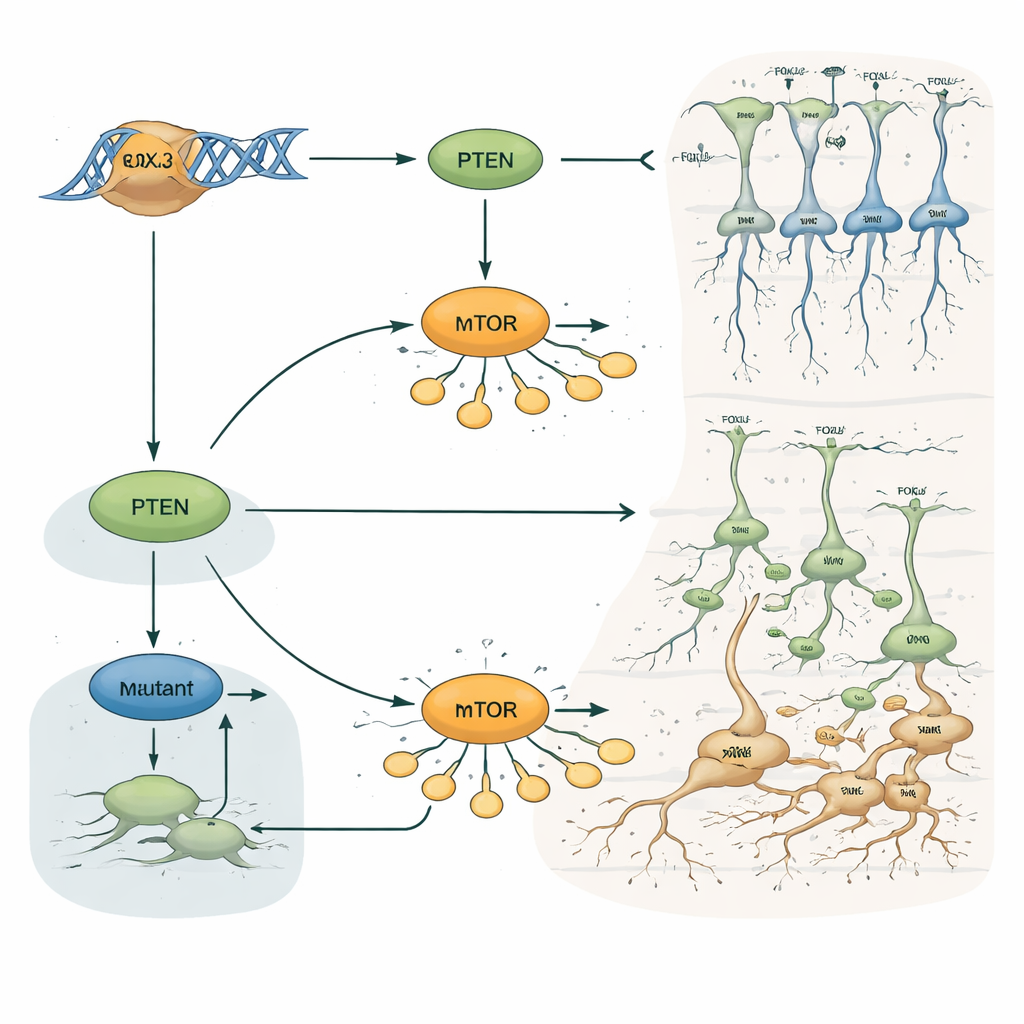
Pourquoi cela compte pour l’épilepsie et les lésions cérébrales cachées
Pour un non-spécialiste, le message essentiel est qu’un seul facteur de transcription, FOXJ3, contribue à décider quand et où les neurones corticaux naissent, comment ils se déplacent et dans quelle couche ils s’intègrent finalement. En agissant via la voie de croissance PTEN–mTOR, FOXJ3 maintient la construction du cerveau selon un calendrier précis. De rares variations de ce gène peuvent faire pencher cet équilibre, provoquant de petites zones de cortex mal câblées et mal laminées, même lorsque les IRM semblent normales. Ce travail propose non seulement FOXJ3 comme une nouvelle cause génétique possible de dysplasie corticale focale et d’épilepsie, mais illustre aussi comment des décalages subtils au début du développement cérébral peuvent résonner des décennies plus tard sous forme de crises difficiles à traiter.
Citation: Cheng, HY., Liu, C., Nien, CW. et al. Epilepsy-associated FOXJ3 variants link a transcriptional program of the PTEN-mTOR pathway to neuronal specification and cortical lamination. Nat Commun 17, 1815 (2026). https://doi.org/10.1038/s41467-026-69241-2
Mots-clés: dysplasie corticale focale, gène FOXJ3, voie PTEN mTOR, développement cortical, épilepsie focale