Clear Sky Science · fr
Stockage amélioré du sodium dans le carbone dur via un électrolyte à co-intercalation de solvant permettant des cellules pouch Ah à basse température
Pourquoi des batteries résistantes au froid sont importantes
Des voitures électriques dans des régions enneigées aux capteurs dans l’Arctique profond, de nombreux dispositifs modernes nécessitent des batteries qui fonctionnent par grand froid. Les batteries lithium et sodium actuelles perdent souvent de la puissance ou cessent complètement de fonctionner à très basse température parce que leur chimie interne ralentit. Cette étude explore une nouvelle façon de concevoir des batteries sodium-ion — en utilisant un liquide spécialement formulé à l’intérieur de la batterie — afin qu’elles puissent stocker et délivrer de l’énergie de manière fiable même à des températures aussi basses que −50 °C.
Le défi des batteries qui gèlent
Les batteries stockent l’énergie en déplaçant des atomes chargés, appelés ions, entre deux électrodes solides via un électrolyte liquide. Dans les batteries sodium-ion, les ions sodium doivent franchir un film de surface fin puis entrer dans une électrode négative à base de carbone appelée carbone dur. À basse température, deux choses se produisent : les ions se déplacent plus lentement dans le liquide, et ils ont du mal à se débarrasser des molécules de solvant qui les entourent avant de pénétrer dans le carbone dur. Parallèlement, le film de surface protecteur — appelé la couche d’interface électrolytique solide (SEI) — a tendance à s’épaissir et à devenir plus résistif par le froid. Tout cela complique le déplacement des ions sodium, si bien que la batterie peut délivrer bien moins d’énergie quand elle est le plus nécessaire.
Un nouveau mélange liquide pour faciliter le trajet des ions
Les chercheurs ont abordé ce problème en repensant l’électrolyte pour que les ions sodium n’aient plus à se dénuder complètement de leur coque de solvant avant d’entrer dans le carbone dur. Ils ont mélangé deux solvants à base d’éther : le diéthylène glycol diméthyl éther (G2), qui se lie fortement aux ions sodium et favorise un mouvement ionique rapide, et le 2-méthyloxolane (MO), un liquide moins polaire qui reste fluide à très basses températures. Dans l’électrolyte dit « à co-intercalation », les ions sodium se coordonnent principalement avec le G2, tandis que le MO agit surtout comme un solvant libre non liant qui aide à maintenir le mélange liquide jusqu’à −50 °C. Des simulations informatiques et des mesures spectroscopiques ont montré que ce mélange forme une structure stable où les ions sodium et le G2 voyagent ensemble en petit groupe.
Laisser les ions entrer dans le carbone sans se déshabiller
Plutôt que de forcer les ions sodium à perdre leur coque de solvant à la surface de l’électrode, le nouvel électrolyte permet aux clusters sodium–G2 de glisser directement à travers le film de surface et dans les espaces feuilletés du carbone dur. Ce processus, appelé co-intercalation de solvant, évite l’étape lente de « déshabillage » qui limite habituellement les performances par grand froid. Des tests microscopiques et spectroscopiques ont révélé que le film de surface formé avec cet électrolyte est plus fin et plus riche en composés inorganiques que dans les systèmes conventionnels. Cette combinaison protège l’électrode tout en permettant aux ions de traverser rapidement. Des mesures de diffusion ionique et de résistance électrique ont confirmé que les ions se déplacent plus vite à l’intérieur du carbone et à travers l’interface, en particulier à basse température.
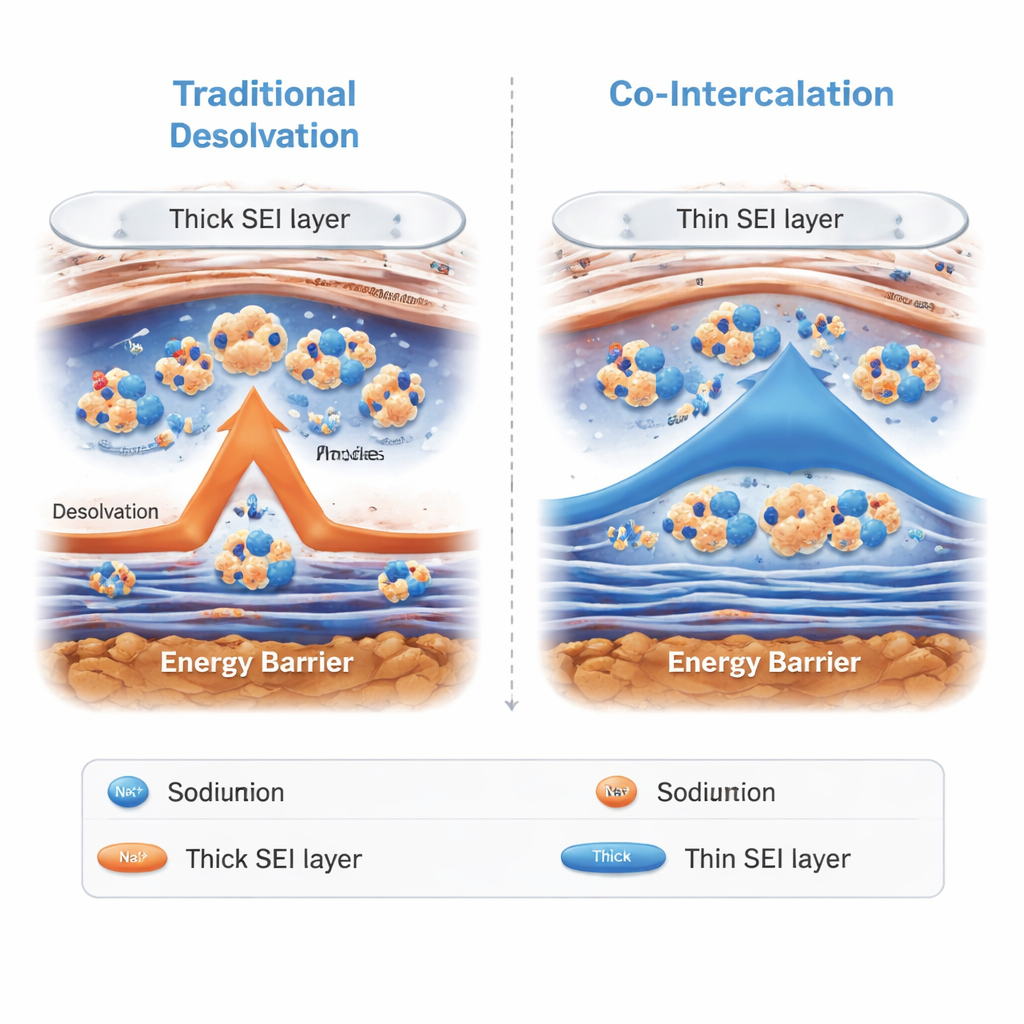
Performances solides même à −50 °C
Lorsque l’équipe a testé des cellules au format pile bouton utilisant du carbone dur et le nouvel électrolyte, elle a constaté que les batteries conservaient une forte capacité et une bonne efficacité de la température ambiante jusqu’à −50 °C. À −50 °C, l’électrode en carbone dur affichait encore environ 80 % de son efficacité de charge initiale et conservait plus de 90 % de sa capacité après 200 cycles de charge–décharge. Au-delà des petites cellules, les chercheurs ont fabriqué des cellules pouch — batteries plates similaires à celles des appareils électroniques grand public — d’une capacité d’environ 1,2 ampère-heure. Ces batteries sodium-ion complètes ont atteint une énergie spécifique de 163 watt-heures par kilogramme à température ambiante et de 107 watt-heures par kilogramme à −50 °C, tout en continuant d’alimenter des lampes LED pendant plus de 10 heures dans une chambre à −50 °C.
Ce que cela signifie pour les batteries des futurs climats froids
Pour les non-spécialistes, le message principal est que les auteurs ont trouvé un moyen de laisser les ions sodium conserver leur couche de solvant utile lorsqu’ils pénètrent dans l’électrode en carbone de la batterie. En concevant un électrolyte qui reste liquide par grand froid et forme un film de surface fin et favorable aux ions, ils ont levé un obstacle majeur aux performances à basse température. Cette approche pourrait aider à rendre les batteries sodium-ion — une alternative moins coûteuse aux lithium-ion — plus pratiques pour une utilisation dans les climats hivernaux, les régions d’altitude et autres environnements rudes où un stockage d’énergie fiable et abordable est indispensable.
Citation: Li, M., Liu, Z., Zhao, Y. et al. Enhanced sodium storage in hard carbon via solvent co-intercalation electrolyte enabling Ah-level pouch cells at low temperatures. Nat Commun 17, 1478 (2026). https://doi.org/10.1038/s41467-026-69237-y
Mots-clés: batteries sodium-ion, batteries basse température, conception d'électrolyte, anodes en carbone dur, stockage d'énergie