Clear Sky Science · fr
Base moléculaire de la galactosylation du collagène par GLT25D1
Comment de petites étiquettes sucrées contribuent à construire des tissus solides
Le collagène est la protéine la plus abondante de l’organisme, formant l’armature de la peau, des os, des vaisseaux sanguins et de nombreux autres tissus. Mais le collagène ne travaille pas seul : il doit être orné de petites molécules sucrées à des sites précis pour acquérir la bonne résistance et la bonne souplesse. Cette étude révèle, au niveau atomique, comment une enzyme clé, GLT25D1, fixe un sucre particulier au collagène et comment des défauts de ce processus peuvent conduire à des vaisseaux fragiles, des problèmes musculaires et peut‑être même au cancer.
Un regard rapproché sur la transformation cachée du collagène
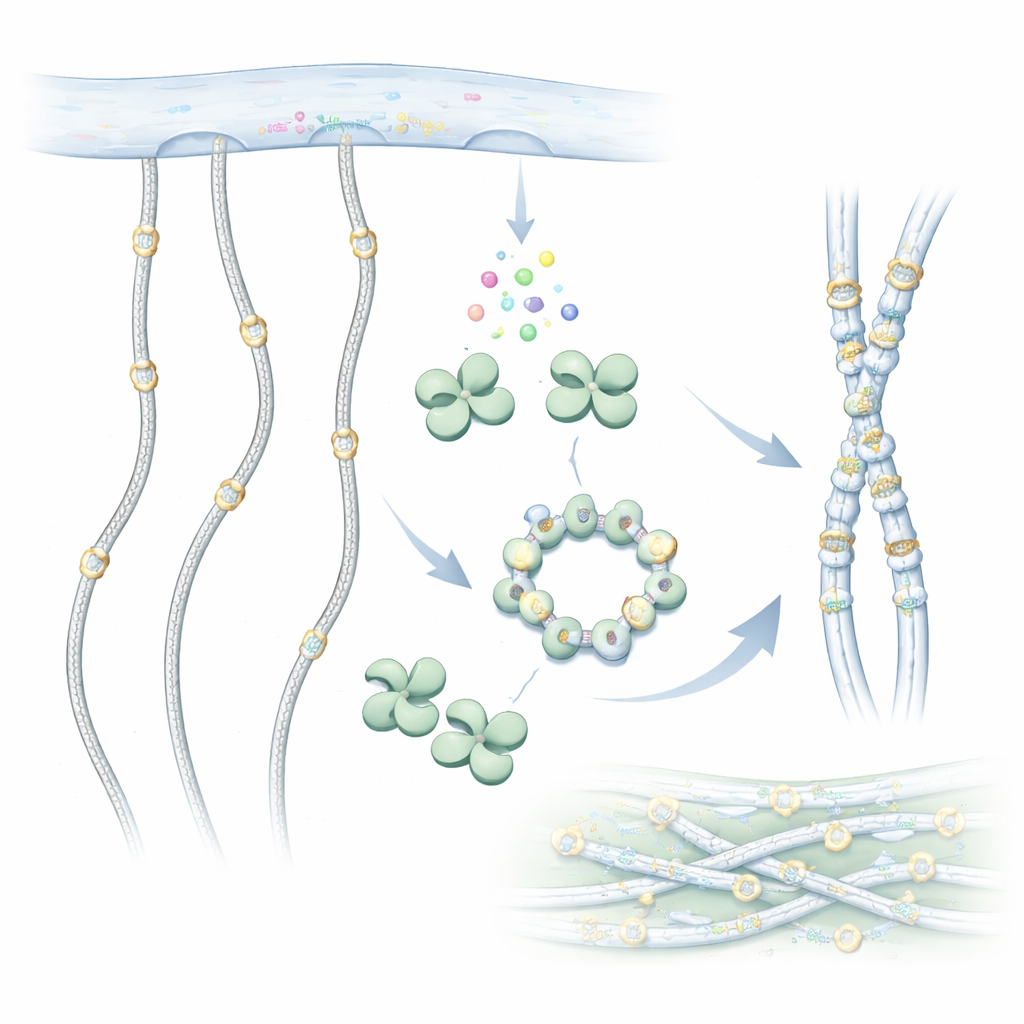
Les molécules de collagène sont de longues chaînes semblables à des cordes qui s’assemblent en fibres robustes à l’extérieur des cellules. Avant de quitter la cellule, elles sont toutefois modifiées chimiquement. Une modification importante est l’ajout de groupes sucrés sur des résidus spéciaux appelés hydroxylysines le long de la chaîne de collagène. GLT25D1 effectue la première étape de ce marquage sucré, transférant un sucre galactose depuis une molécule donneuse sur l’hydroxylysine. Cette décoration sucrée est conservée des animaux simples jusqu’aux humains et aide le collagène à se replier correctement, à interagir avec les cellules et à résister à l’usure.
Révéler la forme d’un « décorateur » du collagène
Pour comprendre le fonctionnement de GLT25D1, les chercheurs ont utilisé la cryo‑microscopie électronique pour imager l’enzyme humaine à une résolution quasi atomique. Ils ont découvert que chaque molécule de GLT25D1 possède deux lobes similaires, tous deux apparentés à un repli enzymatique commun observé dans les protéines transférant des sucres. Ces lobes s’associent pour former des dimères allongés, et trois dimères peuvent s’assembler en un hexamère en forme d’anneau. Dans ces assemblages, les véritables lieux de travail — les centres catalytiques — sont éloignés les uns des autres, une organisation qui pourrait permettre à plusieurs sites d’ajout de sucre d’opérer simultanément le long d’une chaîne de collagène étirée.
Les pièces en action : où le transfert de sucre a lieu
L’équipe a résolu des structures de GLT25D1 liée à la fois à son donneur de sucre et à un court peptide de type collagène contenant une hydroxylysine. Ce complexe ternaire a montré que seul le second lobe, appelé domaine C‑terminal, réalise réellement la chimie. Là, la molécule donneuse se niche dans une poche stabilisée par un ion métallique, tandis que le peptide repose dans une gouttière étroite qui impose un motif local spécifique : une hydroxylysine immédiatement suivie d’une petite glycine. Un seul résidu d’aspartate agit comme base chimique, activant le groupe hydroxyle de l’hydroxylysine pour qu’il attaque le sucre et complète le transfert. Des modifications de l’un quelconque de ces acides aminés clés réduisent drastiquement ou abolissent l’activité, confirmant leurs rôles essentiels.
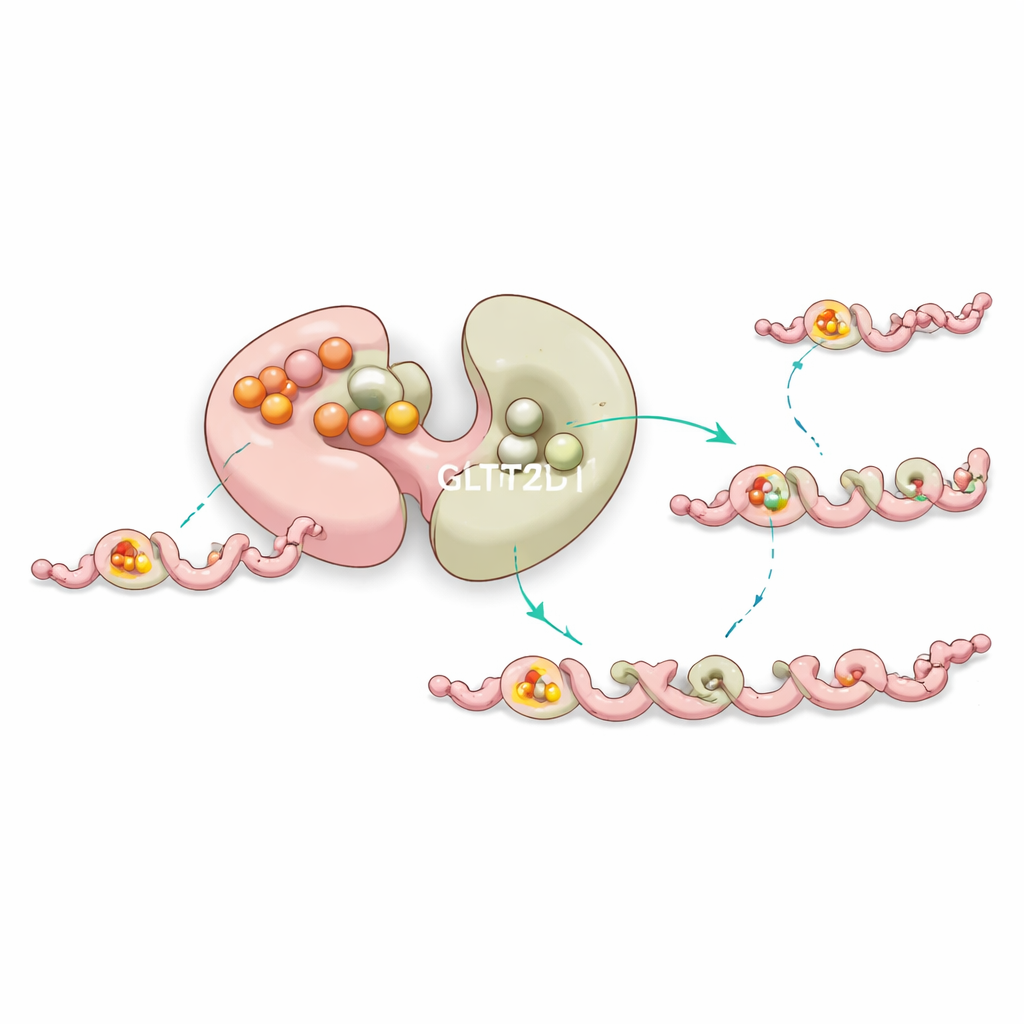
Un stabilisateur intégré et un contrôle à longue distance
Curieusement, le premier lobe de GLT25D1 lie très fortement un donneur de sucre mais n’effectue pas le transfert. Au lieu de cela, des expériences et des simulations informatiques suggèrent que ce site « silencieux » aide à stabiliser l’enzyme et ajuste subtilement le comportement du lobe actif via une communication à longue portée au sein de la protéine. Des mutations près de cette poche non catalytique déstabilisent souvent l’enzyme ou modifient son efficacité, laissant entendre que la nature utilise ce site de liaison supplémentaire comme une forme de contrôle qualité interne pour maintenir la modification du collagène en bon ordre.
Quand le décorateur échoue : liens avec la maladie
En cartographiant des mutations dérivées de patients sur leur modèle structural, les auteurs ont pu expliquer comment des erreurs dans GLT25D1 entraînent des maladies humaines. Certaines mutations suppriment entièrement le lobe catalytique, d’autres déstabilisent le cœur protéique, et d’autres encore atteignent directement les sites de liaison au sucre ou au collagène. Ces défauts réduisent ou éliminent l’ajout de sucre au collagène et ont été associés à des maladies des petits vaisseaux cérébraux, des troubles cognitifs ainsi qu’à des défauts musculaires et squelettiques. Des mutations liées au cancer se regroupent également dans des régions cruciales, suggérant qu’une décoration altérée du collagène peut influencer la croissance et la dissémination tumorales.
Pourquoi cela compte pour la santé et les traitements futurs
En dressant une feuille de route tridimensionnelle détaillée de GLT25D1 en action, ce travail explique comment des petites étiquettes sucrées sont ajoutées au collagène et pourquoi cette étape est si importante pour l’intégrité des tissus. Pour le grand public, le message clé est que de minuscules changements chimiques sur le collagène peuvent avoir des effets disproportionnés sur les vaisseaux sanguins, les os et possiblement le risque de cancer. La carte structurale de GLT25D1 offre désormais une boussole pour diagnostiquer des variantes nocives et pour concevoir des thérapies — qu’il s’agisse de petites molécules stabilisant des enzymes défaillantes ou de stratégies basées sur les gènes — qui pourraient un jour corriger à la source les défauts d’étiquetage sucré du collagène.
Citation: Sun, H., Zhang, M., Shi, Y. et al. Molecular basis of collagen galactosylation by GLT25D1. Nat Commun 17, 2426 (2026). https://doi.org/10.1038/s41467-026-69234-1
Mots-clés: glycosylation du collagène, GLT25D1, matrice extracellulaire, maladie vasculaire, structure cryo‑EM