Clear Sky Science · fr
MYC module la diffusion de TOP2A pour favoriser la détection des substrats et son activité
Pourquoi c’est important pour notre ADN
Chaque fois qu’une cellule lit ses gènes, elle tord et enchevêtre son ADN. Si ces nœuds ne sont pas rapidement éliminés, ils peuvent bloquer l’activité génétique et endommager le génome. Cette étude révèle comment une protéine bien connue, liée au cancer et nommée MYC, accélère le mouvement d’une enzyme « démêlante » de l’ADN, TOP2A, à l’intérieur du noyau cellulaire. En découvrant comment MYC suralimente cette enzyme, les chercheurs ouvrent la voie à des approches visant à ralentir sélectivement l’activité génique incontrôlée dans les cellules cancéreuses tout en épargnant les cellules normales.
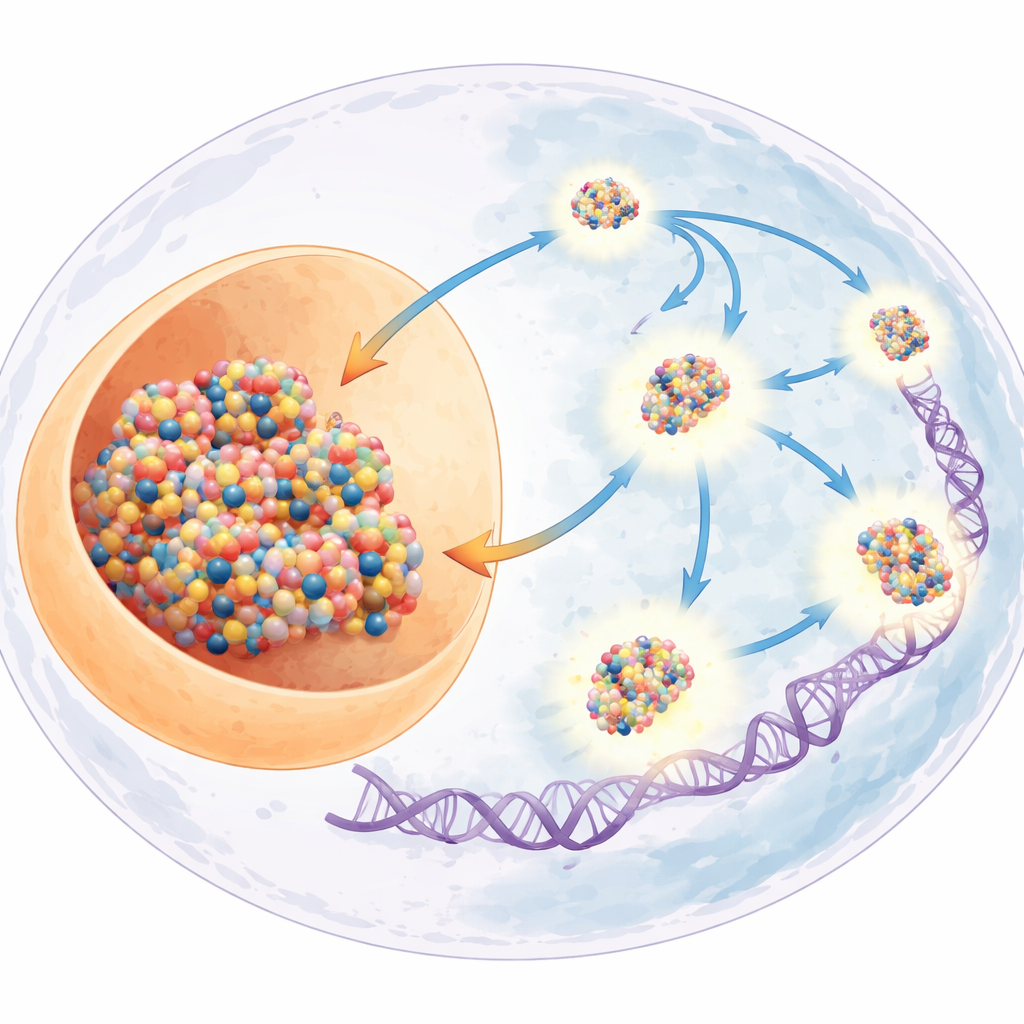
Les nœuds d’ADN et les outils de démêlage de la cellule
L’ADN dans nos cellules est compacté dans un espace réduit, mais il doit constamment être lu, copié et réparé. Ces activités tordent la double hélice et créent des surenroulements et des croisements, un peu comme des boucles dans un cordon de téléphone trop enroulé. Des enzymes spécialisées, appelées topoisomérases, résolvent ce problème en coupant des brins d’ADN, en les faisant passer les uns autour des autres, puis en les recollant. TOP2A, un membre de cette famille, réalise des coupures temporaires dans les deux brins de la double hélice pour éliminer des enchevêtrements majeurs. Parallèlement, MYC agit comme un puissant amplificateur de l’activité génique dans de nombreux cancers, stimulant la transcription au point de générer un stress de torsion supplémentaire sur l’ADN. La grande question abordée ici est la suivante : comment MYC empêche-t‑il sa propre flambée d’activité génique d’être asphyxiée par les nœuds d’ADN qu’elle génère ?
Un équilibre dynamique à l’intérieur du noyau
Les chercheurs ont d’abord cartographié la localisation de TOP2A dans le noyau de cellules cancéreuses humaines. Ils ont constaté que TOP2A fait constamment la navette entre deux zones principales : le nucléole, une région dense où les ribosomes sont assemblés, et des centres de transcription disséminés où de nombreux gènes sont activement lus. Ce mouvement établit un équilibre dynamique, TOP2A pouvant se relocaliser rapidement lorsque le stress sur l’ADN augmente. Lorsque les scientifiques ont artificiellement augmenté le surenroulement, par exemple en désactivant une enzyme apparentée ou en bloquant la capacité de TOP2A à se réinitialiser après une coupure, TOP2A a rapidement quitté le nucléole et s’est accumulée dans le reste du génome, là où elle pouvait agir sur l’ADN soumis au stress. Fait important, ce déplacement corrélait avec une augmentation de molécules de TOP2A chimiquement « prises sur le fait » sur l’ADN, montrant que la relocalisation reflète un engagement de travail réel et non un simple dérive passive.
Trois modes de mouvement pour TOP2A
En utilisant le suivi de molécules uniques dans des cellules vivantes, l’équipe a montré que TOP2A ne se déplace pas de manière homogène. Elle existe en réalité en trois états diffusifs. Un état « lié » bouge à peine et correspond à TOP2A clampée sur la chromatine. Un état « lent » erre à l’intérieur de très petites régions correspondant à la taille et à la localisation des condensats de transcription — ces pôles semblables à des gouttelettes où la machinerie de transcription se concentre. Un état « rapide » se déplace plus librement dans le nucléoplasme. Le nucléole contient principalement des TOP2A lentes et liées, tandis que le reste du noyau présente un mélange des trois états. Quand TOP2A était piégée sur l’ADN par un médicament, la fraction liée augmentait au détriment des états plus rapides. Ensemble, ces observations suggèrent que TOP2A se déplace rapidement pour chercher les points problématiques, échantillonne brièvement les condensats de transcription, puis s’engage pleinement sur l’ADN lorsqu’elle trouve un enchevêtrement.
Comment MYC accélère le mouvement de TOP2A
La découverte clé est que MYC agit comme un « accélérateur » de TOP2A. Lorsqu’on a rapidement éliminé MYC des cellules, la diffusion de TOP2A a ralenti aussi bien dans les pools rapides que lents, tandis que son mouvement dans le nucléole — où MYC est rare — n’a pas changé. La fractionnement biochimique a confirmé que, sans MYC, TOP2A a tendance à former des assemblages moléculaires plus volumineux. Dans des expériences in vitro, la TOP2A purifiée peut former des gouttelettes denses rappelant des condensats protéiques. L’ajout de MYC rendait ces gouttelettes plus petites et moins sujettes à se déposer, cohérent avec une moindre agrégation et des complexes plus mobiles. Cet effet ne nécessitait pas un autre partenaire topoisomérase, TOP1, bien que TOP1 puisse rejoindre les mêmes complexes. En bref, MYC limite le nombre de molécules TOP2A qui s’agglomèrent, réduit la taille moyenne des complexes et permet à chaque molécule de TOP2A de diffuser plus rapidement dans l’environnement nucléaire.
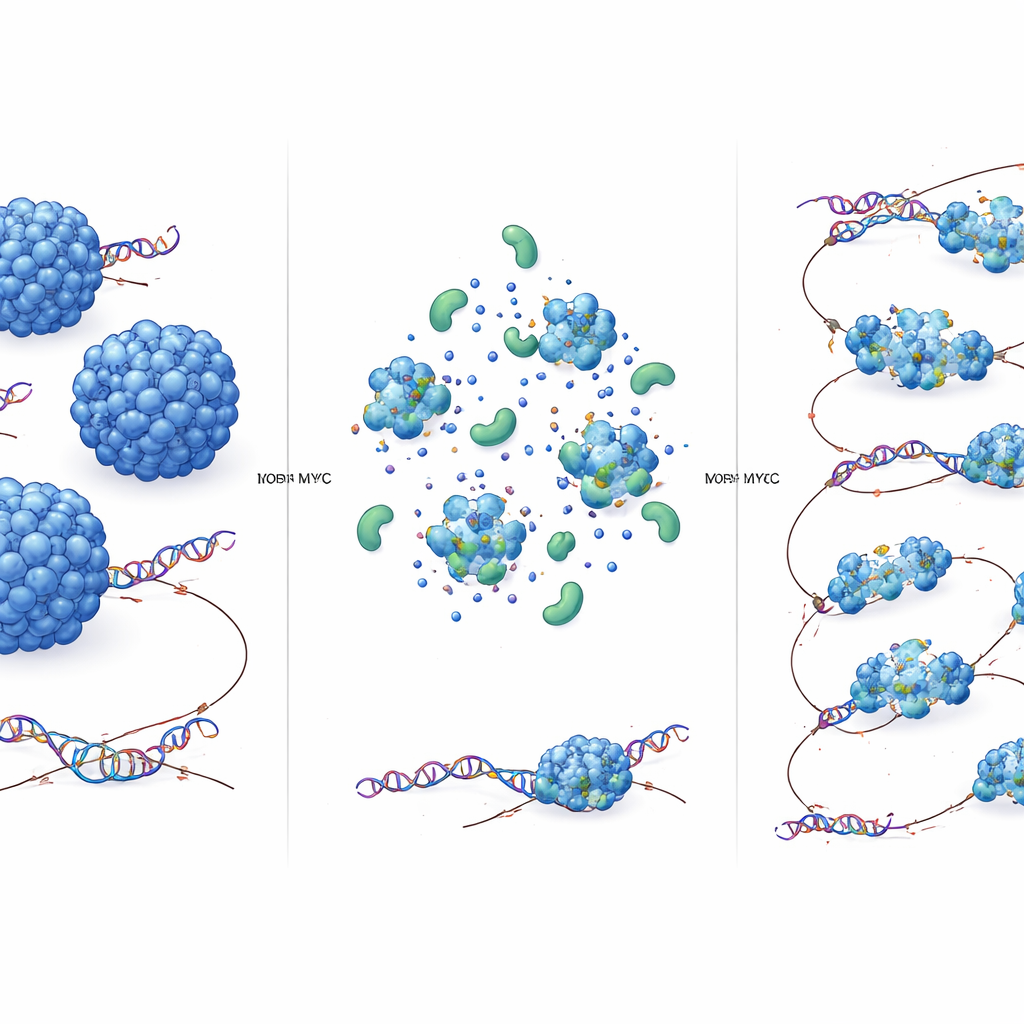
Recherche plus rapide, plus de démêlage d’ADN
Cette accélération a‑t‑elle un impact fonctionnel ? À l’aide d’un dispositif spécialisé de pinces optiques, les auteurs ont construit des croisements d’ADN individuels — de petits modèles de nœuds d’ADN — et ont observé la liaison de TOP2A fluorescente à ces structures. En présence de MYC, TOP2A visitait ces croisements plus fréquemment, indiquant une meilleure détection des substrats. Dans les cellules, un test génomique qui capture les molécules de TOP2A liées de façon covalente à l’ADN a montré une forte activité de TOP2A au début et à la fin des gènes fortement exprimés. Une déplétion rapide de MYC réduisait substantiellement ces complexes actifs TOP2A–ADN, alors que les niveaux globaux de transcription changeaient à peine dans cette fenêtre temporelle. Cela signifie que MYC améliore directement la capacité de TOP2A à trouver et à agir sur l’ADN enchevêtré, plutôt que d’augmenter simplement l’expression génique.
Implications pour le cancer et les traitements futurs
En regroupant ces éléments, l’étude propose une idée simple mais puissante : en maintenant les complexes TOP2A relativement petits, MYC les rend plus diffusifs, leur permet de repérer plus efficacement les nœuds d’ADN et d’être plus actifs aux sites de transcription intense. Dans les cellules saines, ce couplage aide à préserver une activité génique fluide. Dans les cancers pilotés par MYC, cependant, le même mécanisme peut suralimenter le démêlage de l’ADN, permettant aux cellules tumorales de tolérer un stress transcriptionnel extrême. Cibler le partenariat MYC–TOP2A, ou la façon dont MYC reconfigure les condensats de TOP2A, pourrait donc offrir une voie pour affaiblir sélectivement la capacité des cellules cancéreuses à gérer la contrainte de l’ADN sans supprimer les processus essentiels des tissus normaux.
Citation: Cameron, D.P., Jackson, K., Loffreda, A. et al. MYC modulates TOP2A diffusion to promote substrate detection and activity. Nat Commun 17, 2527 (2026). https://doi.org/10.1038/s41467-026-69232-3
Mots-clés: MYC, TOP2A, topologie de l’ADN, condensats de transcription, biologie du cancer