Clear Sky Science · fr
La carence en sclérostine sensibilise les adipocytes blancs aux signaux thermogéniques induisant le beiging chez la souris
Pourquoi réchauffer votre graisse pourrait refroidir la maladie
La plupart d’entre nous considèrent l’os et la graisse corporelle comme deux mondes séparés : l’un nous donne la structure, l’autre stocke l’énergie. Cette étude chez la souris révèle que l’os et la graisse entretiennent une conversation chimique permanente, et qu’une protéine produite par les cellules osseuses peut décider si notre graisse « blanche » reste là à stocker des calories ou se transforme en une graisse plus active et brûleuse de calories, la graisse « beige ». Comprendre ce dialogue caché pourrait ouvrir de nouvelles voies pour lutter simultanément contre l’obésité, le diabète et la perte osseuse.
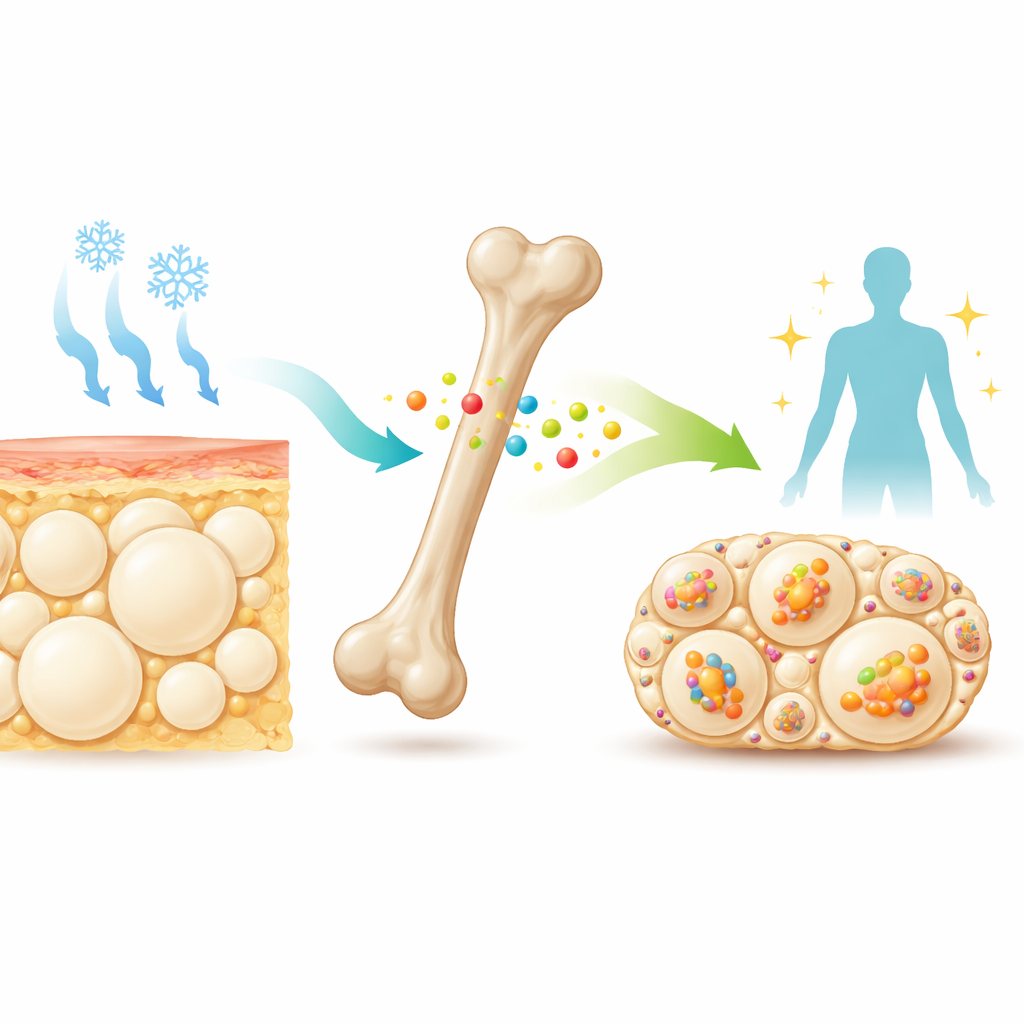
Un messager discret venu de l’os
Au cœur des os, des cellules spécialisées libèrent une petite protéine appelée sclérostine dans la circulation sanguine. Les médecins ciblent déjà la sclérostine avec des médicaments pour renforcer les os chez les patients à risque de fractures. Des travaux antérieurs ont montré que les souris dépourvues de sclérostine sont non seulement très solides au niveau osseux, mais aussi plus maigres et plus sensibles à l’insuline. Leur graisse sous-cutanée, notamment autour des hanches (graisse blanche inguinale), contient de minuscules adipocytes à compartiments multiples ressemblant à la graisse « beige », capable de brûler des combustibles pour produire de la chaleur. Ces indices ont amené les chercheurs à se demander si la sclérostine agit normalement comme un frein à la capacité de l’organisme à convertir la graisse blanche en graisse beige lorsqu’il est exposé au froid ou à des médicaments mimant les signaux nerveux vers la graisse.
Signaux du froid, signaux osseux et allumage de la graisse
L’équipe a exposé des souris normales et des souris dépourvues du gène de la sclérostine (Sost-/-) à un médicament qui active un récepteur spécifique des adipocytes (récepteur β3-adrénergique), ou à un froid léger. Chez les animaux normaux, ces signaux thermogéniques ont augmenté la production de sclérostine dans l’os et ont élevé son taux dans le sang. Cette augmentation était liée à une perte d’os spongieux mais seulement à des changements modestes dans la graisse sous-cutanée. En revanche, les souris déficientes en sclérostine ont montré une réponse beaucoup plus marquée : leur graisse inguinale a capté davantage de glucose, libéré plus d’acides gras, réduit de taille et s’est remplie de cellules de type beige riches en mitochondries, les centrales énergétiques cellulaires. Les principaux gènes thermogéniques se sont activés plus fortement chez ces souris, en particulier dans la graisse sous-cutanée, tandis que la graisse brune classique restait largement inchangée.
Ajuster la combustion des graisses via un interrupteur partagé
Pour comprendre comment la sclérostine exerce ce contrôle, les chercheurs se sont concentrés sur la β-caténine, une protéine impliquée dans la voie de signalisation Wnt que la sclérostine supprime normalement dans l’os. Dans la graisse, l’activation de la β‑caténine après la naissance a poussé les cellules blanches vers un état de type beige et a renforcé leur réponse aux signaux β3-adrénergiques, mais cet effet a disparu quand les souris étaient hébergées à une température thermoneutre où l’organisme n’a plus besoin de chaleur supplémentaire. Inversement, la suppression de la β‑caténine spécifiquement dans les adipocytes de souris déficientes en sclérostine a effacé leur graisse beige, rétabli des adipocytes blancs de plus grande taille et annulé les améliorations de l’insuline et des taux d’acides gras. Ces expériences suggèrent que, lorsque la sclérostine est faible, la β‑caténine dans les adipocytes devient un levier intracellulaire important qui rend la graisse blanche plus réceptive aux signaux thermogéniques.
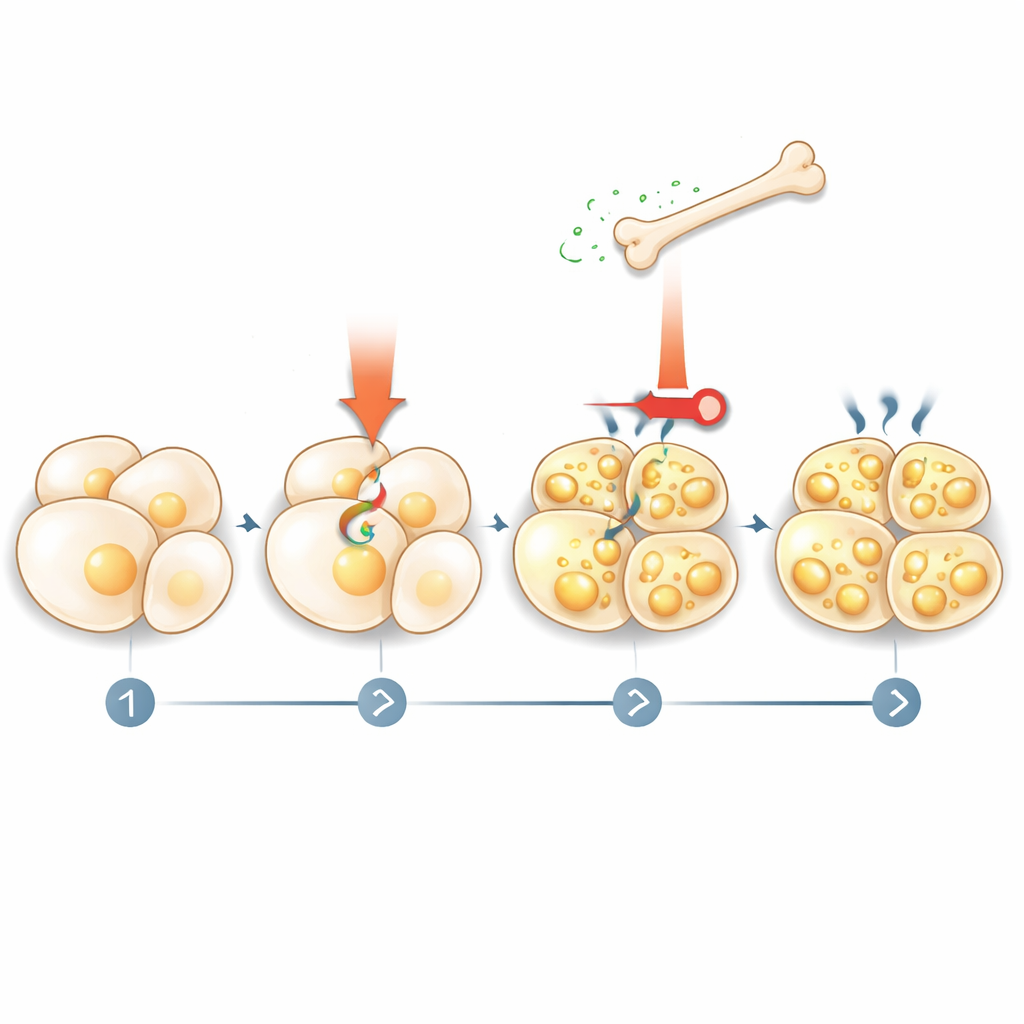
Comment la graisse répond à l’os
L’histoire ne s’est pas arrêtée à l’os disant à la graisse quoi faire. L’équipe a constaté que la stimulation thermogénique active la dégradation des lipides (lipolyse), libérant des acides gras dans le sang. Ces acides gras agissent ensuite sur les cellules osseuses via un récepteur nucléaire appelé PPARγ, augmentant la production de sclérostine. Lorsque les chercheurs ont bloqué la lipolyse dans les adipocytes ou supprimé PPARγ des cellules osseuses, les médicaments mimant le froid n’ont plus pu élever les niveaux de sclérostine. Cela révèle une boucle de rétroaction : les signaux thermogéniques déclenchent la libération de carburant par la graisse, ce carburant dit à l’os de sécréter plus de sclérostine, et la sclérostine freine ensuite l’activation supplémentaire et le beiging de la graisse.
Associer médicaments os et graisse pour la santé métabolique
Enfin, les chercheurs ont testé si interrompre cette boucle pouvait être utile dans un contexte de maladie. Des souris obèses alimentées avec un régime riche en graisses ont reçu une faible dose de mirabégron (un médicament β3‑adrénergique déjà utilisé pour des problèmes de vessie), un anticorps neutralisant la sclérostine (romosozumab, approuvé pour l’ostéoporose), ou les deux. Alors que chaque médicament seul avait des effets modestes, la combinaison a réduit la masse grasse dans des dépôts clés, orienté la graisse vers des cellules plus petites et plus actives, abaissé l’insuline, les triglycérides et le cholestérol, et préservé la solidité osseuse. Un hébergement au chaud, qui réduit le besoin de chaleur de l’organisme, a largement effacé les bénéfices métaboliques liés à la perte de sclérostine, soulignant que cette voie compte surtout lorsque des signaux thermogéniques sont présents.
Ce que cela signifie pour les traitements futurs
En termes simples, ce travail montre que l’os n’est pas seulement un échafaudage passif mais un régulateur actif de la quantité d’énergie que les adipocytes brûlent. La sclérostine fonctionne comme un bouton de réglage qui limite l’activité de la graisse thermogénique, et donc l’utilisation de carburant. Baisser ce bouton — par des moyens génétiques ou pharmacologiques — rend certaines réserves de graisse blanche plus disposées à passer en mode production de chaleur quand l’organisme est stimulé par le froid ou des médicaments spécifiques. Parce que la même intervention peut renforcer les os et améliorer la santé métabolique chez la souris, des combinaisons soigneusement conçues de thérapies ciblant l’os et la graisse pourraient un jour aider à traiter l’obésité, le diabète et l’ostéoporose ensemble, plutôt qu’une maladie à la fois.
Citation: Choquette, G.M., Kim, S.P., Wilkinson, K.J. et al. Sclerostin deficiency sensitizes white adipocytes to thermogenic signals that induce beiging in mice. Nat Commun 17, 2394 (2026). https://doi.org/10.1038/s41467-026-69227-0
Mots-clés: sclérostine, graisse beige, communication os–graisse, thermogenèse, maladie métabolique