Clear Sky Science · fr
Synthèse locale de PI(4,5)P2 par des isoformes de PIPKIγ associés aux septines contrôle l’association du centralspindlin au midbody pendant la cytokinèse
Comment les cellules terminent leur séparation en deux
La cytokinèse — le pincement final qui divise une cellule en deux — peut sembler aller de soi, mais lorsqu’elle déraille elle contribue au développement du cancer et d’autres pathologies. Cette étude révèle comment un ensemble particulier de molécules agit comme des contremaîtres sur le pont étroit reliant deux cellules nouvelles, en veillant à ce que la séparation s’achève proprement plutôt que de se rétracter ou de s’interrompre.
Le pont final entre cellules filles
Après que la cellule a dupliqué son matériel génétique et séparé ses chromosomes, elle doit se diviser physiquement. Un anneau contractile de filaments protéiques se resserre autour du milieu de la cellule, formant un sillon de division appelé furrow de clivage. À mesure que ce sillon se referme, les deux cellules filles restent reliées par un fin pont intercellulaire contenant un cœur dense, le midbody. Le midbody est une structure minuscule mais complexe composée de microtubules groupés, de protéines échafaudées et de lipides de signalisation ; il sert à la fois d’attache et de centre de contrôle qui coordonne les dernières étapes de la division et la coupure finale entre cellules. 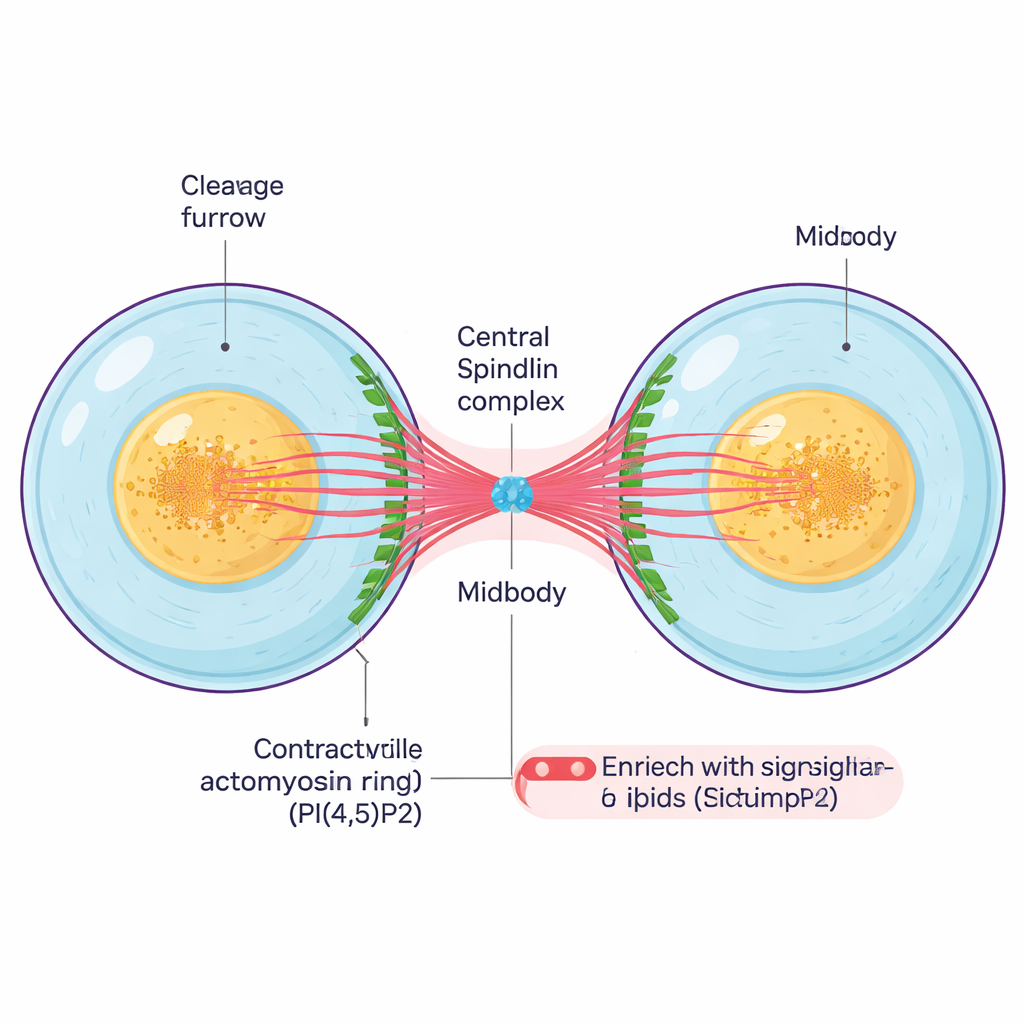
Un signal lipidique qui doit être au bon endroit
Un acteur clé de ce processus est une molécule lipidique de signalisation dans la membrane cellulaire, la PI(4,5)P2. Ce lipide aide à ancrer de nombreuses protéines qui construisent et contractent l’anneau et stabilisent le pont. La question est de savoir comment la cellule contrôle l’emplacement et le moment d’apparition de la PI(4,5)P2, étant donné qu’elle peut diffuser dans la membrane. Les auteurs se sont intéressés aux enzymes appelées kinases PIP de type I, qui synthétisent la PI(4,5)P2, et en particulier au gène PIPKIγ, qui existe sous plusieurs formes d’épissage légèrement différentes. En réduisant sélectivement chaque kinase dans des cellules humaines et en observant les effets par microscopies avancées, ils montrent que PIPKIγ joue un rôle particulier tard dans la cytokinèse, lorsque le pont et le midbody se forment, même si cela n’altère pas fortement les niveaux globaux de PI(4,5)P2 à la surface cellulaire.
Les échafaudages de septines recrutent une enzyme spécialisée
L’équipe a découvert que deux variantes d’épissage de PIPKIγ, appelées i3 et i5, jouent le rôle d’outils de précision amenés au bon endroit par des protéines structurales nommées septines. Les septines forment des filaments et des anneaux qui contribuent à façonner le pont et à organiser d’autres composants. Des expériences biochimiques d’arrachement et des images cellulaires montrent que PIPKIγ-i3 et PIPKIγ-i5 se lient physiquement aux complexes de septines et décorent les filaments de septines, alors que d’autres variants de PIPKIγ ne le font pas. Lorsque les chercheurs ont muté deux acides aminés spécifiques dans ces inserts d’épissage, les enzymes ne pouvaient plus se lier aux septines. Dans les cellules en division, les PIPKIγ-i3/i5 normaux passent d’un motif membranaire diffus à une concentration au niveau du sillon de clivage, puis délimitent le pont intercellulaire et le midbody en synchronie avec les septines et une autre protéine échafaudée, l’anilline. L’élimination uniquement des variants i3 et i5 disperse l’anilline et les septines le long du pont, loin du midbody, et de nombreuses cellules échouent la cytokinèse, se retrouvant avec plusieurs noyaux.
La production lipidique locale verrouille la machinerie de division
Pour tester si ces effets dépendaient de la production locale de PI(4,5)P2, les auteurs ont mesuré la PI(4,5)P2 autour du midbody et manipulé des enzymes qui ajoutent ou retirent ce lipide. La déplétion de PIPKIγ-i3/i5 réduit la PI(4,5)P2 au midbody, tandis que le blocage d’une enzyme dégradant la PI(4,5)P2 a l’effet inverse. De façon importante, restaurer une forme d’épissage catalytiquement active de PIPKIγ, capable de se lier aux septines, rétablit le regroupement correct de l’anilline et des septines au niveau du pont, alors que des mutants catalytiquement inactifs ou déficients pour la liaison aux septines ne le font pas. Grâce à des images en direct et à une technique de microscopie d’expansion qui gonfle physiquement l’échantillon pour révéler des détails fins, l’équipe montre que sans PIPKIγ-i3/i5, les septines n’envahissent plus les microtubules du pont, le pont devient plus court et moins groupé, et un complexe crucial appelé centralspindlin n’arrive pas à rester étroitement associé au midbody. 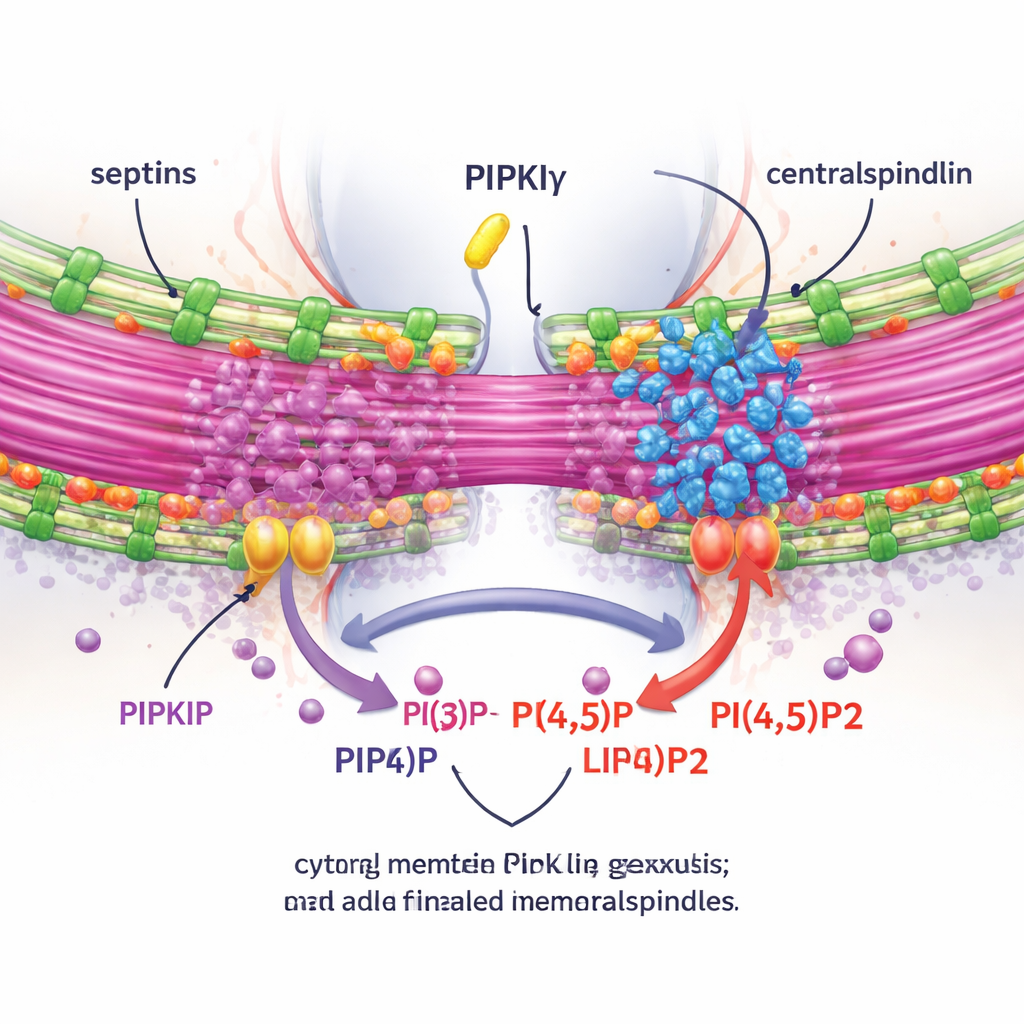
Construire un point de contrôle pour une coupure nette
Le centralspindlin aide à relier les microtubules du midbody à la membrane environnante et régule de petites molécules commutatrices qui contrôlent la forme cellulaire. L’étude montre que le centralspindlin s’associe à la fois aux septines et à PIPKIγ, et que la perte de l’un ou de l’autre affaiblit de façon similaire sa présence au midbody. Les auteurs proposent que les septines recrutent PIPKIγ-i3/i5 au niveau du sillon ingressé, où ces enzymes créent une zone concentrée de PI(4,5)P2. Cette réserve lipidique locale stabilise alors l’anilline, le centralspindlin et les septines à proximité du midbody, favorise le regroupement et la stabilisation des microtubules du pont, et permet au pont intercellulaire de mûrir jusqu’à la coupure finale d’abscission. Si ce système est perturbé, la PI(4,5)P2 apparaît aux mauvais endroits, les protéines échafaudées se dispersent, les microtubules sont mal groupés, et la cytokinèse échoue souvent.
Pourquoi cela compte au-delà de la biologie cellulaire fondamentale
En identifiant comment des variants d’épissage spécifiques de PIPKIγ et les septines coopèrent pour générer un signal lipidique local au midbody, ce travail explique comment les cellules imposent une précision spatiale à une molécule de signalisation très mobile. Cette précision est cruciale pour l’achèvement sûr de la division cellulaire, aidant à prévenir des més-ségréations chromosomiques et des nombres cellulaires anormaux susceptibles de favoriser le développement tumoral. Les mêmes structures du midbody influencent aussi le destin cellulaire et la prolifération après la division, si bien que comprendre leur assemblage ouvre de nouvelles voies pour explorer comment des erreurs dans ces échafaudages nanoscopiques pourraient contribuer au cancer et, potentiellement, pour manipuler des cellules souches.
Citation: Russo, G., Hümpfer, N., Jaensch, N. et al. Local PI(4,5)P2 synthesis by septin-associated PIPKIγ isoforms controls centralspindlin association with the midbody during cytokinesis. Nat Commun 17, 1482 (2026). https://doi.org/10.1038/s41467-026-69224-3
Mots-clés: division cellulaire, cytokinèse, lipides de signalisation, septines, biologie du cancer