Clear Sky Science · fr
Édition stéréosélective photocatalytique des alcynes en molécules 3D via une épimérisation dynamique médiée par transfert d'atome d'hydrogène
Pourquoi transformer des molécules plates en formes 3D est important
De nombreux médicaments modernes partent de morceaux moléculaires plats, faciles à synthétiser mais pas toujours idéaux dans l'organisme. Les chercheurs en découverte de médicaments ont appris que des architectures compactes tridimensionnelles se comportent souvent mieux : elles peuvent s'insérer plus précisément dans des cibles biologiques, se distribuer différemment dans le corps et parfois entraîner moins d'effets secondaires. Cet article décrit une nouvelle méthode activée par la lumière pour plier des « fils » moléculaires plats et simples en cages 3D complexes en une seule étape, ce qui peut accélérer la recherche de médicaments de nouvelle génération et de matériaux fonctionnels.
Des lignes droites aux petites cages
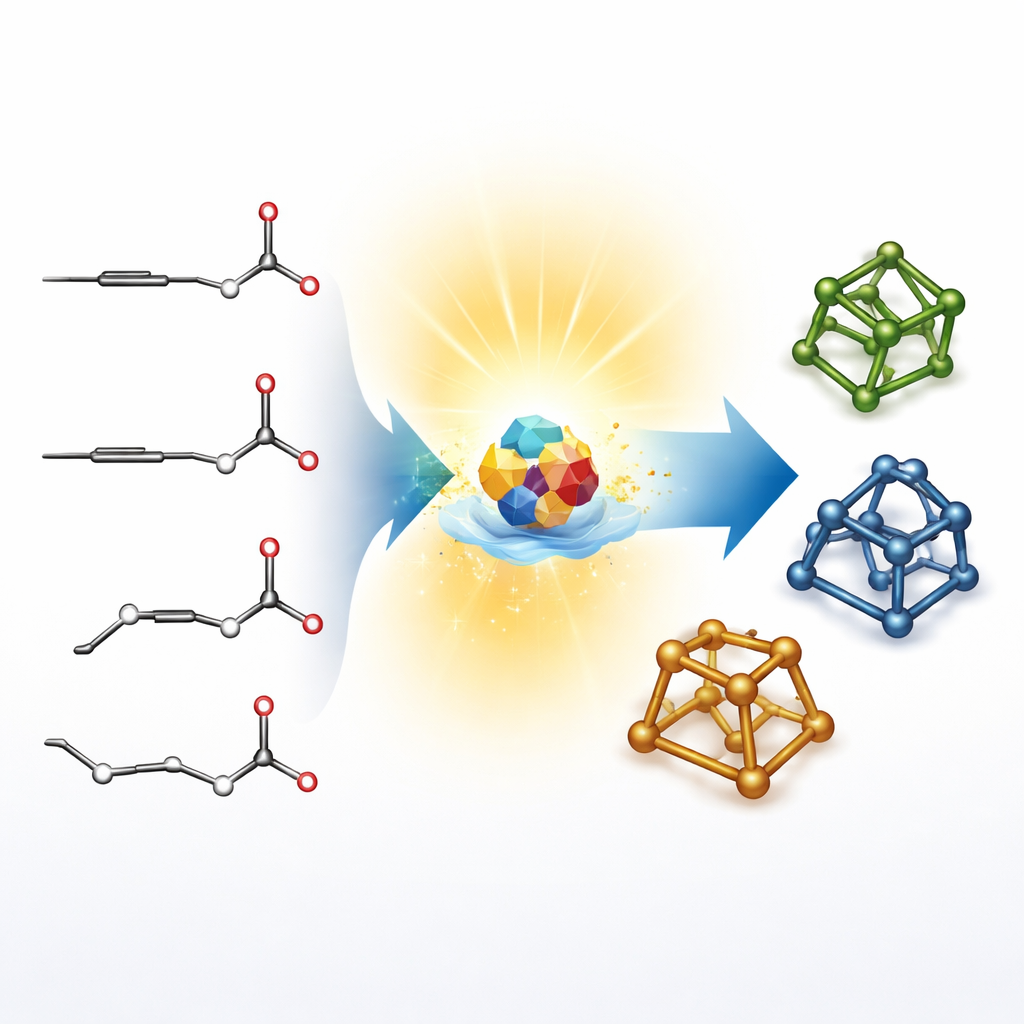
La plupart des méthodes classiques pour construire ces structures en forme de cage, appelées cycles pontés, suivent une voie indirecte : les chimistes préparent d'abord des systèmes cycliques relativement plats, puis les relient dans une seconde étape. Cette stratégie en deux temps fonctionne, mais elle est lente et limite les formes accessibles. Les auteurs partent au contraire d'ingrédients très simples et unidimensionnels : des alcynes linéaires (liaisons carbone–carbone triples) et des aldéhydes (petites unités carbone–oxygène). Leur objectif est de passer directement de ces chaînes droites à des architectures 3D compactes en une seule opération, évitant les détours habituels et ouvrant de nouveaux « espaces chimiques » utiles pour la conception de médicaments.
Laisser la lumière faire le travail lourd
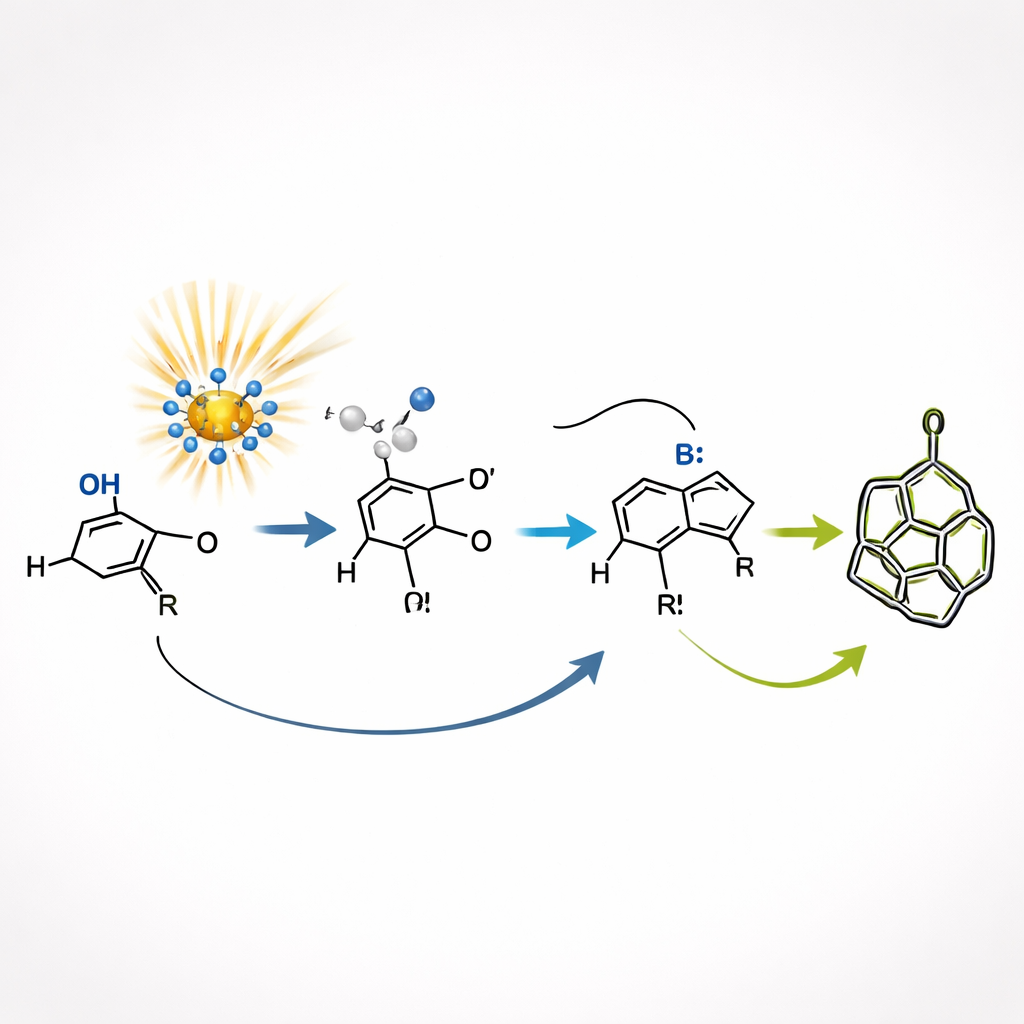
L'équipe exploite un catalyseur photosensible particulier à base de polyoxométalate, la décatungstate. Sous une lumière violette, ce catalyseur peut arracher un atome d'hydrogène au partenaire aldéhyde, générant brièvement un fragment hautement réactif. Ce fragment s'additionne à l'alcyne, se replie sur lui-même et se referme en un cycle à cinq membres. À lui seul, ce premier pas de formation du cycle donne un mélange désordonné de dispositions 3D aux atomes clés. L'astuce est que le même système activé par la lumière peut ensuite réarranger ces dispositions en temps réel en arrachant et en rendant répétitivement des atomes d'hydrogène, ce qui permet au mélange d'évoluer vers les formes les plus stables.
Édition 3D auto-correctrice
Au cœur de la découverte se trouve une sorte d'auto-correction intégrée, connue sous le nom de résolution cinétique dynamique. L'intermédiaire cyclique initial existe sous deux formes 3D étroitement liées, qui ne diffèrent que par l'orientation spatiale des atomes. Le déplacement rapide d'hydrogène, activé par la lumière, interconvertit rapidement ces formes, tandis qu'une étape de fermeture assistée par une base favorise seulement l'une d'entre elles pour la formation finale de la cage. Ainsi, l'intermédiaire « préféré » est constamment consommé pour donner un produit bicyclique unique et bien défini, tandis que la forme moins favorisée est continuellement reconvertie en sa partenaire. Cette interaction entre inversion réversible de conformation et piégeage sélectif fournit des produits avec un excellent contrôle de l'orientation à plusieurs positions, même si la première étape est assez peu sélective.
Construire des architectures 3D diverses et utiles
Les auteurs montrent que cette approche photodirigée fonctionne pour une large gamme de matériaux de départ, décorant les cages obtenues avec de nombreux groupes chimiques prisés comme points de manipulation. Ils obtiennent deux familles d'architectures, les bicyclo[2.2.1]heptanones et les bicyclo[3.2.1]octanones, qui sont toutes deux des blocs de construction recherchés en chimie médicinale. Ces structures se retrouvent dans des produits naturels, des catalyseurs et des matériaux. L'équipe démontre en outre que leurs cages 3D peuvent être transformées en composés plus élaborés, y compris un intermédiaire clé pour un matériau électroluminescent et une version rigidifiée d'un antagoniste connu d'un récepteur cérébral. Dans un cas, le remplacement d'un cycle flexible du médicament par une cage 3D nouvellement formée a même amélioré modérément sa puissance biologique.
Un raccourci vers des formes moléculaires plus riches
En termes simples, ce travail montre comment prendre des « bâtons » moléculaires droits et simples et, à l'aide de la lumière et d'un catalyseur malin, les plier en « sculptures » 3D précises en un seul geste. Le processus remplit deux fonctions à la fois : il construit l'ossature sous-jacente et ajuste la disposition spatiale des atomes, le tout dans des conditions douces. Parce que les alcynes sont des ingrédients courants et peu coûteux, cette stratégie pourrait devenir un raccourci général pour transformer des matières premières bon marché en architectures complexes de type médicament. À mesure que les chimistes explorent davantage le monde des molécules tridimensionnelles, des outils comme celui-ci pourraient jouer un rôle clé pour concevoir des médicaments et des matériaux plus performants par conception.
Citation: Gu, Z., Zeng, T., Yuan, Z. et al. Photocatalytic Stereoselective Editing of Alkynes to 3D Molecules via Hydrogen Atom Transfer-Mediated Dynamic Epimerization. Nat Commun 17, 2518 (2026). https://doi.org/10.1038/s41467-026-69219-0
Mots-clés: photocatalyse, transfert d'atome d'hydrogène, échafaudages moléculaires 3D, résolution cinétique dynamique, chimie médicinale