Clear Sky Science · fr
L’inhibiteur pan‑RAF exarafenib cible les BRAF de classe II/III dans les NSCLC et révèle une résistance ARAF‑KSR1 ainsi que des stratégies de combinaison
Pourquoi cette recherche compte pour les patients atteints de cancer du poumon
La plupart des gens ont entendu parler de médicaments anticancéreux ciblés qui s’attaquent à des altérations génétiques précises. Mais pour de nombreux patients atteints de cancer du poumon, en particulier ceux dont les tumeurs portent des mutations moins fréquentes du gène BRAF, les traitements ciblés actuels sont souvent inefficaces. Cette étude présente un nouveau médicament expérimental, l’exarafenib, conçu pour viser un ensemble plus large de tumeurs pilotées par BRAF, et explique comment les cellules cancéreuses tentent d’y échapper — révélant des traitements combinés susceptibles de maintenir ces tumeurs sous contrôle plus longtemps.
Une majorité cachée de mutations négligées
Les chercheurs ont commencé par une question simple : quelle est la fréquence des différents types de mutations BRAF dans les cancers avancés, et en particulier dans le cancer du poumon non à petites cellules (CPNPC) ? En utilisant une très grande base de données d’analyses sanguines (liquid biopsy) de plus de 160 000 patients, ils ont analysé des fragments d’ADN tumoral circulant dans le sang. Ils ont constaté que, dans le cancer du poumon, les mutations BRAF surviennent chez environ 4–5 % des patients, ce qui représente néanmoins plusieurs milliers de personnes dans le monde. Fait crucial, environ deux tiers de ces tumeurs pulmonaires portaient des mutations BRAF dites de classe II et III — des types que les médicaments BRAF approuvés ne ciblent pas efficacement. Les patients porteurs de l’une de ces classes, en particulier la classe II, avaient tendance à vivre moins longtemps que ceux porteurs de la mutation plus connue de classe I, probablement parce que les patients de classe I ont accès à des thérapies ciblées établies, tandis que les patients de classe II/III reçoivent majoritairement une chimiothérapie ou une immunothérapie standard.
Un médicament de nouvelle génération qui cible l’ensemble de la voie
BRAF fait partie d’un relais de protéines (la voie MAPK) qui transmet des signaux de croissance de la surface cellulaire jusqu’au noyau. Beaucoup des médicaments BRAF existants ont été conçus pour bloquer une seule forme mutante et peuvent même stimuler involontairement des protéines apparentées dans les cellules normales. Exarafenib a été conçu différemment : c’est un inhibiteur « pan‑RAF » destiné à inhiber plusieurs membres de la famille RAF (ARAF, BRAF et CRAF) sous leurs formes monomériques et dimériques, tout en épargnant la plupart des autres enzymes cellulaires. Dans des tests biochimiques portant sur des centaines de kinases humaines, l’exarafenib a fortement bloqué les trois protéines RAF mais a présenté peu d’effets hors cible, ce qui suggère un profil de sécurité plus propre que les anciens composés pan‑RAF.
Effets puissants sur des modèles de tumeurs difficiles à traiter
L’équipe a testé l’exarafenib sur une série de lignées cellulaires et de modèles murins portant différentes mutations BRAF et RAS, y compris des tumeurs dérivées de patients. En cultures cellulaires, l’exarafenib a freiné la croissance et supprimé la signalisation MAPK non seulement dans les cellules cancéreuses classiques BRAF V600E, mais aussi dans celles porteuses de mutations de classe II et III et dans de nombreuses cellules mutées pour RAS qui manquent actuellement de bonnes options ciblées. Chez des souris porteuses de tumeurs pulmonaires avec ces altérations, l’exarafenib a réduit ou ralenti la croissance tumorale de façon dépendante de la dose et a montré des corrélations nettes entre les niveaux de médicament, la suppression de la voie et la réponse tumorale. Des données cliniques précoces provenant de deux patients atteints d’un cancer du poumon avancé à mutation BRAF — l’un avec une fusion BRAF rare et l’autre avec une mutation ponctuelle de classe II — ont montré des réponses partielles et un soulagement des symptômes significatif, soutenant la pertinence des travaux précliniques.
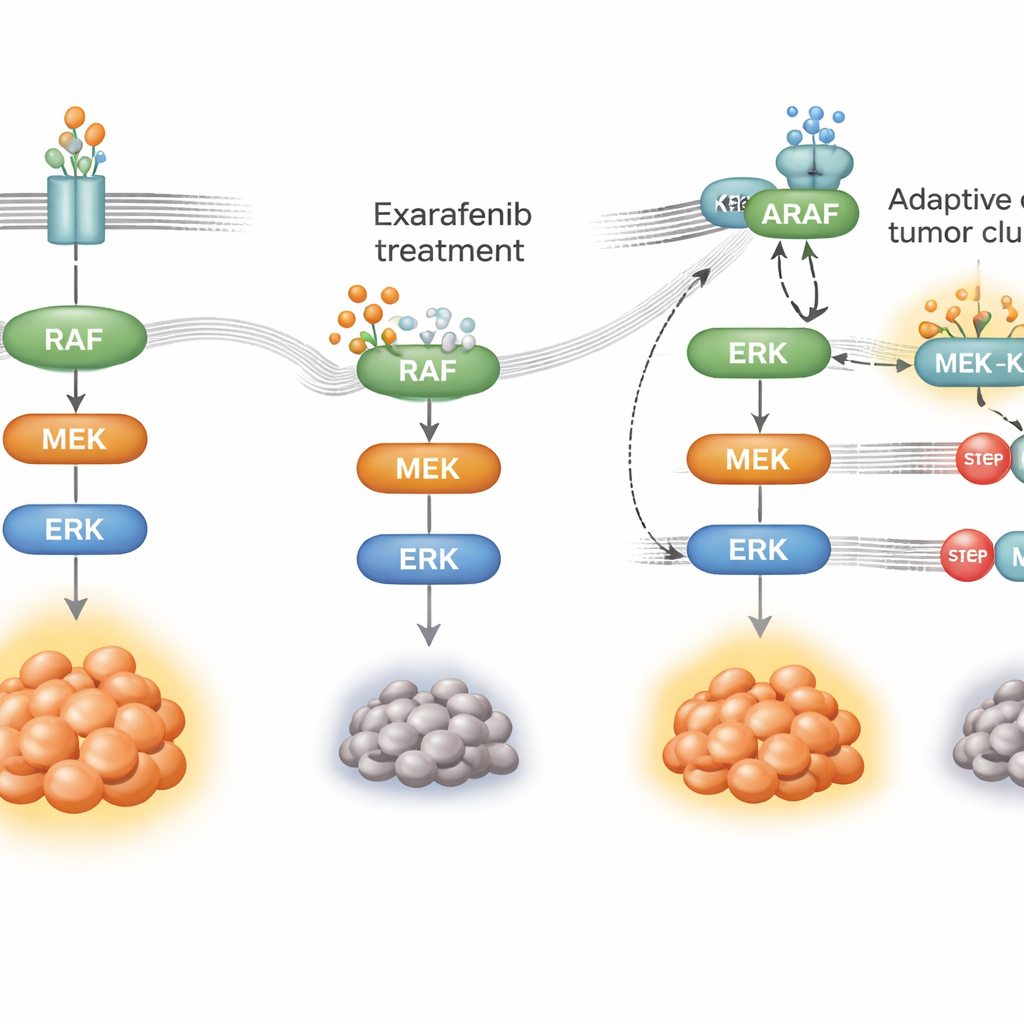
Comment le cancer apprend à contourner le médicament
Aucune thérapie ciblée n’est efficace indéfiniment ; les cellules cancéreuses s’adaptent. Pour comprendre comment les tumeurs pourraient résister à l’exarafenib, les chercheurs ont exposé des cellules de cancer pulmonaire mutées pour BRAF au médicament pendant des mois, jusqu’à l’émergence de populations résistantes. Ces cellules dépendaient toujours de la même voie de croissance mais l’avaient réacheminée. Plutôt que de dépendre principalement du BRAF muté, elles ont augmenté l’activité d’un commutateur en amont appelé RAS et se sont tournées vers l’utilisation d’un autre membre de la famille, ARAF, conjointement avec une protéine échafaudage nommée KSR1. Sous la pression du médicament, ARAF et KSR1 formaient des complexes serrés qui aidaient à maintenir le relais MAPK en fonctionnement même lorsque l’exarafenib était lié. Lorsque les scientifiques ont silencé sélectivement ARAF ou KSR1, ou réduit l’activité de RAS, les cellules résistantes sont redevenues sensibles à l’exarafenib et les signaux de survie se sont effondrés.
Stratégies de combinaison pour devancer la résistance
Munie de cette cartographie mécanistique, l’équipe a recherché des médicaments partenaires capables de bloquer la voie à des points d’étranglement partagés par les voies d’origine et de contournement. Ils ont constaté que l’association de l’exarafenib avec des inhibiteurs de MEK ou d’ERK — étapes clés en aval dans le relais MAPK — produisait une forte synergie dans de nombreux modèles cellulaires et murins, y compris des tumeurs intrinsèquement moins sensibles ou ayant acquis une résistance. Ces combinaisons maintenaient la voie fermée plus longtemps, déclenchaient davantage de mort cellulaire et, chez l’animal, fonctionnaient souvent aussi bien ou mieux que des doses plus élevées d’exarafenib seul, sans toxicité supplémentaire évidente. Des agents ciblant directement RAS ont également renforcé les effets de l’exarafenib dans des modèles où RAS était clairement le moteur de la résistance, suggérant une autre tactique cliniquement prometteuse.
Ce que cela signifie pour les patients
Pour les personnes atteintes de CPNPC portant des mutations BRAF de classe II ou III — ou des fusions BRAF complexes et des co‑mutations RAS — il n’existe actuellement pas de thérapies ciblées approuvées, et les résultats sont inférieurs à ceux des patients porteurs d’altérations plus courantes. Cette étude apporte un solide argument scientifique en faveur du fait que l’exarafenib pourrait combler cette lacune en supprimant largement la signalisation pilotée par RAF. Elle explique aussi comment les tumeurs peuvent s’adapter via un contournement ARAF‑KSR1 et montre que frapper la voie à plusieurs niveaux, en particulier en combinant des inhibiteurs RAF et MEK ou en ajoutant des inhibiteurs de RAS, pourrait permettre un contrôle tumoral plus profond et plus durable. Ensemble, ces acquis tracent une voie vers des essais cliniques visant à proposer des thérapies ciblées combinées et personnalisées à un large groupe de patients atteints de cancer du poumon jusque‑là peu desservis.
Citation: Manabe, T., Bergo, H.C., Li, Q. et al. Pan-RAF inhibitor exarafenib targets BRAF class II/III NSCLC and reveals ARAF-KSR1 resistance and combination strategies. Nat Commun 17, 2484 (2026). https://doi.org/10.1038/s41467-026-69216-3
Mots-clés: Cancer du poumon à mutation BRAF, inhibiteur pan‑RAF, signalisation MAPK, résistance aux médicaments, combinaisons de thérapies ciblées