Clear Sky Science · fr
Ingénierie d’une cytochrome P450 en peroxygénase pour l’hydroxylation sélective des stéroïdes
Fabriquer des médicaments à partir de molécules difficiles à ajuster
Les médicaments stéroïdiens — des anti‑inflammatoires oraux aux thérapies hormonales — font partie des médicaments les plus utilisés au monde. Pourtant, affiner ces molécules en ajoutant un seul atome d’oxygène au bon endroit est notoirement difficile avec la chimie traditionnelle. Cette étude montre comment des scientifiques ont re‑conçu une enzyme naturelle pour qu’elle puisse « polir » précisément des stéroïdes en utilisant du simple peroxyde d’hydrogène, ouvrant potentiellement des voies plus écologiques et moins coûteuses vers des médicaments importants.
Pourquoi les stéroïdes sont si difficiles à personnaliser
Les stéroïdes sont constitués d’un empilement compact d’anneaux carbonés, avec de nombreux liaisons carbone–hydrogène presque identiques. Les méthodes chimiques classiques peinent à cibler une seule de ces liaisons sans affecter les autres, nécessitant souvent des réactifs agressifs, des températures élevées et de multiples étapes de protection qui génèrent des déchets. Pourtant, de petites modifications — comme l’ajout d’un groupe hydroxyle (–OH) à une position spécifique — peuvent modifier profondément le comportement d’un stéroïde dans l’organisme. Les enzymes de la famille des cytochromes P450 sont les spécialistes naturels de ce type d’activation précise des liaisons C–H, mais à l’état naturel elles requièrent généralement des cofacteurs coûteux et des machines de gestion de l’oxygène, ce qui limite leur utilisation directe en production industrielle.
Découverte d’une enzyme prometteuse comme point de départ
Par criblage génomique, les chercheurs ont identifié une P450 autonome, nommée P450stri, provenant d’une bactérie du sol. Contrairement à l’enzyme modèle P450BM3, qui préfère les acides gras courts, P450stri accepte naturellement des molécules stéroïdiennes volumineuses comme la testostérone. Dans ses conditions natives, alimentée par le cofacteur cellulaire NADH, P450stri introduit des hydroxyles en trois positions sur la testostérone, produisant un mélange de produits. Cette capacité intrinsèque à reconnaître les stéroïdes faisait de P450stri un « échafaudage » attractif pour concevoir un catalyseur plus sélectif et adapté à l’industrie.
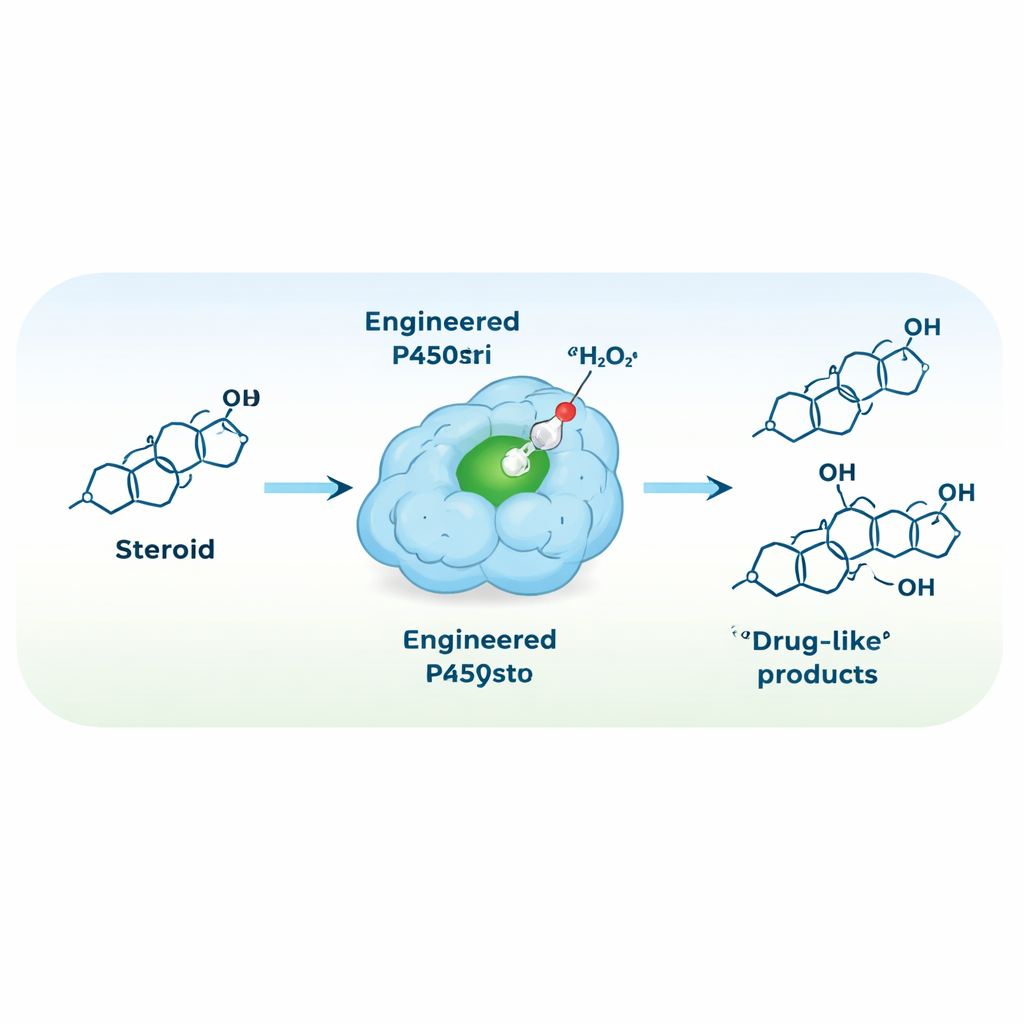
Reprogrammer l’enzyme pour qu’elle fonctionne avec du peroxyde d’hydrogène
Pour simplifier le dispositif réactionnel, l’équipe a cherché à convertir P450stri en peroxygénase — une enzyme qui utilise directement le peroxyde d’hydrogène comme oxydant, supprimant le besoin de cofacteurs et de protéines auxiliaires. Une mutation stratégique unique, remplaçant une phénylalanine volumineuse juste au‑dessus du centre héminique par une alanine plus petite, a créé une variante nommée M1. Ce changement a ouvert de l’espace autour du centre réactif en fer et a, de façon surprenante, rendu l’enzyme à la fois plus tolérante à des niveaux élevés de peroxyde d’hydrogène et bien plus sélective. En mode peroxyde, M1 a converti la testostérone principalement en un seul produit hydroxylé en position 15β, avec environ 94 % de sélectivité — contre 35 % pour l’enzyme d’origine.
Un modèle « Flacon Ronde » pour une conception d’enzyme plus intelligente
Pour améliorer encore les performances, les auteurs ont introduit un concept de conception qu’ils appellent le modèle « Flacon Ronde ». Ils considèrent le site actif où la chimie a lieu comme la base arrondie et les tunnels d’accès étroits comme le col et le bouchon. La base détermine quelle position du stéroïde est modifiée, tandis que le col contrôle la facilité d’accès du stéroïde et du peroxyde d’hydrogène au centre réactif. Guidés par des simulations informatiques et des logiciels de cartographie des tunnels, ils ont ajusté de façon systématique un petit nombre d’acides aminés bordant ces tunnels, en modulant leur taille et leur hydrophobicité. Cette stratégie bidimensionnelle a permis d’obtenir une variante remarquable, M4, qui conserve une forte sélectivité 15β tout en augmentant fortement la vitesse de réaction et en tolérant des concentrations de peroxyde d’hydrogène atteignant plusieurs centaines de millimolaires.
Du plan de travail du laboratoire à des améliorations de stéroïdes à l’échelle
L’enzyme M4 optimisée a ensuite été testée à plus grande échelle sur la testostérone et sur un stéroïde apparenté utilisé dans certains contextes de performance. Dans des mélanges aqueux simples à température ambiante, alimentée uniquement par du peroxyde d’hydrogène, M4 a converti plus de 90 % du matériau de départ et a fourni des produits 15β‑hydroxylés isolés avec des rendements d’environ 75–80 %. Ces conditions sont bien plus douces et propres que les voies chimiques classiques. Enfin, l’équipe a montré qu’en transplantant les mutations clés dans plusieurs P450 apparentés de la même branche évolutive, ils pouvaient les transformer de façon fiable en peroxygénases tout aussi sélectives et efficaces, soulignant la généralité de leurs règles de conception.
Ce que cela signifie pour les futurs médicaments
Pour un non‑spécialiste, la conclusion est que les chercheurs ont appris à une enzyme naturelle à agir comme une « micro‑usine » alimentée au peroxyde, très précise pour modifier des médicaments stéroïdiens. En combinant un modèle conceptuel simple avec des mutations ciblées, ils ont créé une enzyme capable d’ajouter un groupe OH exactement au bon endroit, dans des conditions douces et évolutives, puis ont transféré cette stratégie à des protéines apparentées. Cette approche pourrait simplifier la production de stéroïdes existants, ouvrir des voies vers de nouveaux candidats médicamenteux et servir de modèle pour l’ingénierie d’autres enzymes capables d’activer proprement des liaisons C–H tenaces dans des molécules complexes.
Citation: Tang, T., Wang, R. & Chen, Y. Engineering a cytochrome P450 enzyme as a peroxygenase for selective hydroxylation of steroids. Nat Commun 17, 1996 (2026). https://doi.org/10.1038/s41467-026-69211-8
Mots-clés: biocatalyse des stéroïdes, ingénierie des cytochromes P450, peroxygénase, catalyse par le peroxyde d’hydrogène, hydroxylation sélective