Clear Sky Science · fr
Biologie structurale à l’échelle d’une seule cellule par cristallographie électronique intracellulaire
Voir la forme de la vie, une cellule à la fois
Les protéines sont de minuscules machines qui maintiennent chaque cellule en vie, mais pour comprendre vraiment leur fonctionnement, les scientifiques doivent voir leurs formes tridimensionnelles avec un grand niveau de détail. Traditionnellement, cela implique de purifier d’énormes quantités de protéine et de faire croître de grands cristaux fragiles à l’extérieur de la cellule — un processus souvent lent et sujet à l’échec. Cette étude présente une nouvelle façon de déterminer la structure protéique directement à partir d’un seul cristal à l’intérieur d’une seule cellule, en utilisant des électrons plutôt que des rayons X. Elle ouvre la voie à un avenir où la biologie structurale à haute résolution pourra être pratiquée dans des laboratoires ordinaires, et même au niveau de cellules individuelles.
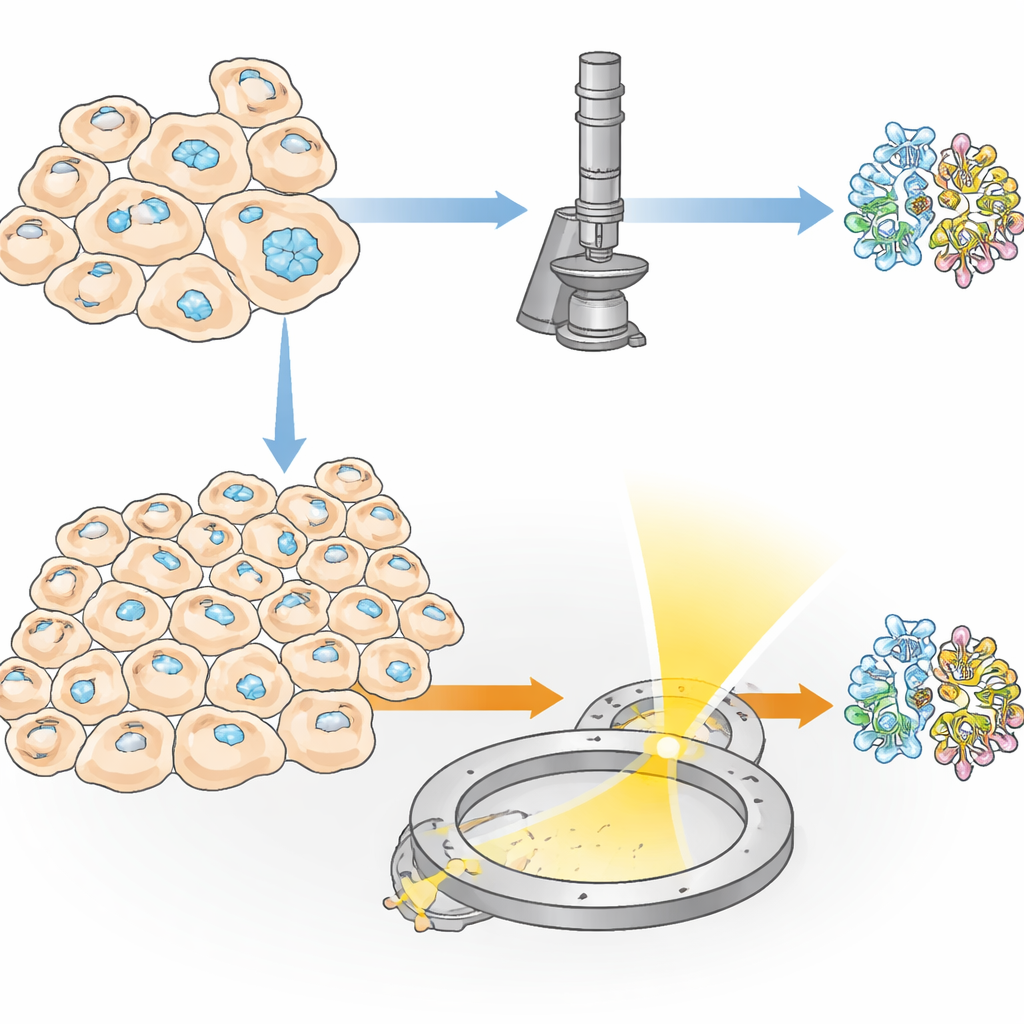
Des cristaux cachés à l’intérieur de cellules vivantes
Certaines protéines s’assemblent naturellement en minuscules cristaux à l’intérieur de cellules vivantes, remplissant des fonctions comme le stockage, la protection ou l’aide à la réponse au stress. Les chercheurs peuvent aussi inciter des cellules à produire de tels cristaux en les modifiant pour qu’elles synthétisent de grandes quantités d’une protéine choisie. Cette cristallisation « in cellulo » présente deux grands avantages : la protéine ne quitte jamais un environnement proche du naturel, et des caractéristiques délicates — comme des décorations glucidiques ou de petites molécules liées — peuvent être préservées là où elles échoueraient souvent dans la cristallisation en éprouvette. Cependant, un obstacle majeur demeure : dans de nombreuses expériences, seule une petite fraction des cellules forme effectivement des cristaux, si bien que les méthodes rayons X traditionnelles exigent des dizaines de milliers de cristaux et, donc, des nombres énormes de cellules.
Une nouvelle voie : des électrons au lieu des rayons X
Les auteurs présentent une méthode qu’ils appellent IncelluloED, qui associe la cristallisation in cellulo à la diffraction électronique tridimensionnelle. Les électrons interagissent bien plus fortement avec la matière que les rayons X, ce qui permet de collecter des données utiles à partir de cristaux à la fois plus petits et moins nombreux. L’équipe a choisi une protéine fongique appelée HEX-1, qui forme naturellement des cristaux hexagonaux aidant à obstruer de minuscules pores entre cellules fongiques sous stress. En produisant cette protéine dans des cellules d’insecte, ils ont créé des cristaux microscopiques réguliers qui ont servi de cas test pour la nouvelle chaîne expérimentale.
Transformer un cristal en une carte détaillée
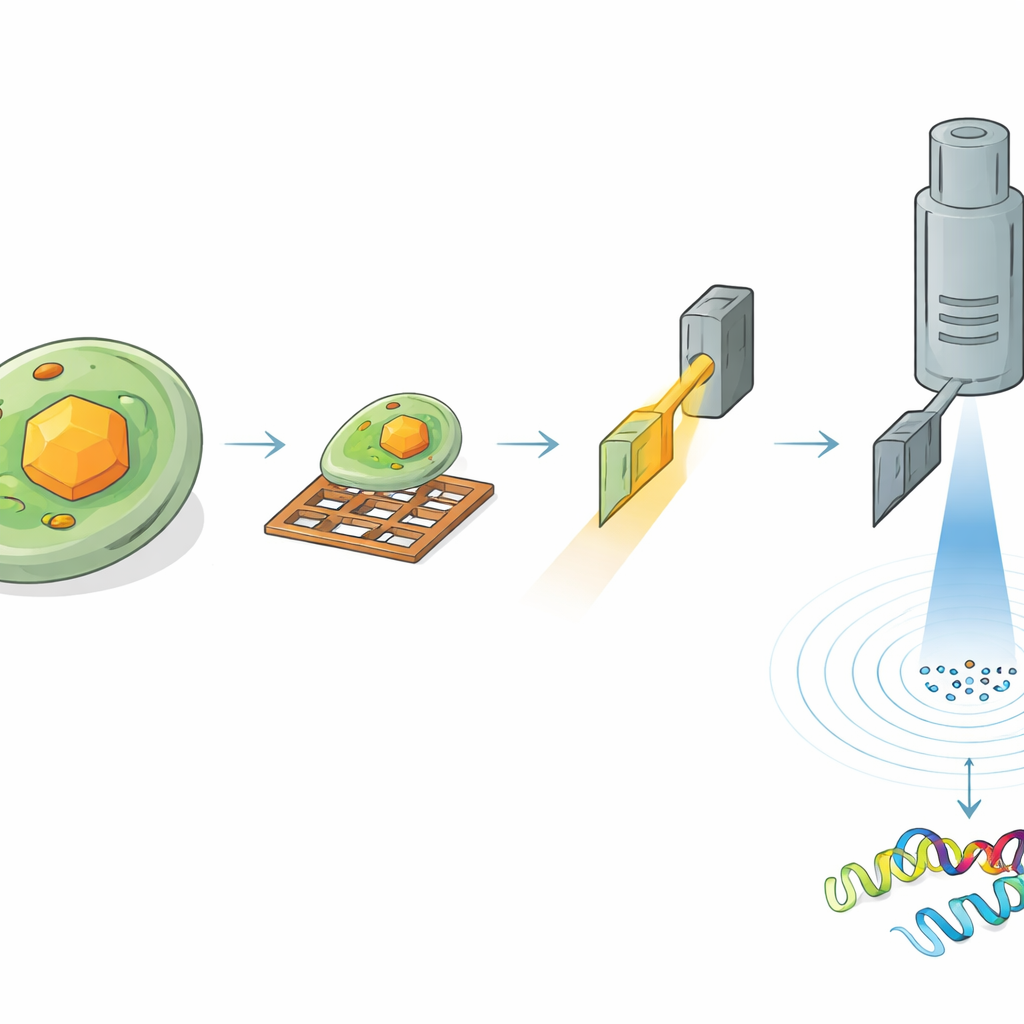
Pour lire la structure de HEX-1 à l’intérieur d’une cellule, les chercheurs ont dû repérer et amincir soigneusement la bonne région de l’échantillon. D’abord, ils ont congelé les cellules contenant des cristaux sur de petites grilles métalliques et recouvert la surface d’une fine couche de platine. À l’aide d’un microscope optique cryogénique, ils ont scanné de grandes zones de la grille pour localiser les cellules contenant des cristaux et mesurer la position tridimensionnelle des cristaux sous la surface. Ensuite, ils ont placé le même échantillon dans un instrument spécialisé combinant un microscope électronique à balayage et un faisceau d’ions focalisé. Guidés par les images optiques précédentes, ils ont retiré la matière environnante par fraisage pour extraire une tranche ultra-mince, ou lamelle, traversant le cristal choisi, de quelques centaines de nanomètres d’épaisseur — idéale pour le passage des électrons.
Les électrons révèlent le détail atomique à partir de volumes microscopiques
Les lamelles préparées ont ensuite été transférées dans un microscope électronique haut de gamme fonctionnant à des températures cryogéniques. Lorsque la tranche cristalline était lentement tournée dans le microscope, un faisceau d’électrons finement contrôlé la traversait, produisant une série de motifs de diffraction — des arrangements de points délicats qui codent la position des atomes. À partir d’un volume cristallin d’environ 1,6 micromètre cube, l’équipe a reconstruit la structure 3D complète de HEX-1 à 1,9 angström de résolution, suffisamment précise pour modéliser la plupart des chaînes latérales de la protéine. Des volumes encore plus petits, d’environ 0,8 micromètre cube, ont fourni une structure quasiment identique à une résolution légèrement inférieure. Fait important, les modèles obtenus correspondaient étroitement à ceux obtenus par une approche X‑ray sérielle conventionnelle nécessitant plus de 60 000 cristaux et un volume cristallin total environ sept millions de fois plus grand.
Comment cela change la donne en biologie structurale
Des comparaisons côte à côte ont montré que la structure déterminée à partir d’un seul cristal par diffraction électronique in cellulo est essentiellement la même que celle moyennée à partir de dizaines de milliers de cristaux avec des rayons X. Les différences étaient mineures et principalement limitées à des boucles flexibles, où des mouvements naturels sont attendus. Les chercheurs ont également démontré que les doses d’électrons utilisées étaient suffisamment faibles pour éviter des dommages radiatifs sérieux, et que chaque cristal traité fournissait des données de haute qualité. Bien que la préparation des lamelles fines requière encore de l’adresse et du temps, les instruments nécessaires — microscopes optiques cryogéniques, systèmes à faisceau d’ions focalisé et microscopes électroniques cryogéniques — sont désormais répandus dans de nombreux centres de recherche.
De nombreuses cellules à un laboratoire structural sur cellule unique
Ce travail montre qu’il est désormais possible de déterminer la structure atomique d’une protéine à partir d’un seul cristal à l’intérieur d’une seule cellule, sans jamais purifier la protéine. IncelluloED pourrait être particulièrement puissant lorsque seules quelques cellules forment des cristaux, ou lorsque les protéines sont difficiles à isoler sans perdre des partenaires importants ou des groupes chimiques. À mesure que le flux de travail devient plus automatisé et s’étend à d’autres protéines, il pourrait permettre aux chercheurs d’explorer comment les structures varient d’une cellule à l’autre, d’étudier les modifications liées aux maladies dans leur cadre natif, et même de soutenir la découverte de médicaments directement dans des cellules vivantes. En pratique, l’étude rapproche considérablement la vision d’un « laboratoire structural à cellule unique » de la réalité.
Citation: Bílá, Š., Pinkas, D., Khakurel, K. et al. Single-cell structural biology with intracellular electron crystallography. Nat Commun 17, 2109 (2026). https://doi.org/10.1038/s41467-026-69205-6
Mots-clés: diffraction électronique, cristallographie in cellulo, biologie structurale unicellulaire, structure des protéines, cryo-EM