Clear Sky Science · fr
14-3-3ζ interagit avec le domaine de liaison à l’ADN de FOXO3a et dissocie compétitivement l’ADN par ancrage à double motif
Comment les cellules cancéreuses désactivent leur propre interrupteur d’autodestruction
Nos cellules disposent de mécanismes de sécurité intégrés qui peuvent déclencher leur mort lorsque les dégâts ou les risques deviennent trop importants. L’un de ces systèmes est contrôlé par une protéine appelée FOXO3a, qui active des gènes poussant les cellules déviantes à s’autodétruire. De nombreuses tumeurs, cependant, trouvent des moyens de faire taire FOXO3a et de poursuivre leur croissance. Cette étude explore les détails moléculaires montrant comment une autre protéine, 14-3-3ζ, aide les cellules cancéreuses à détacher FOXO3a de l’ADN et à neutraliser cet interrupteur d’autodestruction.
La protéine gardienne qui riposte face au cancer
FOXO3a agit comme un inspecteur de sécurité pour la cellule. Elle se lie à des sites spécifiques de l’ADN et active des gènes qui ralentissent la croissance ou déclenchent la mort cellulaire programmée (apoptose) lorsque quelque chose tourne mal. Dans les cellules saines, cela aide à prévenir la formation de tumeurs. Dans de nombreux cancers, toutefois, une voie de signalisation favorisant la croissance, activée par des protéines Ras mutantes, reste en permanence allumée. Cette voie active une kinase appelée AKT, qui marque chimiquement FOXO3a en ajoutant des groupes phosphate sur plusieurs sites. Ces marques créent des sites d’ancrage pour 14-3-3ζ, une protéine adaptatrice dimérique qui reconnaît des motifs phosphorylés sur de nombreuses cibles. Quand 14-3-3ζ se fixe à FOXO3a, les freins internes de la cellule commencent à céder.
Pourquoi la simple force d’affinité n’explique pas l’effet
Des travaux antérieurs sur une protéine apparentée, FOXO4, suggéraient que les protéines 14-3-3 expulsaient les facteurs FOXO de l’ADN simplement parce qu’elles se lient plus fortement. Mais FOXO3a préfère ses cibles naturelles d’ADN plus fortement que ne le supposait l’ancien modèle. Dans cette étude, les chercheurs ont produit une version de FOXO3a comprenant le domaine de liaison à l’ADN et deux sites de phosphorylation clés. Ils ont mesuré l’affinité de cette protéine pour l’ADN ou pour 14-3-3ζ et constaté que les différences d’affinité étaient modestes : 14-3-3ζ n’était qu’environ deux fois plus fort partenaire que l’ADN. Pourtant, dans des expériences en mélange suivant le déplacement des molécules dans une colonne de chromatographie, 14-3-3ζ a pu provoquer une libération presque complète de l’ADN par FOXO3a, comme s’il était environ 100 fois plus compétitif que prévu. Ce décalage suggérait qu’un mécanisme supplémentaire était à l’œuvre.
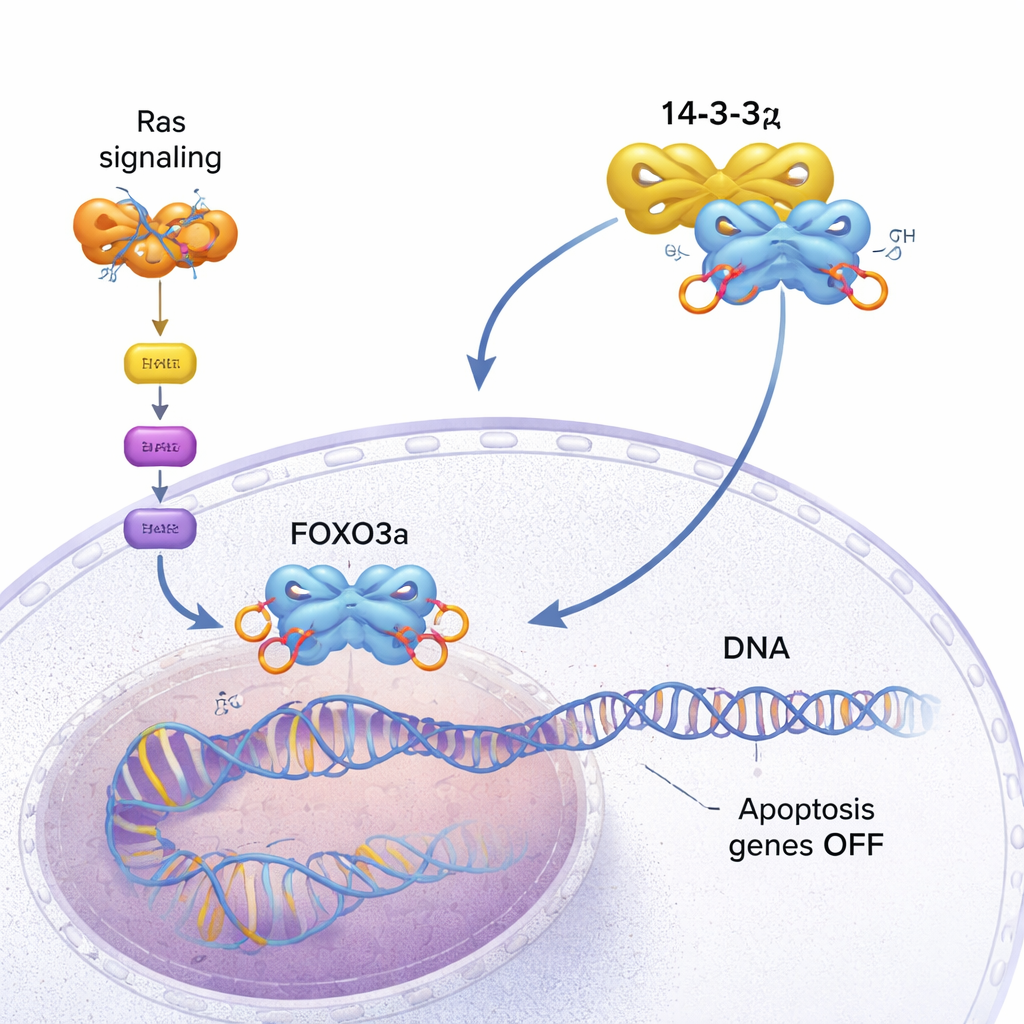
Une prise en trois points qui évince l’ADN
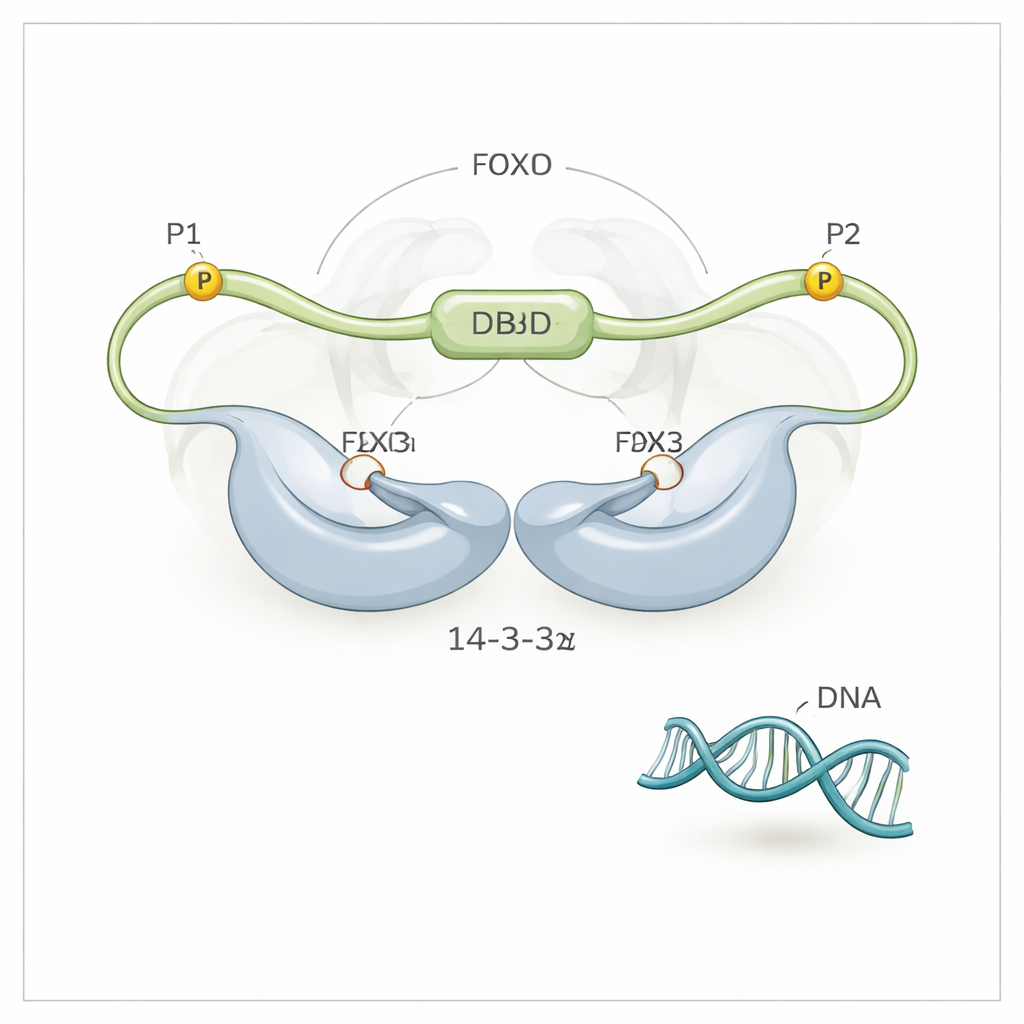
Grâce à la spectroscopie RMN à haute résolution, l’équipe a découvert que 14-3-3ζ fait plus que simplement saisir FOXO3a à ses deux motifs phosphorylés (appelés P1 et P2). Il établit aussi un contact direct, bien que plus faible, avec le domaine de liaison à l’ADN (DBD) de FOXO3a — la surface qui s’accroche normalement à l’ADN. La protéine 14-3-3ζ forme un dimère symétrique avec deux gouttières. Chaque gouttière saisit l’un des motifs phosphorylés de FOXO3a, ancrant ainsi FOXO3a sur 14-3-3ζ en deux points. Comme l’un de ces motifs (P2) est très proche le long de la chaîne du domaine de liaison à l’ADN, ce « rattachement à double motif » positionne efficacement 14-3-3ζ juste à côté du DBD, augmentant considérablement la probabilité que le DBD heurte et se lie à la surface de 14-3-3ζ plutôt qu’à l’ADN. Les chercheurs ont même pu observer que le DBD bascule d’un côté à l’autre du dimère 14-3-3ζ, passant la majeure partie du temps protégé de l’ADN.
Quels tags phosphate comptent le plus
Pour démêler les rôles des deux sites phosphorylés, l’équipe a conçu des variantes de FOXO3a où un seul site pouvait être phosphorylé à la fois. Lorsque seul le site P2 proche du DBD était actif, 14-3-3ζ pouvait partiellement déloger l’ADN mais pas complètement. Lorsque seul le site plus éloigné P1 était actif, 14-3-3ζ pouvait se lier à FOXO3a mais affectait à peine sa tenue sur l’ADN. La libération complète de l’ADN nécessitait les deux sites agissant de concert : P1 fournit un point d’ancrage initial à haute affinité pour 14-3-3ζ, et P2 positionne le dimère suffisamment près du DBD pour rendre la concentration locale de 14-3-3ζ effectivement énorme à cet endroit. Ce rattachement en plusieurs étapes amplifie une préférence d’affinité modestes en une capacité puissante d’expulser l’ADN.
Du bras de fer moléculaire aux nouvelles idées médicamenteuses
Pour un non-spécialiste, l’essentiel est que les cellules cancéreuses exploitent un coup de géométrie moléculaire ingénieux, et pas seulement une force d’affinité brute, pour faire taire une importante protéine suppresseur de tumeur. 14-3-3ζ utilise deux petites étiquettes d’ancrage sur FOXO3a comme points d’ancrage, puis se déploie pour couvrir la surface de liaison à l’ADN du domaine central de FOXO3a, l’empêchant d’activer les gènes de mort cellulaire. Comme les familles FOXO et 14-3-3 sont largement utilisées dans de nombreux tissus, cette stratégie de double rattachement est probablement fréquente dans d’autres cancers également. Perturber soit les ancres dépendantes du phosphate, soit le contact plus faible avec la face du DBD de FOXO3a pourrait restaurer sa capacité à activer les programmes d’autodestruction dans les cellules tumorales, offrant des pistes prometteuses pour la conception de nouveaux anticancéreux.
Citation: Enomoto, S., Kuwayama, T., Nakatsuka, S. et al. 14-3-3ζ interacts with DNA-binding domain of FOXO3a and competitively dissociates DNA by dual-motif tethering. Nat Commun 17, 1503 (2026). https://doi.org/10.1038/s41467-026-69203-8
Mots-clés: FOXO3a, protéines 14-3-3, apoptose, signalisation Ras–AKT, thérapeutiques anticancéreuses