Clear Sky Science · fr
La survie des macrophages résidents dépend de la fonction mitochondriale régulée par SerpinB2 lors d’une inflammation chronique
Pourquoi les cellules immunitaires du tissu adipeux comptent
La plupart des gens considèrent la graisse corporelle comme un simple stockeur passif, alors qu’il s’agit en réalité d’un tissu animé, riche en cellules immunitaires qui régulent l’inflammation et la glycémie. Cette étude révèle comment un groupe spécifique de cellules immunitaires longévives dans la graisse abdominale profonde joue le rôle de gardiens contre le diabète de type 2 — et comment l’inflammation chronique liée à l’obésité les tue progressivement en endommageant leurs petites centrales énergétiques, les mitochondries.
Deux types de gardiens graisseux
Le tissu adipeux viscéral — la graisse entourant les organes internes — contient deux principaux types de macrophages. L’un est de courte durée de vie et constamment renouvelé depuis le sang ; ces macrophages « inflammatoires » favorisent souvent l’inflammation et la résistance à l’insuline. L’autre est un macrophage résident, de longue durée, issu du développement précoce, qui aide normalement à maintenir le tissu calme, à soutenir un stockage adipeux sain et à promouvoir la sensibilité à l’insuline au niveau de l’organisme. En suivant ces cellules chez la souris et en comparant l’activité génique, les chercheurs ont montré que les macrophages résidents sont enrichis en gènes anti‑inflammatoires et sensibilisants à l’insuline, tandis que les macrophages dérivés des monocytes entrants expriment des gènes qui détériorent le contrôle de la glycémie.
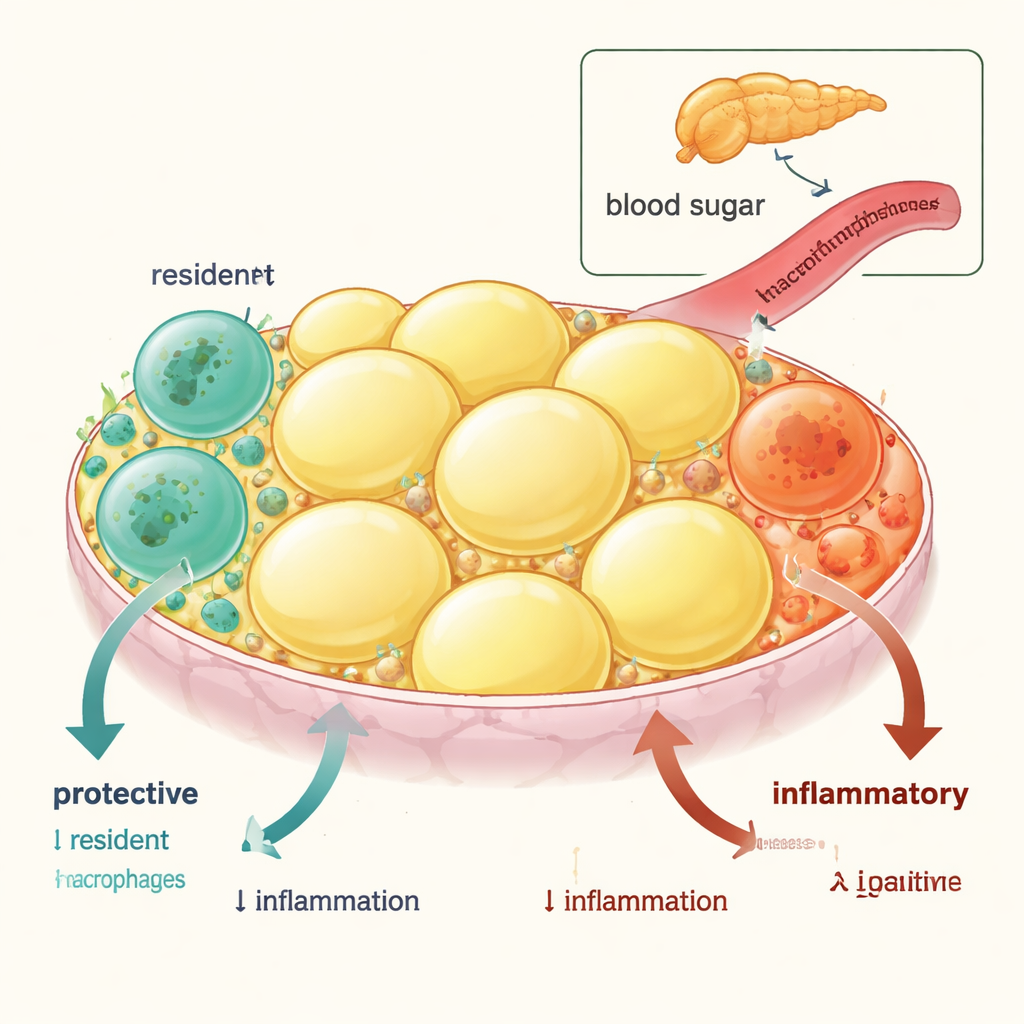
Quand l’inflammation élimine les bons éléments
Dans l’obésité, cet équilibre protecteur bascule. L’équipe a constaté que, chez les souris obèses et chez des personnes obèses ou diabétiques, le nombre de macrophages résidents dans la graisse viscérale diminue, tandis que les macrophages inflammatoires augmentent. Des images détaillées et des marqueurs de mort cellulaire ont expliqué pourquoi : les macrophages résidents subissent davantage de mort cellulaire programmée (apoptose), alors que les cellules inflammatoires n’en subissent pas. De manière remarquable, lorsque des souris obèses ont été retirées d’un régime riche en graisses, la population résidente s’est lentement reconstituée par prolifération locale et la santé métabolique s’est améliorée — montrant que cette perte est provoquée par l’état inflammatoire et peut être renversée.
Une protéine relie les mitochondries à la survie
Un indice clé est une protéine appelée SerpinB2, surtout connue pour son rôle dans la coagulation. Les chercheurs ont découvert que SerpinB2 est produite à des niveaux très élevés à l’intérieur des macrophages résidents, mais beaucoup moins dans les macrophages inflammatoires. Chez les humains et les souris obèses, les macrophages résidents ont fortement réduit l’expression de SerpinB2, et un indice de masse corporelle plus élevé était associé à moins de cellules positives pour SerpinB2. Des expériences sur des cellules dépourvues de SerpinB2 ont montré une augmentation de la fuite du cytochrome c — une protéine cruciale — des mitochondries vers le cytoplasme, un déclencheur classique de l’apoptose. Ces macrophages déficients en SerpinB2 présentaient moins de défenses antioxydantes, davantage d’espèces réactives de l’oxygène (ROS) mitochondriales et une consommation d’oxygène plus élevée, autant de signes de mitochondries stressées et surmenées qui poussent les cellules vers un comportement inflammatoire puis la mort.
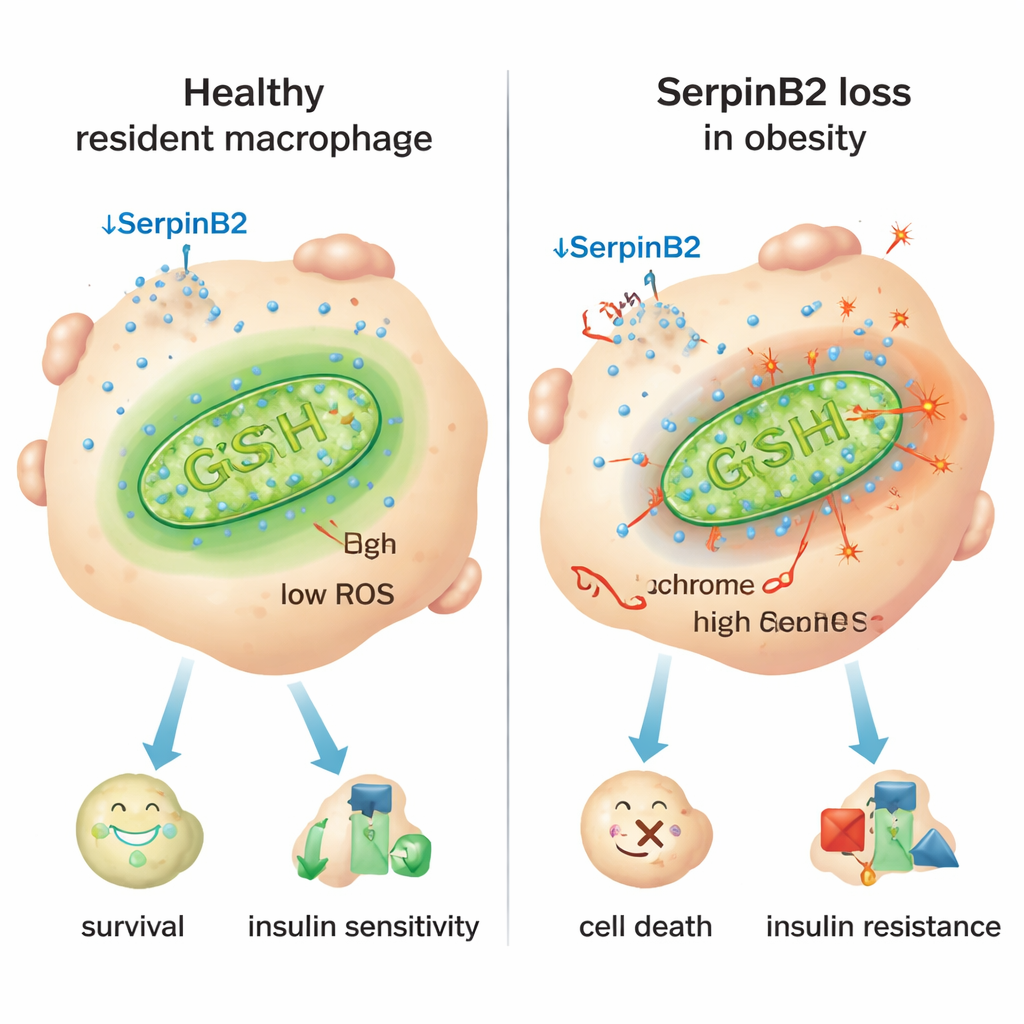
Le commutateur inflammatoire et une piste de réparation
L’étude a relié ce stress mitochondrial aux signaux inflammatoires chroniques de l’obésité, en particulier au messager immunitaire interféron‑γ (IFN‑γ), produit en excès dans le tissu adipeux. L’IFN‑γ active un répresseur transcriptionnel nommé Ikaros qui se lie à la région de contrôle du gène SerpinB2 et en diminue l’expression. Chez des souris génétiquement modifiées pour que leurs cellules myéloïdes ne répondent pas à l’IFN‑γ, les macrophages résidents ont conservé SerpinB2, survécu mieux, et les animaux ont présenté une glycémie plus basse, une meilleure sensibilité à l’insuline et des adipocytes plus petits. Inversement, la suppression spécifique de SerpinB2 dans les macrophages a aggravé l’intolérance au glucose et la résistance à l’insuline, en partie parce que le tissu adipeux devenait plus enflammé et s’étendait. L’augmentation des niveaux de glutathion antioxydant avec le supplément N‑acétylcystéine (NAC) a restauré la protection mitochondriale, sauvé la survie des macrophages résidents, réduit la taille des adipocytes et amélioré les paramètres métaboliques même en l’absence de SerpinB2.
Ce que cela signifie pour la santé métabolique
Pour le lecteur non spécialiste, le message principal est que toutes les graisses ni toutes les cellules immunitaires résidentes ne sont nuisibles. Un groupe spécialisé et longévif de macrophages dans la graisse viscérale nous protège en réalité contre l’inflammation incontrôlée et l’hyperglycémie en maintenant leurs mitochondries en bonne santé via des défenses antioxydantes pilotées par SerpinB2. Dans l’obésité, des signaux inflammatoires chroniques éteignent SerpinB2, les mitochondries sont stressées, ces cellules protectrices meurent et des macrophages plus dommageables prennent le relais, contribuant à la résistance à l’insuline. Les résultats suggèrent que des thérapies visant à préserver les macrophages résidents — en bloquant le frein IFN‑γ/Ikaros sur SerpinB2 ou en soutenant les défenses antioxydantes à base de glutathion — pourraient aider à prévenir ou traiter les maladies métaboliques liées à l’obésité.
Citation: Vasamsetti, S.B., Sadaf, S., Uddin, M.A. et al. Tissue-resident macrophage survival depends on mitochondrial function regulated by SerpinB2 in chronic inflammation. Nat Commun 17, 1493 (2026). https://doi.org/10.1038/s41467-026-69196-4
Mots-clés: graisse viscérale, macrophages, mitochondries, résistance à l’insuline, SerpinB2