Clear Sky Science · fr
Ingénierie métabolique de la biosynthèse de la doxorubicine par optimisation des partenaires rédox des P450 et analyse structurale de DoxA
Pourquoi l’origine d’un médicament anticancer compte
La doxorubicine est l’un des médicaments phares de la chimiothérapie moderne, utilisée pour traiter des cancers allant des leucémies aux tumeurs mammaires. Pourtant, malgré des décennies d’utilisation, sa fabrication reste étonnamment détournée : l’industrie la construit généralement à partir d’un composé apparenté plutôt que de laisser son microbe natif achever la synthèse. Cette étude dévoile pourquoi la bactérie productrice peine à réaliser les dernières étapes chimiques et montre comment la réingénierie de ses machineries internes peut fortement augmenter la production de doxorubicine pleinement formée, ouvrant la voie à des approvisionnements plus fiables et potentiellement moins coûteux.
Des bactéries du sol au médicament salvateur
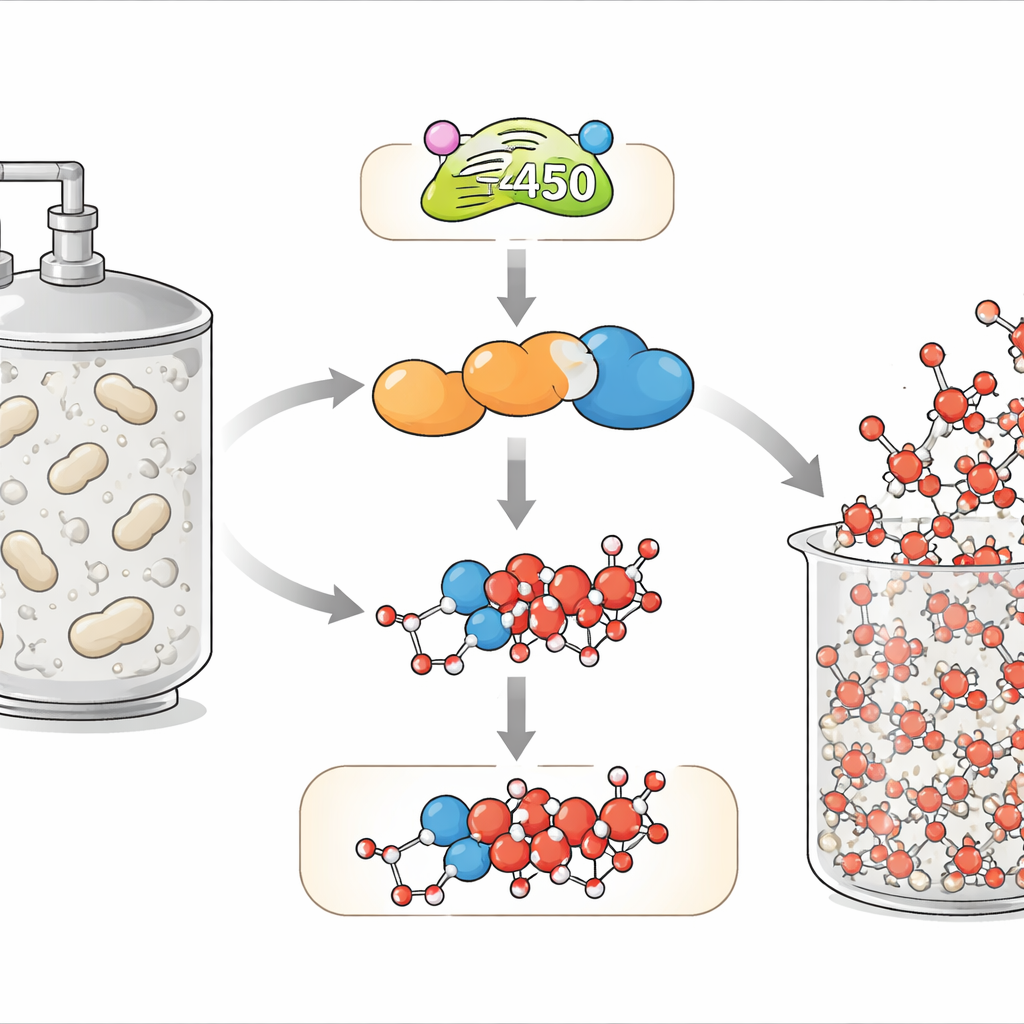
La doxorubicine appartient aux anthracyclines, une famille de molécules naturelles produites par des bactéries du sol du genre Streptomyces. Ces composés partagent un squelette carbone rigide et plan qui s’insère entre les paires de bases de l’ADN, ainsi qu’un sucre qui se loge dans les sillons de l’ADN. Ensemble, ces caractéristiques bloquent les machineries de gestion de l’ADN et déclenchent finalement la mort cellulaire — utile contre les cellules cancéreuses à croissance rapide. Le producteur classique, Streptomyces peucetius, fabrique naturellement principalement un médicament précurseur appelé daunorubicine, et seulement une quantité modeste de la doxorubicine plus efficace, qui diffère par un seul groupe porteur d’oxygène supplémentaire. Ce minime changement structurel améliore considérablement l’activité mais se révèle étonnamment difficile à réaliser efficacement pour le microbe.
Trouver le bon câblage électrique à l’intérieur de la cellule
L’enzyme cruciale qui effectue les trois dernières étapes d’oxydation sur le squelette du médicament s’appelle DoxA, un membre de la famille des cytochromes P450. À la manière d’une petite usine chimique, DoxA nécessite un flux continu d’électrons pour activer l’oxygène et introduire de nouveaux atomes d’oxygène sur la molécule. Dans la bactérie, ces électrons sont fournis via un relais de protéines auxiliaires connues sous le nom de partenaires rédox. Le génome de S. peucetius contient plusieurs candidats, rendant incertains les appariements réels avec DoxA. En comparant l’activité génique et le métabolisme d’une souche normale, d’un mutant riche en daunorubicine et d’un mutant riche en doxorubicine, les chercheurs ont identifié un ferredoxine (Fdx4) et une ferredoxine-réductase (FdR3) comme partenaires naturels. Reconstituer ce trio en réactions in vitro a confirmé que DoxA fonctionne au mieux lorsqu’il est connecté à cette chaîne spécifique de transfert d’électrons, comme en adaptant le bon adaptateur secteur à un appareil.
Alléger le ralentissement auto‑infligé de l’enzyme
Même avec le câblage électrique correct, DoxA a tendance à buter à l’étape finale qui convertit la daunorubicine en doxorubicine. Des travaux antérieurs laissaient entendre que le produit lui‑même peut enrailler l’enzyme. L’équipe s’est intéressée à un gène voisin, dnrV, dont la fonction était restée mystérieuse. Des tests biochimiques ont montré que la protéine DnrV se lie fortement à une gamme de molécules anthracyclines, y compris la doxorubicine, sans les modifier chimiquement. Ajouter DnrV aux réactions de DoxA a grandement amélioré le flux de la chimie, permettant la conversion complète des précurseurs au médicament final tout en évitant des réactions secondaires destructrices. En termes pratiques, DnrV agit comme une éponge interne qui absorbe la doxorubicine fraîchement formée, l’empêchant d’encrasser l’enzyme ou d’endommager l’ADN à l’intérieur de la cellule productrice.
Comprendre pourquoi la dernière étape est si lente
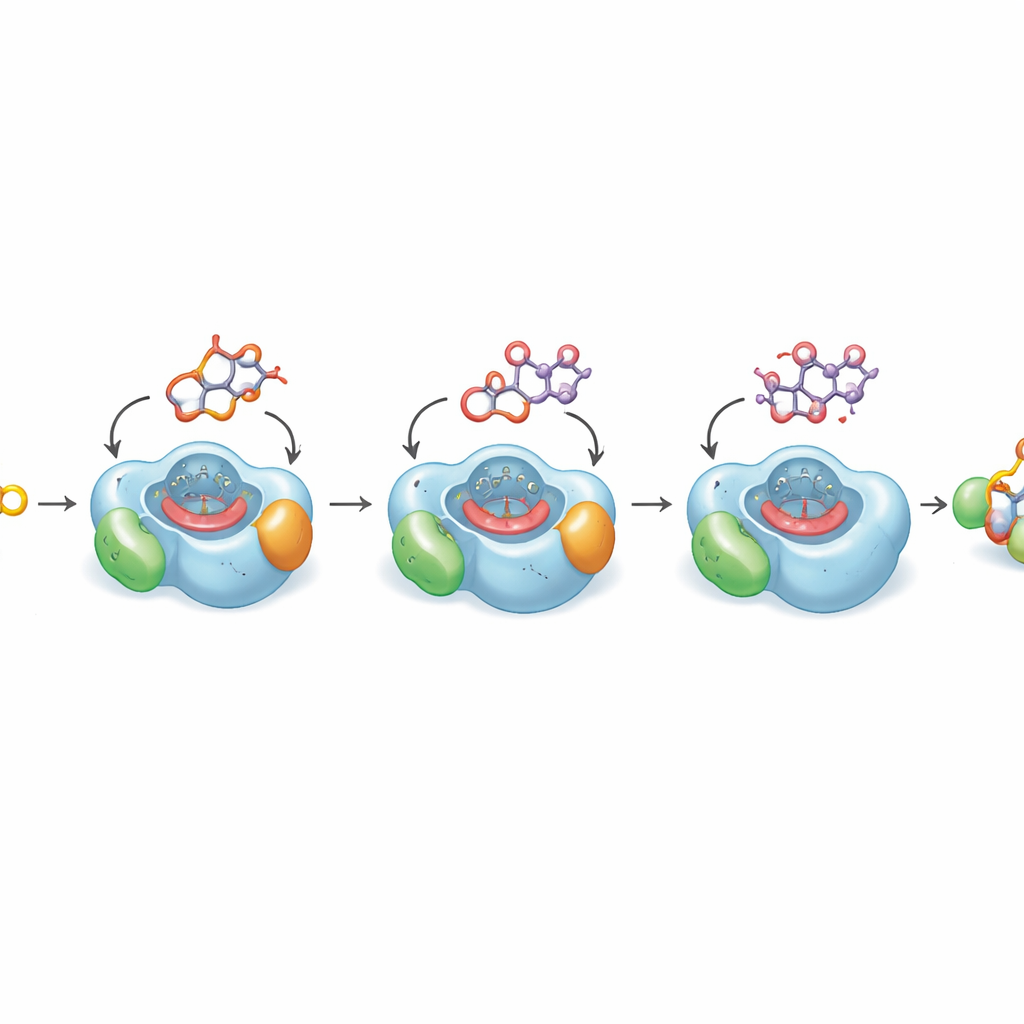
Pour expliquer pourquoi la dernière oxydation clé est intrinsèquement lente, les auteurs ont résolu des structures cristallines à haute résolution de DoxA liée à trois intermédiaires successifs. Ces structures montrent comment le noyau plan du médicament et son sucre attaché se logent dans une poche étroite au‑dessus du groupe hème de l’enzyme, le centre métallique réactif qui réalise l’oxydation. Pour les étapes antérieures, l’atome de carbone à modifier se trouve proche de l’hème dans une position idéale pour la réaction. Mais dans le substrat final, la daunorubicine, la portion de la molécule à hydroxyler se replie loin de l’hème dans une petite cavité huileuse, une disposition que des calculs quantiques montrent énergétiquement favorisée. Des simulations informatiques sur des microsecondes confirment que la molécule ne prend qu’occasionnellement la pose productive nécessaire pour cette dernière insertion d’oxygène. Ce biais structural explique pourquoi la conversion en doxorubicine est naturellement inefficace.
Concevoir une souche meilleure productrice de doxorubicine
Fortes de ces connaissances, les équipes ont repensé la bactérie de façon rationnelle plutôt que par mutagenèse aléatoire. Ils ont introduit un gène de réparation de l’ADN pour stabiliser la production, puis inséré des copies supplémentaires de doxA, des partenaires rédox optimaux fdx4 et fdr3, et du protéine liant utile dnrV sous des promoteurs choisis avec soin pour équilibrer leurs niveaux. Ils ont aussi ajusté les conditions de culture et utilisé des résines spéciales pour absorber les intermédiaires toxiques et adhésifs. En flacons de laboratoire et dans un bioréacteur de 20 litres, la meilleure souche ingénierée a produit 336 milligrammes de doxorubicine par litre de culture avec un ratio 81:19 de doxorubicine à daunorubicine — une augmentation d’environ 180 % par rapport à la souche de départ et un mélange de produits bien plus propre.
Ce que cela signifie pour l’approvisionnement futur en médicaments anticancer
En disséquant à la fois le système d’alimentation en électrons et la structure 3D d’une enzyme clé, ce travail explique pourquoi un microbe d’intérêt médical sous‑performait dans la fabrication de notre anthracycline la plus prisée. Apparier DoxA avec ses partenaires rédox naturels, ajouter une protéine aideuse liant le médicament et rééquilibrer l’expression génique a transformé un producteur réticent en un producteur robuste. Bien qu’un ajustement plus poussé des enzymes puisse accélérer encore l’étape chimique finale, l’étude rapproche déjà la production entièrement biologique de doxorubicine d’une réalité industrielle. Pour les patients et les systèmes de santé, de telles avancées pourraient se traduire par un accès plus sûr, évolutif et rentable à un médicament de chimiothérapie de référence.
Citation: Koroleva, A., Artukka, E., Yamada, K. et al. Metabolic engineering of doxorubicin biosynthesis through P450-redox partner optimization and structural analysis of DoxA. Nat Commun 17, 2358 (2026). https://doi.org/10.1038/s41467-026-69194-6
Mots-clés: production de doxorubicine, biosynthèse des anthracyclines, ingénierie enzymatique, fabrication microbienne de médicaments, cytochrome P450