Clear Sky Science · fr
L’activation d’une protéine kinase C atypique entraîne l’excrétion intestinale de glucose dans le diabète sucré
Transformer l’intestin en une valve à sucre
Les personnes atteintes de diabète vivent avec une trop grande quantité de sucre circulant dans le sang. Les chirurgies bariatriques telles que le bypass gastrique peuvent normaliser la glycémie de manière surprenante et rapide, parfois avant même une perte de poids significative, mais le mécanisme derrière cet effet a longtemps été mystérieux. Cette étude révèle une « valve à sucre » d’origine intestinale — un mécanisme par lequel l’intestin prélève du sucre dans le sang et en renvoie une partie dans la lumière intestinale — suggérant une nouvelle cible médicamenteuse qui pourrait reproduire les bénéfices de la chirurgie sans opération.
Pourquoi la chirurgie modifie si vite la glycémie
Les cliniciens savent depuis longtemps que le bypass gastrique en Y de Roux, une chirurgie fréquente pour la perte de poids, figure aussi parmi les traitements les plus puissants du diabète de type 2. Peu après l’intervention, la glycémie des patients s’améliore souvent de façon spectaculaire, avant même une perte de poids marquée. Des travaux antérieurs de ce groupe avaient montré qu’après le bypass, certaines régions de l’intestin grêle se comportent comme une éponge, absorbant le glucose du sang et en libérant une partie dans la lumière intestinale. Ce comportement inhabituel, appelé excrétion intestinale de glucose, semblait dépendre d’un transporteur nommé GLUT1. La grande question était : quel interrupteur moléculaire pousse l’intestin à basculer vers ce mode d’élimination du sucre ?
Utiliser le Big Data pour trouver un interrupteur moléculaire
Pour identifier cet interrupteur, les chercheurs ont utilisé un système informatique de découverte de médicaments à grande échelle fondé sur la Connectivity Map, une base de données montrant comment des milliers de composés modifient l’activité génique dans des cellules. Ils ont comparé les profils d’expression génique issus de cinq situations où l’excrétion intestinale de glucose est élevée — y compris des tissus de rats opérés et des cellules traitées par un signal de croissance intestinale — aux profils produits par des médicaments connus. Une classe de composés a constamment émergé : les activateurs de la protéine kinase C (PKC), une famille d’enzymes qui transmettent des signaux à l’intérieur des cellules. En creusant davantage, l’équipe a ciblé le sous-groupe « atypique » des PKC, en particulier PKCζ, dont l’activité dans les cellules intestinales correspondait le mieux à l’état de type bypass, responsable de l’excrétion de glucose.
La pompe à sucre des cellules intestinales en action
En se focalisant sur des cellules intestinales individuelles par séquençage ARN unicellulaire, les auteurs ont trouvé que la chirurgie de bypass augmente à la fois PKCζ et GLUT1 dans des cellules absorbantes spécifiques qui tapissent la partie distale de l’intestin grêle. En cultures cellulaires et dans des organoïdes intestinaux humains, l’augmentation artificielle de PKCζ ou le traitement par la prostratine — un composé d’origine végétale qui active sans danger ces PKC atypiques — a entraîné la relocalisation de GLUT1 à la surface des cellules. Là, GLUT1 a fonctionné comme une pompe bidirectionnelle : il prélève davantage de glucose du côté faisant face au sang et permet à l’excès de glucose de sortir vers la lumière intestinale. De manière importante, cette dérivation du glucose n’a pas significativement accéléré la glycolyse intracellulaire, indiquant que l’effet principal est l’élimination du glucose plutôt qu’une production d’énergie accrue.
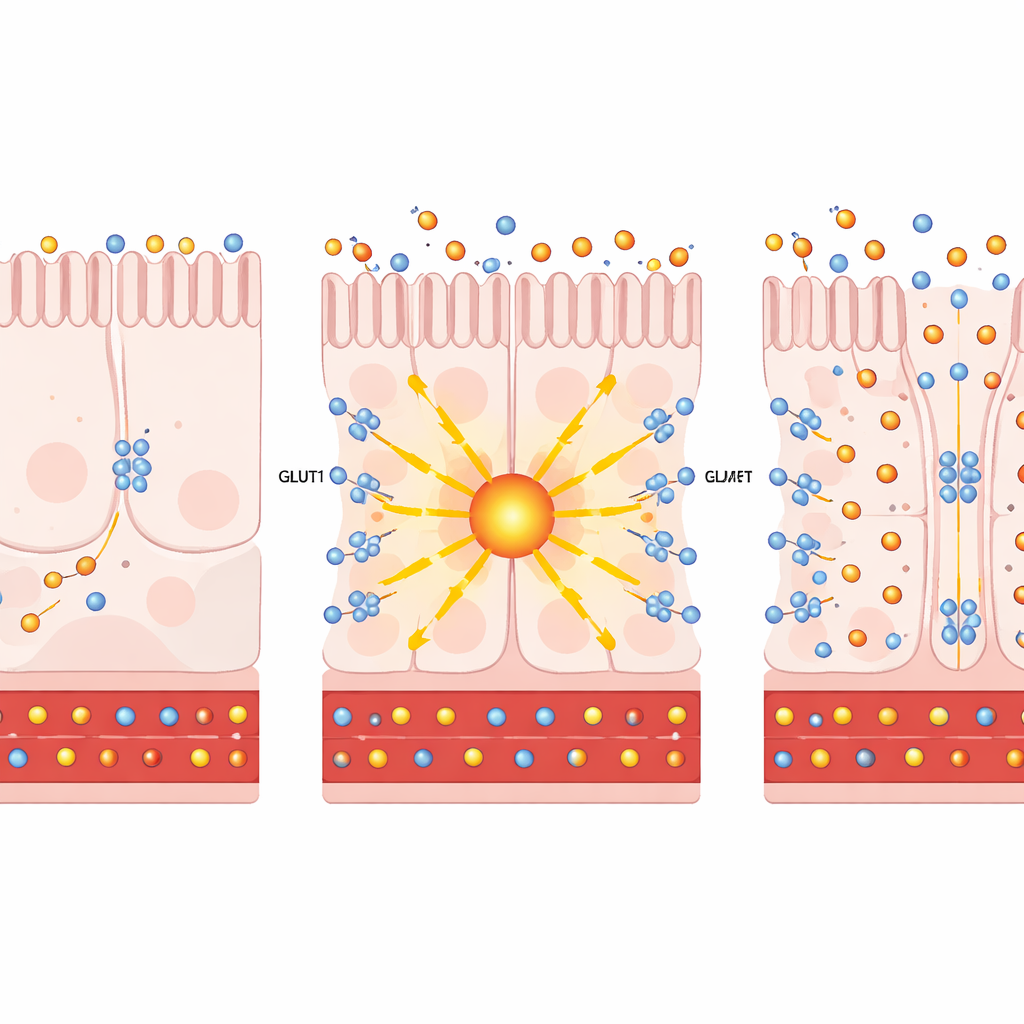
Des cellules aux souris : imiter la chirurgie sans scalpel
L’équipe a ensuite testé si l’activation de cette voie chez des animaux vivants pouvait améliorer le diabète. Chez des souris obèses et résistantes à l’insuline, l’expression accrue de PKCζ spécifiquement dans l’intestin a entraîné un gain de poids plus lent, une glycémie à jeun plus basse et une meilleure tolérance au glucose. Des traceurs de sucres radioactifs ont montré une plus grande captation de glucose par l’intestin distal et son élimination dans la lumière intestinale. Un tableau similaire est apparu dans des modèles murins diabétiques traités par la prostratine : ils ont pris moins de poids, ont mieux toléré des charges de glucose et ont détourné davantage de glucose vers le tractus intestinal, sans modification des taux d’insuline, de l’apport alimentaire ou de l’intégrité de la barrière intestinale. Dans des tranches de tissu, GLUT1 apparaissait aux faces à la fois vasculaire et luminale des cellules, idéalement positionné pour prélever le sucre de la circulation et le pousser vers l’intestin.
Ce que cela pourrait signifier pour la prise en charge future du diabète
Pour un non-spécialiste, le message clé est que l’intestin peut être transformé en une voie d’échappement contrôlée pour l’excès de sucre sanguin. En activant une enzyme spécifique à l’intérieur des cellules intestinales — la PKC atypique — les chercheurs ont pu inciter les cellules à déplacer davantage de transporteurs GLUT1 à leur surface et à agir comme un drain réversible, aspirant le sucre du sang et en déversant une partie dans l’intestin. Chez la souris, cette élimination intestinale du glucose a amélioré la glycémie et limité la prise de poids sans stimuler excessivement l’insuline, modifier l’appétit ou endommager l’intestin. Bien que la prostratine et des composés apparentés ne soient pas encore des médicaments approuvés pour le diabète, ces travaux désignent la voie aPKC–GLUT1 comme une cible prometteuse pour de futurs traitements susceptibles de reproduire en partie les bénéfices métaboliques du bypass gastrique sans opération.
Citation: Kang, C.W., Hong, ZY., Oh, J.H. et al. Atypical protein kinase C activation drives intestinal glucose excretion in diabetes mellitus. Nat Commun 17, 2417 (2026). https://doi.org/10.1038/s41467-026-69193-7
Mots-clés: excrétion intestinale de glucose, diabète de type 2, transporteur GLUT1, protéine kinase C atypique, prostratine