Clear Sky Science · fr
Le signal autocrine TGFβ1 déclenché par MerTK régule la réponse microgliale à la neurodégénérescence
Comment l’équipe de nettoyage du cerveau façonne la maladie
Lorsque les cellules nerveuses du cerveau et du nerf optique meurent, elles laissent derrière elles un lot de débris. Des cellules immunitaires spécialisées, les microglies, jouent le rôle d’équipe de nettoyage du cerveau en engloutissant ces déchets. Mais les microglies font plus que ranger : leur réaction peut soit protéger les circuits neuronaux, soit aggraver des maladies comme la maladie d’Alzheimer. Cette étude met au jour une boucle de communication interne cachée dans les microglies qui est activée par les débris provenant de fibres nerveuses mourantes et qui contribue à déterminer l’intensité de la réponse de ces cellules au dommage.
Un déclencheur dissimulé dans les fibres nerveuses mourantes
Pour étudier ce processus, les chercheurs ont utilisé un modèle murin où le nerf optique est écrasé, provoquant la dégénérescence des longs prolongements des neurones de l’œil sans tuer leurs corps cellulaires. Cela isole proprement les conséquences de la rupture des axones. À la surface de ces fibres en dégénérescence, une molécule lipidique bascule vers l’extérieur et joue le rôle d’un signal « mange-moi » adressé aux microglies voisines. Ces signaux sont détectés par un récepteur microglial appelé MerTK, appartenant à une petite famille de protéines reconnaissant les débris. En supprimant sélectivement MerTK dans les microglies, l’équipe a montré que sans ce récepteur, les microglies ne déployaient pas leur réponse habituelle à la blessure : elles se divisaient moins, se déplaçaient moins et activaient moins de gènes liés au contrôle des dommages et à l’inflammation.
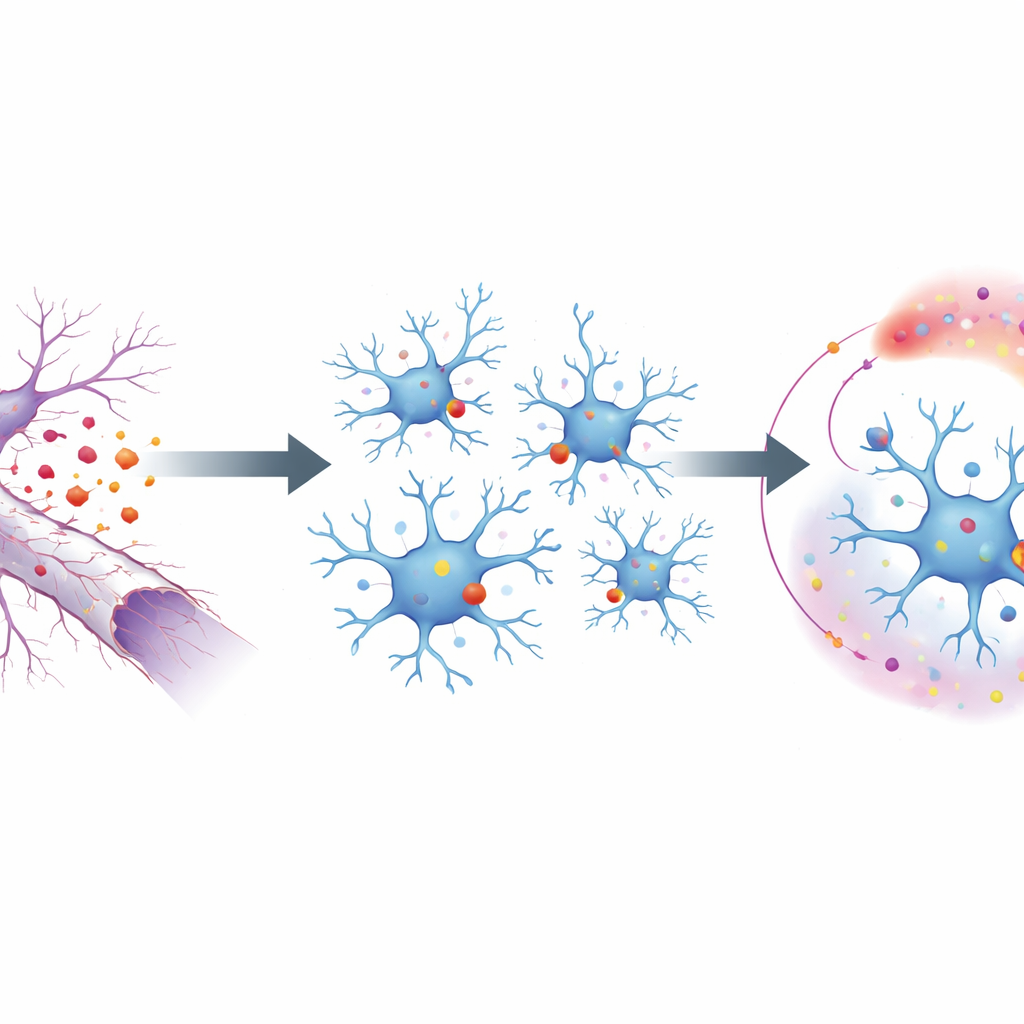
Du signal de surface au reprogrammation génétique
En observant l’intérieur des microglies, les scientifiques ont retracé comment le signal de surface de MerTK se convertit en changements d’activité génique. Ils ont trouvé que MerTK active une cascade moléculaire impliquant la phospholipase C, qui à son tour stimule deux protéines maîtresses au noyau, PU.1 et IRF8. Ces facteurs jouent le rôle de contremaîtres sur la chaîne de montage microgliale, déclenchant l’activation de nombreux gènes nécessaires à un état activé. Grâce à des cartes d’interaction ADN-protéine, l’équipe a découvert que PU.1 et IRF8 se lient directement à un site spécifique du gène codant pour TGFβ1, une puissante protéine de signalisation. Lorsque ce site de liaison a été muté pour empêcher l’ancrage de ces contremaîtres, les microglies dans les nerfs lésés n’ont plus pu augmenter leur production de TGFβ1, alors que d’autres fonctions de base restaient intactes.
Une boucle d’autorétroaction au sein des microglies
La question suivante était de savoir ce que fait réellement le TGFβ1 dans ce contexte. L’étude montre que les microglies produisent du TGFβ1 puis y répondent elles-mêmes, formant une boucle autocrine, c’est‑à‑dire d’autorétroaction. Lorsque le TGFβ1 ou ses récepteurs ont été supprimés génétiquement uniquement dans les microglies, la lésion provoquait toujours la dégénérescence des axones, mais les microglies n’affichaient plus leur programme d’activation complet. Elles proliféraient moins et exprimaient moins de gènes de réponse aux dommages et d’inflammation, même si de nombreux marqueurs d’identité homéostatique restaient supprimés par d’autres signaux. Une molécule clé en aval de la signalisation TGFβ, la SMAD2 phosphorylée, est apparue spécifiquement dans les noyaux microgliaux après la lésion et a largement disparu lorsque le TGFβ1 ou ses récepteurs étaient supprimés, confirmant la rupture de la boucle d’autorétroaction.
Du nerf optique de la souris aux cerveaux atteints d’Alzheimer
Pour tester si cette voie a une importance au‑delà d’un modèle de lésion artificielle, les auteurs ont examiné un modèle murin largement utilisé de la maladie d’Alzheimer. Chez ces animaux, les microglies regroupées autour des plaques amyloïdes présentaient des niveaux élevés de PU.1, IRF8, TGFβ1 et une signalisation TGFβ activée, faisant écho aux observations du nerf optique. L’équipe s’est ensuite tournée vers des données humaines issues de séquençage ARN de noyaux individuels de tissus cérébraux de patients atteints d’Alzheimer. Là, les microglies ressortaient comme les principales cellules exprimant les homologues humains de MerTK, PU.1, IRF8 et TGFB1. Dans des coupes postmortem de cerveaux de patients, les microglies montraient également des signes forts d’une signalisation TGFβ active, contrairement aux tissus de donneurs témoins. Ensemble, ces observations soutiennent l’idée que la même boucle d’autorétroaction opère dans la maladie humaine.
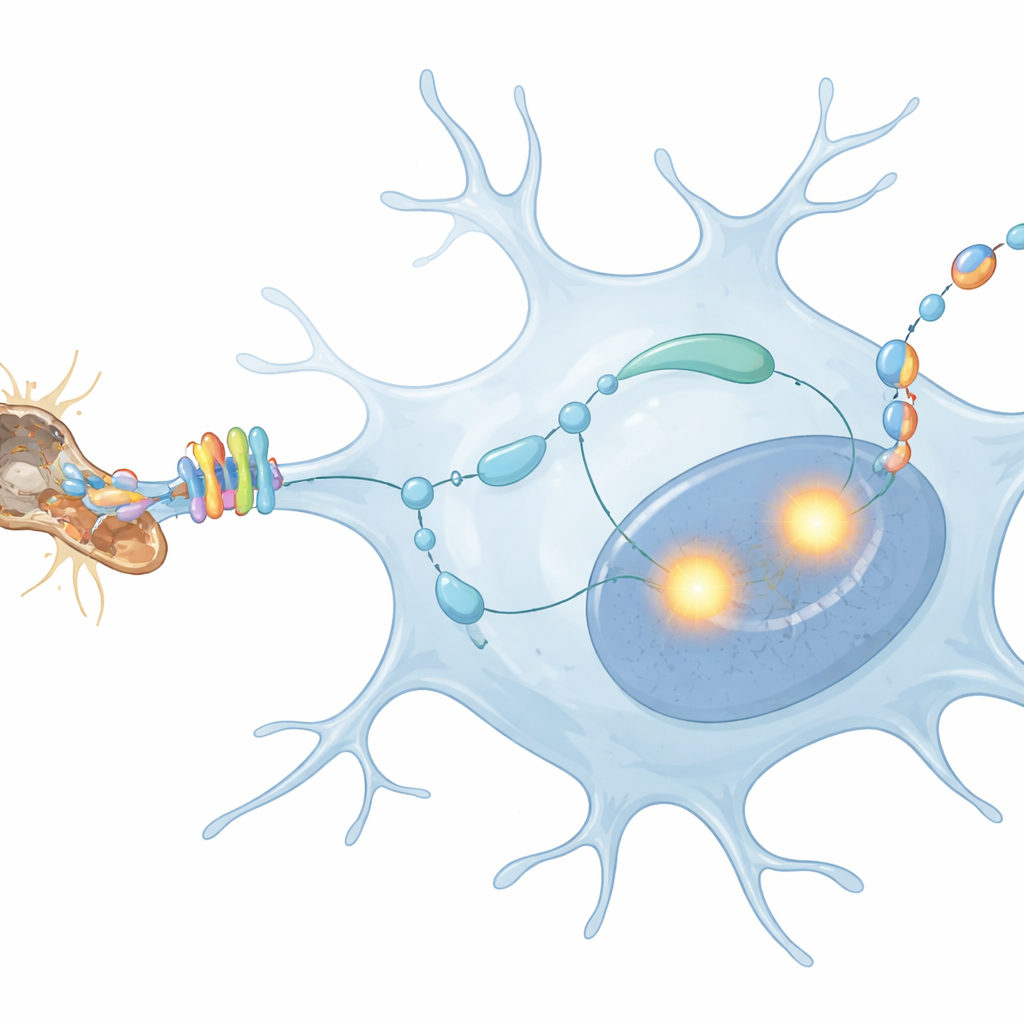
Pourquoi ce dialogue interne compte pour la santé cérébrale
Ce travail révèle une chaîne d’événements où les débris de fibres nerveuses en dégénérescence activent MerTK sur les microglies, qui stimule ensuite PU.1 et IRF8, lesquels à leur tour poussent les microglies à produire du TGFβ1 qui leur renvoie le signal. Ce dialogue interne affine et soutient leur réponse à la neurodégénérescence. Pour un non spécialiste, le message central est que les cellules nettoyeuses du cerveau ne sont pas de simples agents passifs : elles écoutent activement leurs propres signaux, et cette boucle d’autorégulation peut influencer si leurs actions protègent les neurones ou favorisent la progression de maladies comme Alzheimer. Comprendre et éventuellement moduler ce circuit pourrait ouvrir de nouvelles voies pour tempérer l’inflammation nocive tout en préservant le nettoyage bénéfique assuré par les microglies.
Citation: Huang, Y., Deng, Z., Zhou, Z. et al. MerTK-triggered TGFβ1 autocrine signal regulates microglial response to neurodegeneration. Nat Commun 17, 2312 (2026). https://doi.org/10.1038/s41467-026-69189-3
Mots-clés: microglie, neurodégénérescence, maladie d’Alzheimer, inflammation cérébrale, signalisation TGF-bêta