Clear Sky Science · fr
Le mécanisme de pompage Na+ entraîné par le redox dans la NADH-quinone oxydoréductase de Vibrio cholerae repose sur des changements conformationnels dynamiques
Comment la centrale de Choléra est devenue une cible médicamenteuse
La bactérie responsable du choléra, Vibrio cholerae, survit et se multiplie en faisant fonctionner une minuscule centrale moléculaire dans sa membrane cellulaire. Cette étude révèle, avec un niveau de détail inédit, comment l’un de ses moteurs clés — une enzyme appelée Na⁺-NQR — change de conformation en travaillant pour pomper des ions sodium hors de la cellule. Comprendre cette machinerie moléculaire satisfait non seulement la curiosité fondamentale sur la manière dont la vie convertit les nutriments en énergie utilisable, mais indique aussi de nouvelles stratégies pour concevoir des antibiotiques qui arrêtent les bactéries nocives sans affecter les cellules humaines.
Un moteur alimenté au sodium chez les bactéries
De nombreuses bactéries marines et pathogènes dépendent de Na⁺-NQR comme première étape de leur chaîne respiratoire, la série de réactions qui extrait l’énergie des nutriments. Na⁺-NQR est ancrée dans la membrane interne et prélève des électrons d’une molécule combustible appelée NADH, les transmettant le long d’une chaîne de petites molécules « aides » colorées (appelées cofacteurs) jusqu’à la quinone, autre petite molécule intégrée dans la membrane. Au fur et à mesure du flux d’électrons, l’enzyme utilise cette énergie pour expulser des ions sodium (Na⁺) de l’intérieur vers l’extérieur de la cellule, créant un gradient de sodium. Ce gradient fonctionne comme une batterie chargée : il alimente le moteur flagellaire bactérien pour la nage, aide à produire l’ATP (la monnaie énergétique de la cellule) et propulse l’absorption des nutriments ainsi que l’expulsion des médicaments. Parce que Na⁺-NQR n’existe que chez les bactéries et diffère fortement de l’enzyme apparentée dans nos mitochondries, elle constitue une cible attractive pour des antibiotiques très sélectifs.
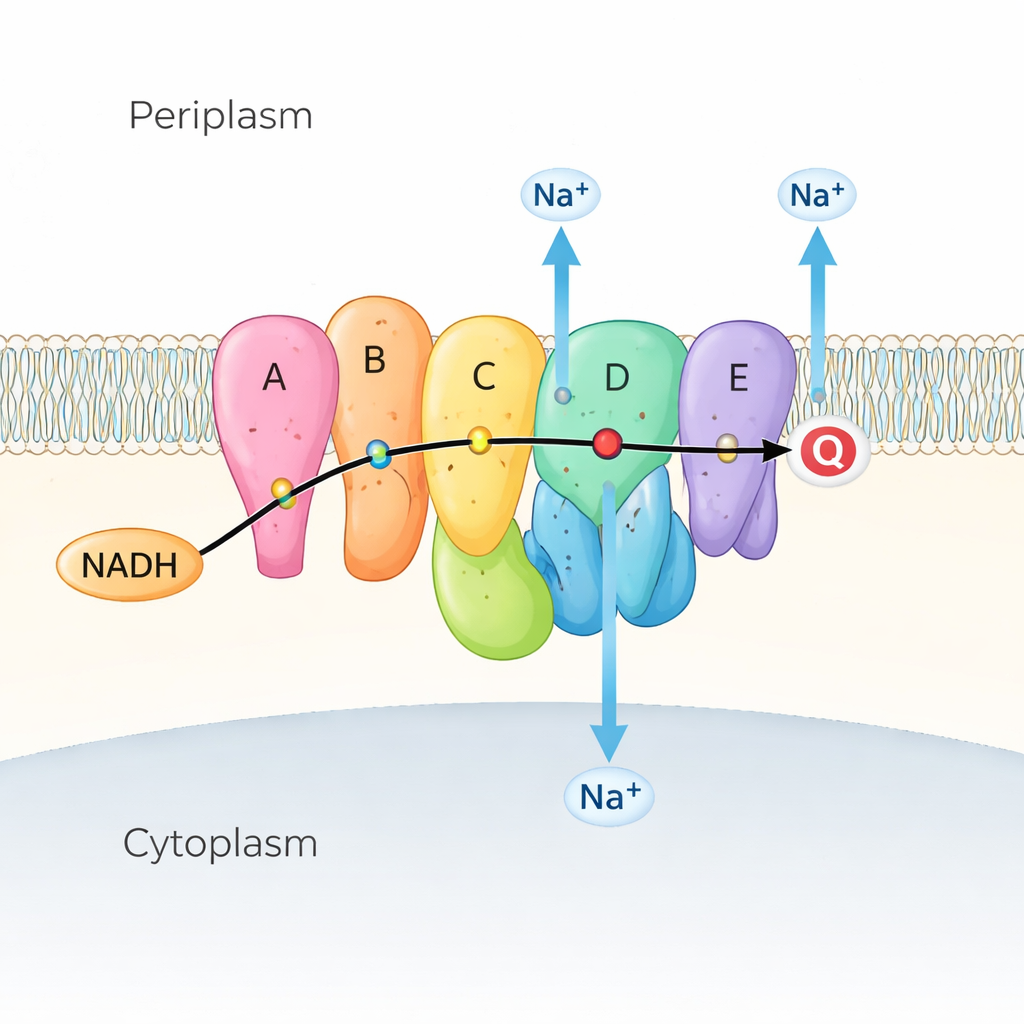
Observer la machine en mouvement
Des clichés antérieurs en rayons X et en cryo-microscopie électronique montraient où se situent les sous-unités et les cofacteurs de Na⁺-NQR, mais révélaient aussi une énigme : certains sauts électroniques critiques étaient trop éloignés pour que les électrons se déplacent efficacement, sauf si la protéine changeait de forme. Les auteurs ont abordé ce point en capturant Na⁺-NQR dans de nombreuses conditions légèrement différentes. Ils ont utilisé des mutants supprimant des cofacteurs spécifiques, des médicaments arrêtant la réaction à des étapes particulières, et des solutions avec ou sans sodium. Grâce à la cryo-EM à haute résolution et à une analyse d’images avancée, ils ont pu séparer et reconstruire plusieurs conformations de la même enzyme, transformant en pratique des clichés statiques en un film de son cycle de fonctionnement.
Un bras flexible et une pince navetteuse
Une découverte clé concerne une sous-unité cytoplasmique flexible, NqrF, qui porte deux cofacteurs transportant des électrons. L’équipe a identifié trois positions pour son domaine « de type ferredoxine » — surnommées les positions « haute », « moyenne » et « basse ». Dans l’état rare mais crucial « bas », ce petit domaine se balance dans une poche formée par deux sous-unités membranaires, NqrD et NqrE, rapprochant son cluster fer–soufre suffisamment pour transmettre un électron. Parallèlement, une sous-unité périplasmique (externe) appelée NqrC se comporte comme une pince mobile. Dans une conformation (« stable »), elle se cale contre une autre sous-unité membranaire, NqrB, positionnée pour transférer les électrons vers l’accepteur final quinone. Dans une seconde conformation (« déplacée »), NqrC se rapproche de NqrD/E, amenant son cofacteur flavine plus près pour accepter un électron de leur centre fer–soufre. Ces mouvements montrent que NqrF et NqrC agissent comme des coursiers dynamiques, comblant de larges écarts dans la chaîne de cofacteurs.
Comment les changements de forme pompent le sodium
Le cœur de la pompe à sodium réside dans les sous-unités appariées NqrD et NqrE, qui forment un faisceau central d’hélices transmembranaires. En combinant structures et simulations de dynamique moléculaire à l’échelle atomique, les auteurs montrent que lorsque le cluster fer–soufre de NqrD/E est réduit (gagne un électron), il crée un site chargé négativement qui attire un ion Na⁺ et quelques molécules d’eau depuis le côté cytoplasmique, formant une poche de liaison transitoire. Des acides aminés hydrophobes au-dessus et en dessous de cette poche jouent le rôle de portes interne et externe, contrôlant l’accès à l’ion. Quand NqrD/E passent d’une conformation « ouverte vers l’intérieur » à une conformation « ouverte vers l’extérieur », le Na⁺ se déplace vers le côté périplasmique et est finalement libéré lorsque le cluster fer–soufre est réoxydé. Les simulations montrent que le Na⁺ reste partiellement hydraté mais ne voit jamais de tunnel continu rempli d’eau, ce qui suggère que l’enzyme est étanche et évite les fuites protoniques indésirables.
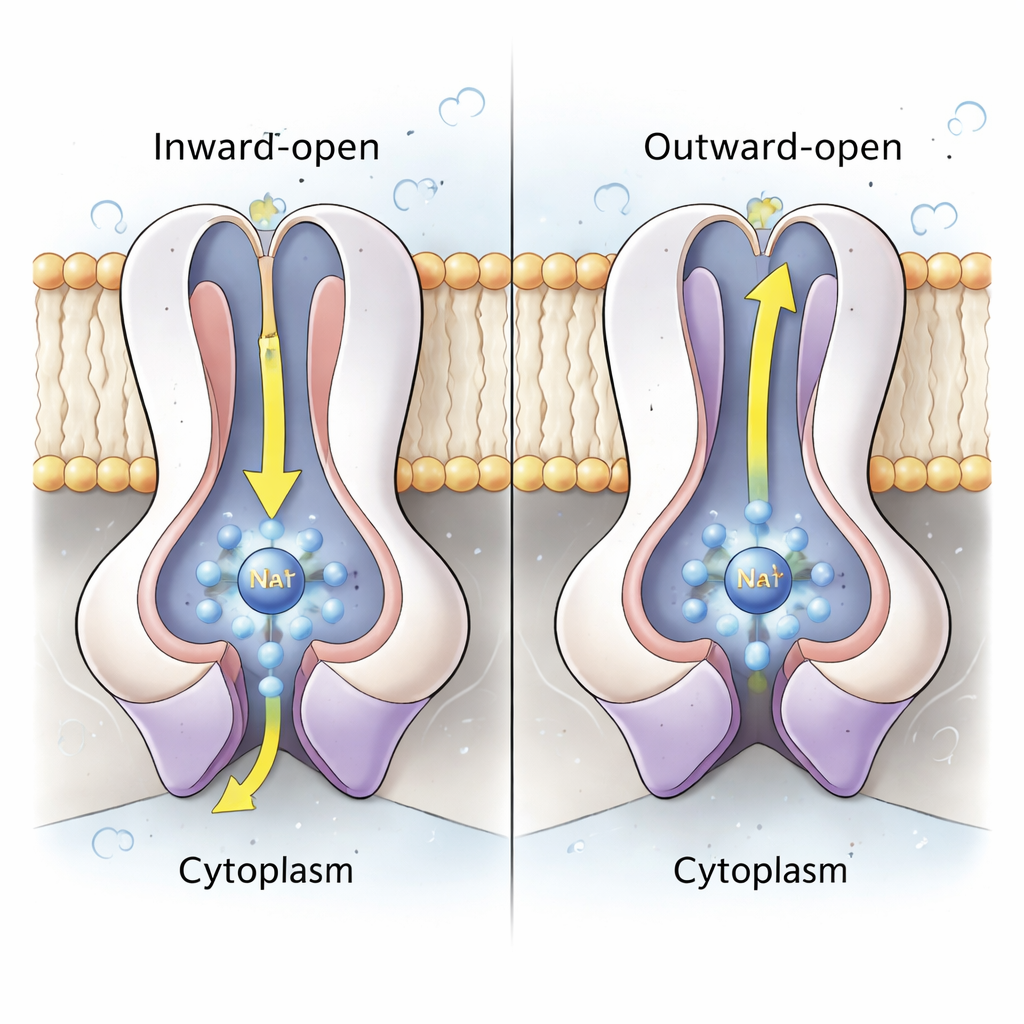
Un cycle coordonné qui verrouille la direction
En combinant tous leurs états structurels et les simulations, les chercheurs proposent un cycle en six étapes. Le NADH se lie d’abord et donne des électrons à NqrF, qui transfère ensuite un électron à NqrD/E, déclenchant la capture de Na⁺ depuis le cytoplasme et le remplissage de la poche centrale. Le changement conformationnel résultant de NqrD/E vers la forme ouverte vers l’extérieur expulse à la fois le Na⁺ vers le périplasme et favorise le déplacement de NqrC pour accepter l’électron. Les étapes suivantes transfèrent les électrons vers les cofacteurs flavine et riboflavine, puis enfin vers la quinone, qui doit recevoir deux électrons pour devenir la quinol. De manière importante, les mêmes changements de conformation qui déplacent le Na⁺ relâchent et rigidifient alternativement NqrF et NqrC, rendant le flux d’électrons en avant probable uniquement lorsque le Na⁺ est pompé vers l’extérieur et décourageant les retours en arrière. Cet couplage aide l’enzyme à pomper le Na⁺ contre un gradient existant, maintenant la « batterie » bactérienne chargée.
Pourquoi cela compte pour la médecine et la biologie
Pour un non-spécialiste, ce travail illustre comment la vie assemble des machines finement chorégraphiées à partir de protéines, où de petits changements de charge déclenchent des mouvements importants et utiles. Pour la recherche sur les maladies infectieuses, il clarifie que la translocation du Na⁺ dans Na⁺-NQR se produit principalement via le cœur NqrD/E, et non via la sous-unité NqrB précédemment suspectée. Cette connaissance affine les sites où les futurs médicaments devraient se lier afin de perturber au mieux le moteur qui alimente Vibrio cholerae et d’autres agents pathogènes, tout en épargnant les enzymes humaines. Plus largement, l’étude fournit une feuille de route structurelle sur la manière dont des réactions redox peuvent être reliées au pompage d’ions — un principe de conception que la nature réutilise dans de nombreuses machineries bioénergétiques.
Citation: Ishikawa-Fukuda, M., Seki, T., Kishikawa, Ji. et al. The redox driven Na+-pumping mechanism in Vibrio cholerae NADH-quinone oxidoreductase relies on dynamic conformational changes. Nat Commun 17, 1394 (2026). https://doi.org/10.1038/s41467-026-69182-w
Mots-clés: pompe à sodium, respiration bactérienne, Na+-NQR, cryo-EM, cibles antibiotiques