Clear Sky Science · fr
Un système synthétique de pyroptose réactif à l'ARN basé sur une nucléase‑protéase CRISPR de type III‑E
Transformer des explosions cellulaires meurtrières en outils ciblés
Nos organismes se défendent parfois en provoquant l'explosion des cellules infectées ou endommagées via une forme d'autodestruction inflammatoire. Cette déflagration élimine non seulement les cellules dangereuses mais attire aussi le système immunitaire. Cette nouvelle étude présente un circuit génétique synthétique, appelé DAMAGE, capable de lire les messages ARN à l'intérieur d'une cellule et de décider si celle‑ci doit être détruite. En reliant un système de défense microbien à la machinerie de mort cellulaire humaine, les chercheurs montrent un moyen d'éliminer sélectivement des cellules infectées par un virus, cancéreuses ou âgées, tout en épargnant les voisines saines. 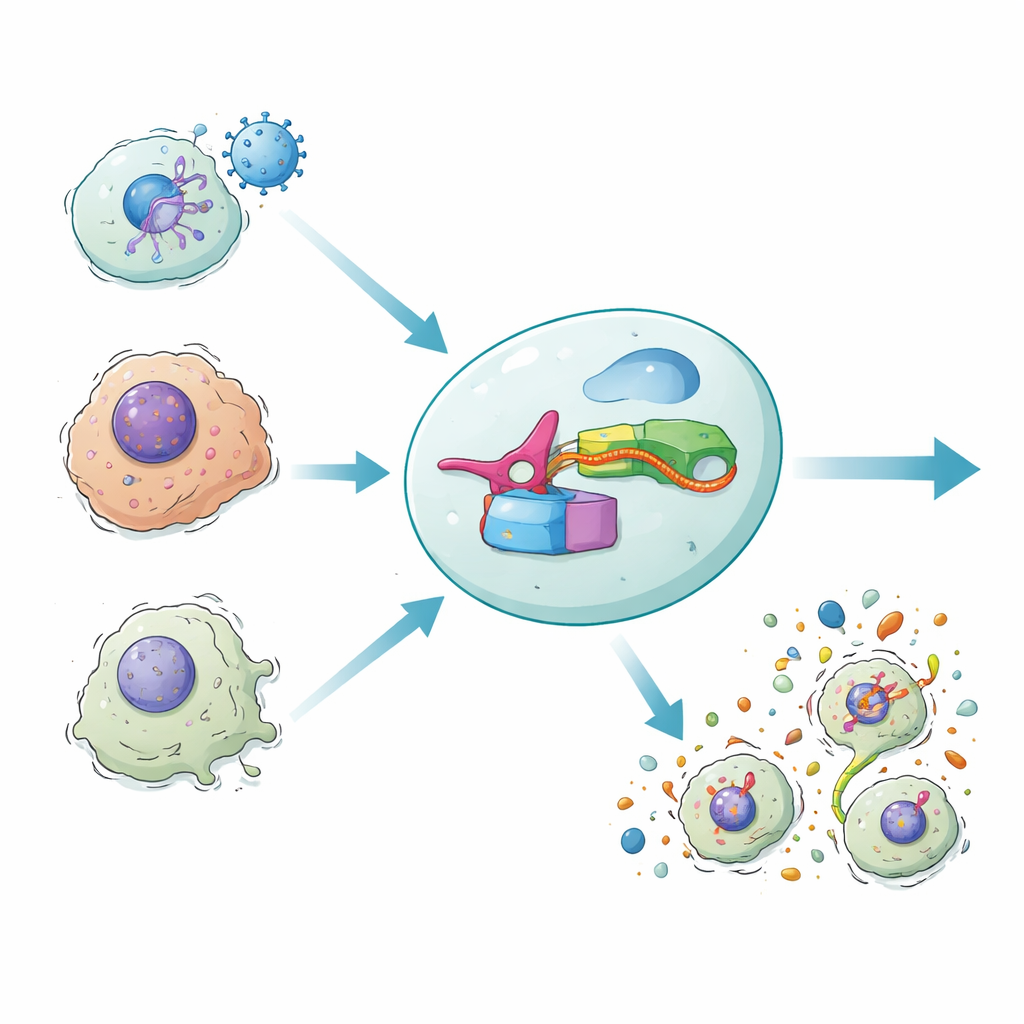
Comment les cellules s'auto‑détruisent normalement
Dans la mort cellulaire inflammatoire, une famille de protéines appelées gasdermines est présente dans les cellules comme des charges prêtes à éclater. Chaque gasdermine comporte une moitié « tueuse » à l'avant capable de percer les membranes cellulaires, et une moitié arrière qui joue le rôle de « capuchon de sécurité » pour la contenir. Quand les senseurs immunitaires détectent un danger, des enzymes coupent les gasdermines en deux, libérant la moitié avant qui assemble des pores dans la membrane externe. La cellule gonfle, éclate et libère des signaux d'alarme qui mobilisent les cellules immunitaires. Cette réponse puissante aide à combattre infections et tumeurs, mais son réseau de contrôle naturel est complexe et difficile à réorienter pour des thérapies.
Emprunter les défenses bactériennes pour lire l'ARN
Les bactéries ont développé des modules de défense compacts connus aujourd'hui via la technologie CRISPR. L'un d'eux, le système de type III‑E, utilise une protéine appelée Cas7‑11 qui peut se lier à des séquences ARN spécifiques à l'aide d'un court ARN guide. Quand Cas7‑11 trouve un ARN cible correspondant, il active une enzyme associée, Csx29, qui clive une protéine partenaire, Csx30. Les auteurs ont réalisé que Csx30 pouvait servir de « charnière » personnalisable entre deux parties protéiques quelconques. Ils ont inséré cette charnière entre les moitiés tueuse et capuchon des gasdermines humaines, créant des effecteurs artificiels qui ne sont séparés que lorsque le senseur de type CRISPR détecte l'ARN choisi à l'intérieur d'une cellule.
Un interrupteur de mort programmable pour les cellules malades
Ce dispositif, nommé DAMAGE (pour Death Manipulation Gene), est composé de cinq éléments : le senseur Cas7‑11, le clivage Csx29, une fusion gasdermine–Csx30, un ARN guide et l'ARN cible dans la cellule. Lorsque le bon message ARN apparaît, Cas7‑11 s'y lie, active Csx29, et Csx29 coupe la charnière Csx30 dans la protéine de fusion. La moitié tueuse de la gasdermine est libérée, perce des pores dans la membrane et la cellule meurt dans une explosion inflammatoire. En changeant simplement l'ARN guide, l'équipe a redirigé DAMAGE vers différents cibles cellulaires. Ils ont montré qu'il pouvait reconnaître l'ARN du virus respiratoire syncytial, des papillomavirus humains à haut risque dans des cellules de cancer du col, et plusieurs mutations oncogéniques de KRAS différant de l'ARN normal d'une seule lettre. Dans chaque cas, les cellules portant l'ARN suspect ont été éliminées de façon sélective, tandis que les cellules témoins voisines restaient intactes. 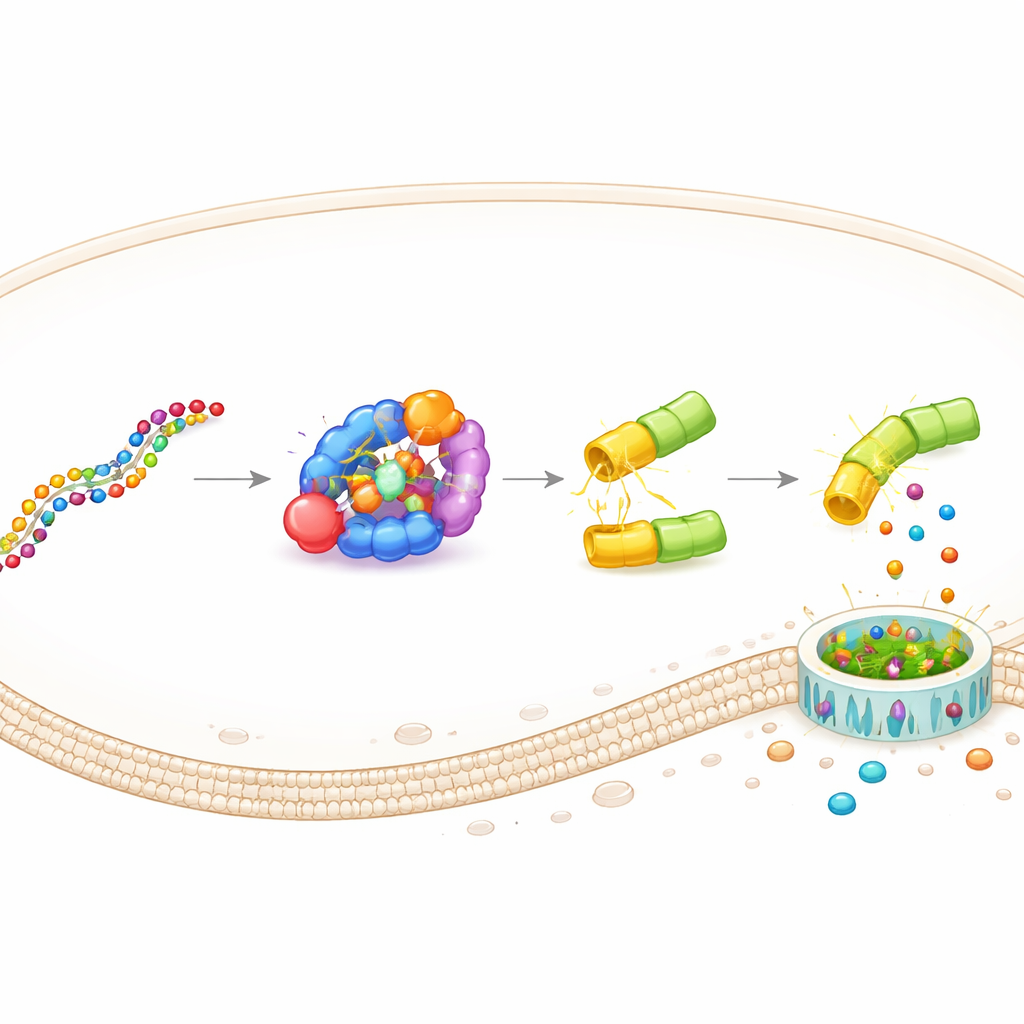
Cibler les cellules âgées
Les chercheurs ont également testé si DAMAGE pouvait traquer les cellules sénescentes — des cellules vieillies ou stressées qui cessent de se diviser mais s'accumulent dans les tissus et contribuent à la fragilité et aux maladies chroniques. Ces cellules augmentent souvent la production de deux protéines gardiennes, p16 et p21. En programmant des guides contre les ARN de p16 et p21, l'équipe a créé une version appelée DAMAGE‑Aging. Ce circuit a tué les cellules présentant de forts niveaux de ces messages tout en épargnant des cellules dont p16 avait été génétiquement supprimé, confirmant que le système lit l'abondance d'ARN en temps réel plutôt que des changements fixes de l'ADN. Des traitements pharmacologiques qui augmentent les niveaux de p16 ou p21 rendaient les cellules plus vulnérables à cette autodestruction ciblée.
Conditionner le système pour de futures thérapies
Pour se rapprocher d'une utilisation pratique, les auteurs ont compressé les nombreuses parties d'ADN de DAMAGE en une construction rationalisée, DAMAGE‑Plus, et ont montré qu'elle fonctionnait toujours de manière fiable. Ils ont ensuite transcrit cette construction en ARNm synthétique, l'ont emballée dans des nanoparticules lipidiques similaires à celles utilisées dans les vaccins COVID‑19, et l'ont délivrée à des cellules en culture. La version ARNm a correctement assemblé le circuit et déclenché la mort inflammatoire ciblée dans des cellules portant des ARN viraux ou liés au cancer. Bien que le système global reste volumineux et n'ait été testé que sur des lignées cellulaires, ces résultats laissent entrevoir que l'élimination cellulaire programmable guidée par l'ARN pourrait un jour être administrée via des formulations d'ARNm injectables.
Une nouvelle façon de lire et de réagir aux messages cellulaires
En termes clairs, DAMAGE est un videur moléculaire qui vérifie « l'identifiant » ARN interne de chaque cellule et n'expulse que celles qui paraissent dangereuses — infectées par un virus, porteuses de mutations ou sénescentes — en les forçant dans une forme explosive d'autodestruction. Le travail démontre que des senseurs ARN bactériens peuvent être couplés à la machinerie de mort cellulaire humaine avec une grande précision, distinguant même des différences d'une seule lettre dans les messages génétiques. Bien qu'il reste beaucoup d'ingénierie à faire avant qu'un tel système puisse être utilisé en toute sécurité chez les animaux ou les humains, il trace une stratégie puissante : lire le brouhaha ARN en direct à l'intérieur des cellules et le traduire directement en décisions de vie ou de mort.
Citation: He, M., Wang, W., Zhou, H. et al. A synthetic system for RNA-responsive pyroptosis based on type III-E CRISPR nuclease-protease. Nat Commun 17, 2565 (2026). https://doi.org/10.1038/s41467-026-69179-5
Mots-clés: pyroptose, CRISPR, thérapie ciblant l'ARN, immunothérapie contre le cancer, sénescence cellulaire