Clear Sky Science · fr
hnRNPM coopère avec BCAS2 pour moduler l’épissage alternatif au cours du développement des ovocytes
Pourquoi la qualité de l’ovocyte compte
Toute vie humaine commence par un seul ovocyte, et pourtant les scientifiques découvrent encore comment ces cellules exceptionnellement grandes se préparent au moment de la fécondation. Bien avant l’arrivée des spermatozoïdes, les ovocytes en croissance accumulent des milliers de messages ARN qui guideront leur maturation et les premiers jours du développement embryonnaire. Cette étude révèle comment une protéine peu connue, travaillant avec une partenaire, édite finement ces messages dans les ovocytes de souris — et ce qui se produit lorsque ce système d’édition fait défaut.
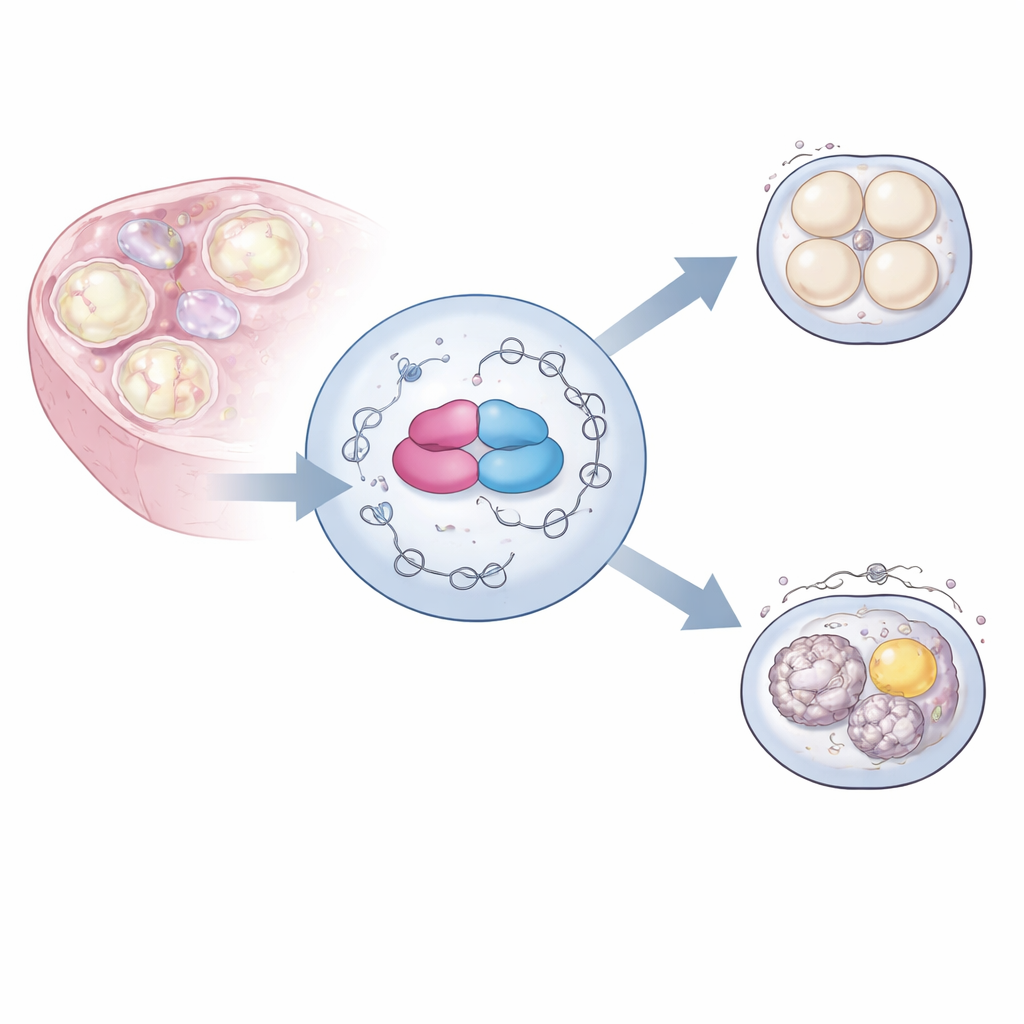
Les gardiens des messages génétiques
Les ovocytes croissent dans l’ovaire pendant des semaines tandis que leur ADN reste largement silencieux. Pendant ce temps, ils accumulent une vaste bibliothèque de messages ARN maternels copiés plus tôt à partir du génome. Ces messages doivent être retaillés et assemblés de différentes manières, un processus appelé épissage alternatif, afin de produire le bon mélange de variantes protéiques aux stades appropriés. Les auteurs se sont concentrés sur une protéine appelée hnRNPM, qui fait partie d’une grande famille de protéines liant l’ARN, et sur sa partenaire BCAS2, toutes deux abondantes dans le système reproducteur féminin. Des travaux antérieurs laissaient entendre que ces protéines se lient à de nombreux ARN dans les ovocytes, mais leur rôle précis dans la fertilité était resté flou.
Ce qui déraille sans cet éditeur
Pour sonder la fonction de hnRNPM, l’équipe a utilisé le génie génétique pour supprimer le gène Hnrnpm spécifiquement dans les précurseurs des ovocytes de souris. Les ovaires de ces femelles semblaient normaux et produisaient un nombre d’ovocytes similaire à celui des témoins. Pourtant, lorsqu’on fécondait ces ovocytes en laboratoire, ils ne dépassaient presque jamais les premières divisions, rendant les femelles complètement infertiles. Un examen plus attentif des ovocytes immatures a révélé des amas sombres dans un cytoplasme normalement clair. La microscopie électronique a montré qu’un fin échafaudage interne appelé lattice cytoplasmique était en grande partie absent, et que des organites clés tels que les mitochondries et les gouttelettes lipidiques étaient anormalement regroupés plutôt que répartis uniformément. Ces changements témoignaient d’un grave problème d’organisation interne de l’ovocyte.
Mécanique de division cellulaire compromise
Les mêmes ovocytes mutants peinaient aussi à achever la méiose, la division cellulaire spéciale qui réduit de moitié le nombre de chromosomes. Lorsque les chercheurs ont fait mûrir les ovocytes en culture, ils pouvaient initier la méiose mais s’arrêtaient généralement avant de la terminer. Au microscope, les structures qui séparent les chromosomes — les fuseaux — étaient tordues, multipolaires ou mal ancrées. Une protéine appelée péricentrine, qui aide à organiser les pôles du fuseau, apparaissait tardivement et aux mauvais endroits. Ensemble, ces défauts empêchaient les ovocytes d’aligner et de séparer les chromosomes de façon fiable, ce qui explique probablement l’échec complet du développement après la fécondation.
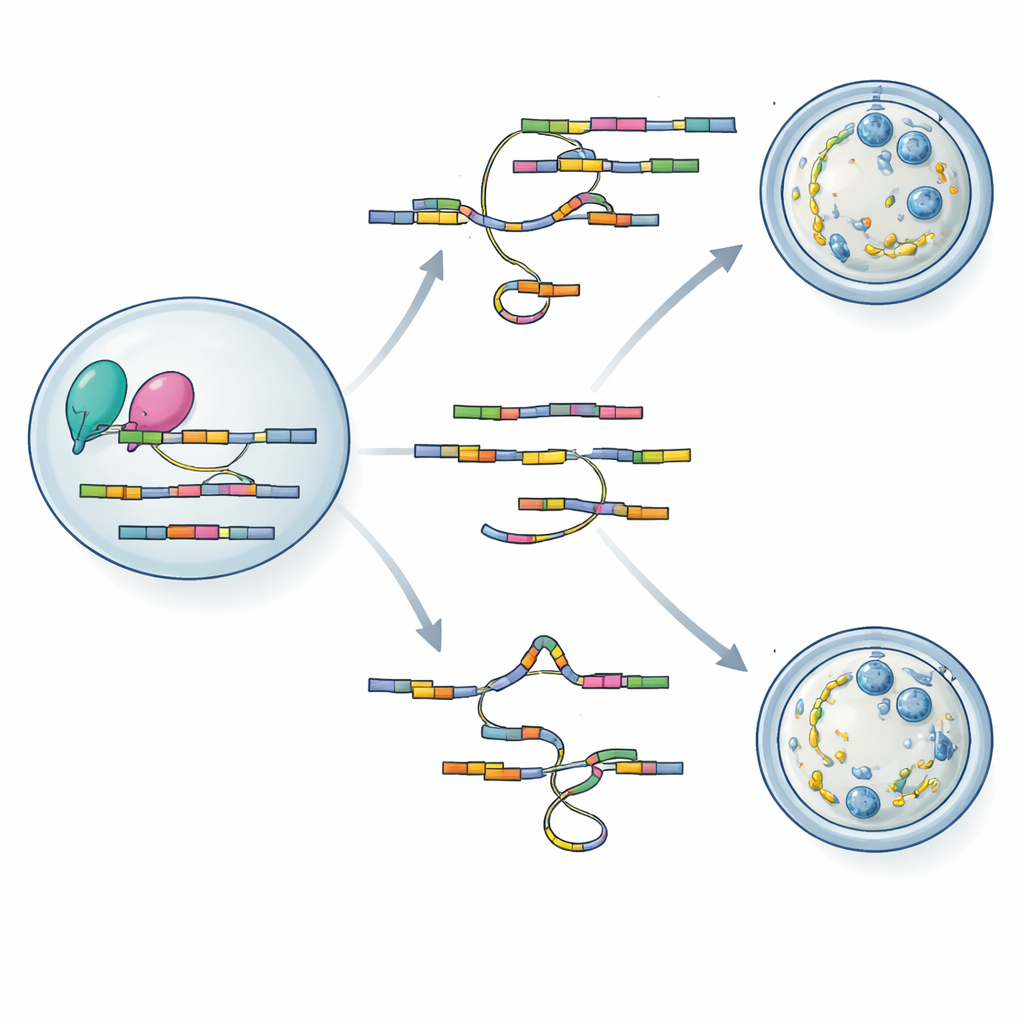
Lire et réécrire les instructions ARN
Pour comprendre comment la perte de hnRNPM conduit à de tels défauts généralisés, l’équipe a eu recours à deux puissantes méthodes de séquençage adaptées aux échantillons d’ovocytes minces. En utilisant SCAN-seq, qui lit des molécules d’ARN en longueur complète à partir d’ovocytes individuels, ils ont découvert plus d’un millier de modifications d’épissage dans les ovocytes mutants, y compris de nombreux variants ARN auparavant inconnus. Les gènes impliqués dans la construction du lattice cytoplasmique, le contrôle du comportement du fuseau et la régulation du cycle méiotique étaient particulièrement touchés. Une seconde méthode, LACE-seq, a cartographié avec précision où hnRNPM se lie sur les ARN, révélant une préférence pour des trames riches en GU à l’intérieur des exons. En superposant les deux jeux de données, les auteurs ont montré que hnRNPM se positionne directement sur de nombreux messages dont l’épissage change lorsque la protéine est absente, liant ainsi son activité de liaison à la précision de l’épissage.
Un modèle de travail d’équipe pour le contrôle de l’ovocyte
Des études d’interaction protéique ont montré que hnRNPM s’associe physiquement à BCAS2 et à des composants centraux de la machinerie d’épissage. Les deux partenaires se lient à de nombreuses cibles ARN communes et altèrent souvent ces cibles de la même façon lorsque l’une ou l’autre des protéines est perturbée. De manière intrigante, la perte de hnRNPM réduisait le niveau de protéine BCAS2 et affaiblissait l’empreinte de BCAS2 sur les cibles ARN partagées, ce qui suggère que hnRNPM n’édite pas seulement les messages mais aide aussi à stabiliser sa partenaire sur ces messages. Les auteurs proposent un modèle dans lequel hnRNPM et BCAS2 forment un complexe coopératif qui ajuste des ARN maternels clés pendant la croissance des ovocytes, garantissant l’assemblage correct du lattice cytoplasmique et une division méiotique fiable.
Ce que cela signifie pour la fertilité
Concrètement, ce travail montre qu’une équipe d’édition moléculaire — hnRNPM et BCAS2 — agit en coulisses pour préparer les ovocytes à la vie après la fécondation. Quand cette équipe fait défaut, l’échafaudage interne de l’ovocyte s’effondre, sa machinerie de tri des chromosomes dysfonctionne, et même si l’ovocyte est produit en nombre normal, il ne peut pas soutenir le développement embryonnaire. Parce que hnRNPM est très similaire chez la souris et l’homme, ces découvertes mettent en lumière un système de contrôle qualité conservé qui pourrait sous-tendre certaines formes d’infertilité féminine inexpliquée et offrir de nouveaux points d’accès pour le diagnostic ou le traitement.
Citation: Zhou, S., Liu, D., Gan, S. et al. hnRNPM cooperates with BCAS2 to modulate alternative splicing during oocyte development. Nat Commun 17, 2681 (2026). https://doi.org/10.1038/s41467-026-69176-8
Mots-clés: développement des ovocytes, épissage alternatif, infertilité féminine, protéines liant l’ARN, lattice cytoplasmique