Clear Sky Science · fr
Impact des forces du solvant et de la symétrie brisée sur l’assemblage de protéines conçues à une interface liquide‑solide
Pourquoi ce monde minuscule à la surface compte
Des cellules solaires aux capteurs médicaux, de nombreuses technologies futures dépendront de la construction de structures précises là où des molécules biologiques rencontrent des matériaux solides. Cette étude examine comment des « tiges » protéiques conçues sur mesure s’organisent sur des surfaces minérales en solution saline. La leçon surprenante est que l’eau au contact de la surface, et des asymétries subtiles dans le cristal sous‑jacent, peuvent modifier complètement l’alignement de ces protéines — produisant parfois des motifs que la théorie classique juge improbables.
Concevoir des protéines pour s’adapter à un cristal
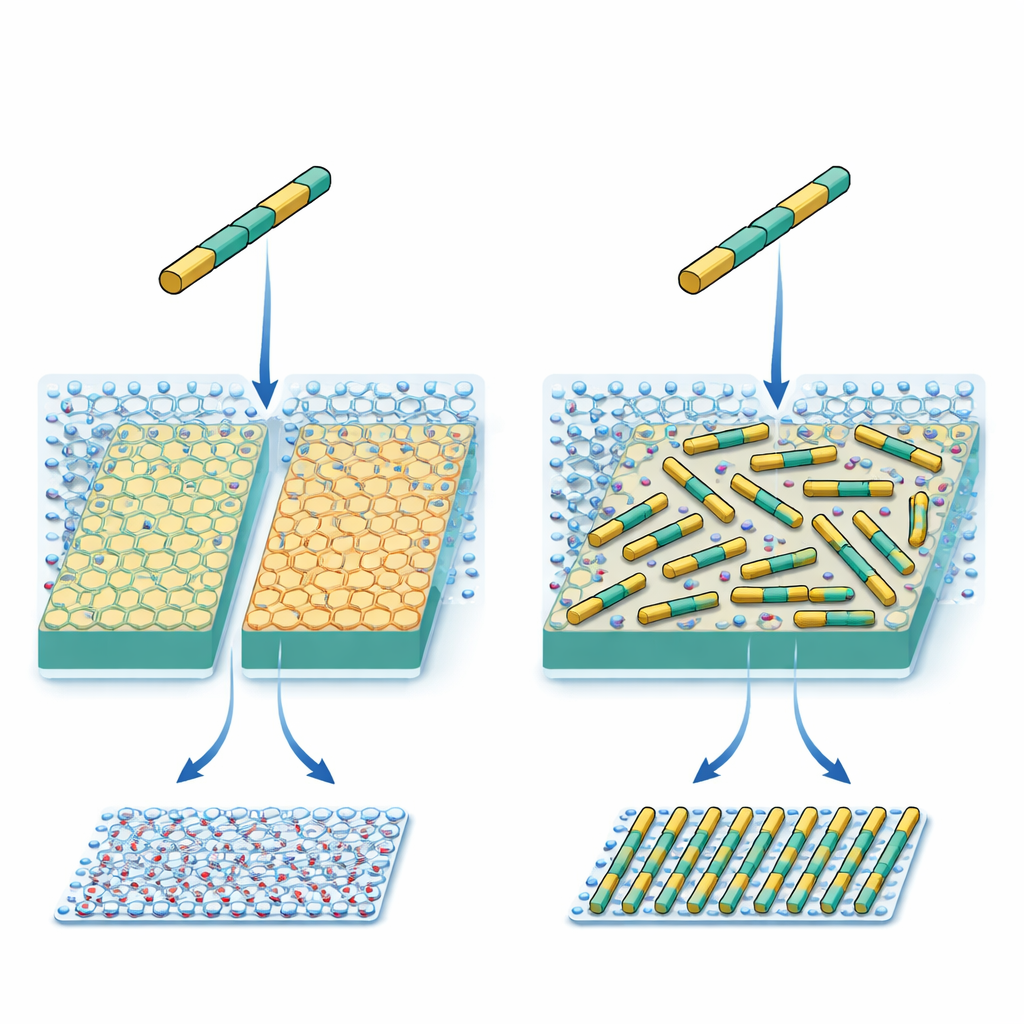
Les chercheurs travaillent avec une protéine synthétique en forme de courte tige rigide. Sa chimie de surface et le positionnement de ses groupes chargés ont été soigneusement conçus pour correspondre au réseau d’ions potassium d’un minéral courant, la mica. En principe, cela devrait amener chaque tige protéique à préférer trois directions équivalentes sur la surface cristalline, comme l’alignement le long de trois rayons d’une roue. Des travaux antérieurs ont montré que, malgré une telle conception soignée, les protéines formaient plusieurs motifs inattendus au lieu d’un seul prévu par les ingénieurs. Cette incohérence suggérait qu’une force importante manquait dans les règles de conception actuelles.
Deux surfaces presque identiques, deux résultats très différents
Pour suivre ce qui se passait, l’équipe a utilisé la microscopie à force atomique à grande vitesse, capable d’observer en temps réel le mouvement et l’assemblage de tiges protéiques individuelles sur une surface. Ils ont comparé deux formes de mica étroitement apparentées. Les deux exposent le même réseau de potassium, mais leurs structures atomiques internes diffèrent légèrement, ce qui modifie la manière dont l’eau s’organise en couches juste au‑dessus de la surface. À des concentrations salines modestes, les tiges formaient un tapis dense mais localement désordonné sur les deux surfaces, avec seulement de petits amas alignés. Lorsque la concentration en sel était très élevée, en revanche, le comportement divergea : sur un type de mica les tiges restèrent désordonnées le long des trois directions, tandis que sur l’autre elles formèrent spontanément de longues rangées parallèles et régulièrement espacées sur l’ensemble de la surface.
Couches d’eau et symétrie brisée
La modélisation numérique des minéraux et de l’eau environnante a aidé à expliquer cette personnalité double. Sur la forme de mica la plus symétrique, les première et deuxième couches de molécules d’eau conservent un motif hexagonal régulier. Sur la forme moins symétrique, des atomes internes et des groupes enfouis dans le cristal rompent cette symétrie triple, et ce motif brisé se transmet aux couches d’eau voisines, qui développent des régions en bandes. Les protéines n’entrent pas en contact avec le cristal nu ; elles interagissent aussi avec cette eau structurée. En conséquence, une orientation des tiges devient légèrement plus favorable que les deux autres, même si la concordance conçue protéine–cristal suggérerait que les trois orientations devraient être équivalentes.
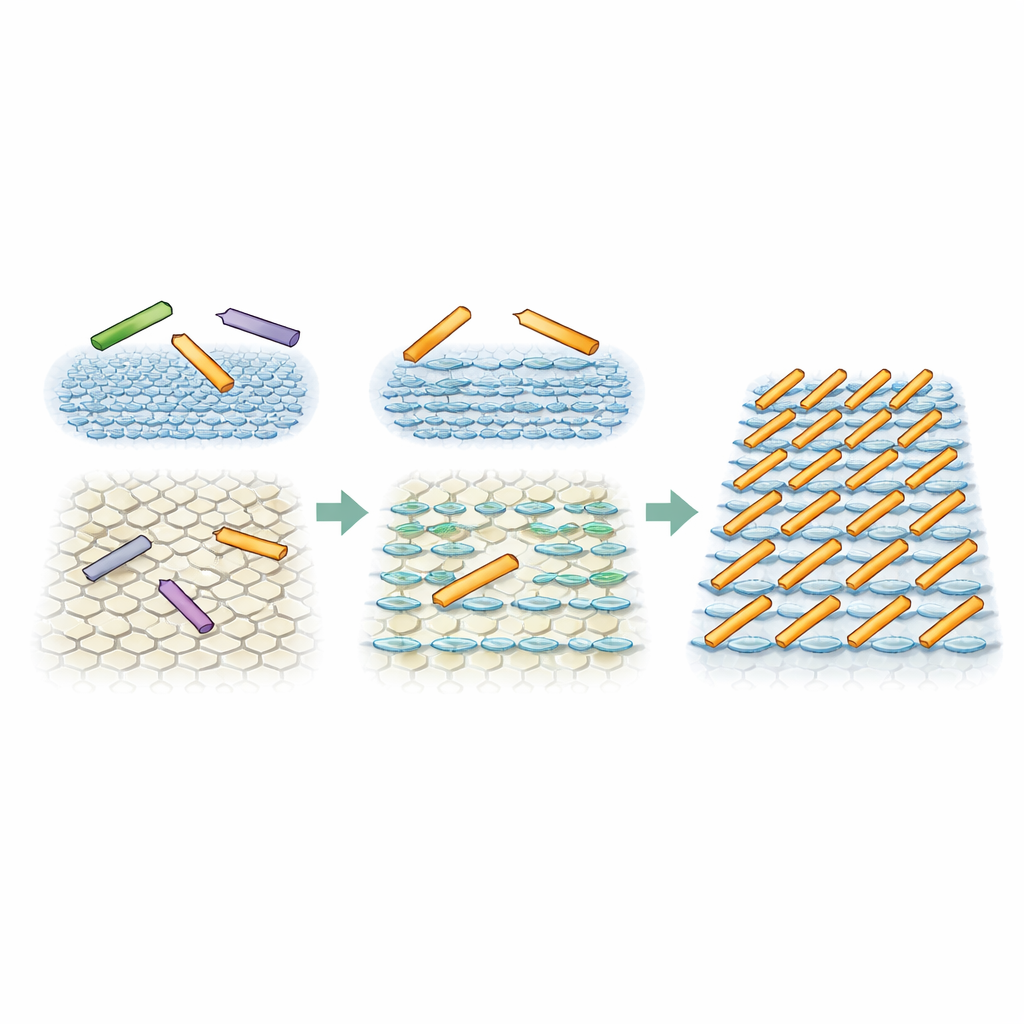
Les simulations révèlent une phase inattendue
Pour tester si un biais directionnel subtil de l’environnement de surface pouvait vraiment expliquer les motifs observés, les chercheurs ont exécuté des simulations Monte Carlo de rectangles durs simples représentant les tiges protéiques. Dans un ensemble de simulations, les trois orientations étaient également probables, imitant la surface pleinement symétrique. Dans ce cas, les tiges restaient dans un état dense mais désordonné, avec seulement des alignements temporaires ou limités, exactement comme observé sur un type de mica. Dans un second ensemble, une direction fut rendue seulement modestement plus favorable — environ deux fois plus probable que les deux autres — incarnant l’influence des couches d’eau en bandes. Dans ces conditions, et lorsque les tiges pouvaient suffisamment se déplacer, le système évoluait naturellement vers un état de rangées parallèles et régulièrement espacées. Il s’agit d’une phase dite smectique, que la théorie classique considère comme improbable pour des tiges non interactives en deux dimensions, pourtant la petite poussée directionnelle de l’interface la rend stable.
Repenser la conception de matériaux bio‑inspirés
En termes simples, ce travail montre qu’une chimie protéine–surface finement réglée ne suffit pas pour prédire comment des protéines conçues s’organiseront sur des matériaux réels. L’eau intercalée entre la protéine et le solide, et la manière dont le cristal rompt subtilement la symétrie, peuvent orienter l’assemblage vers des motifs que les modèles classiques n’auraient jamais anticipés. En combinant microscopie à grande vitesse, apprentissage automatique pour quantifier l’ordre, et simulations fondées sur la physique, l’étude propose un moyen d’intégrer ces effets cachés du solvant et de la symétrie dans de futurs outils de conception protéique. Pour quiconque souhaite concevoir des matériaux hybrides bio‑inorganiques fiables, le message est clair : il faut concevoir non seulement pour la protéine et la surface, mais aussi pour la couche d’eau structurée qui les relie.
Citation: Yadav Schmid, S., Helfrecht, B., Stegmann, A. et al. Impact of solvent forces and broken symmetry on the assembly of designed proteins at a liquid-solid interface. Nat Commun 17, 2446 (2026). https://doi.org/10.1038/s41467-026-69170-0
Mots-clés: auto‑assemblage des protéines, interfaces liquide‑solide, structure de l’eau interfaciale, ordre smectique, matériaux bioinspirés