Clear Sky Science · fr
Un mécanisme d’adaptateur multivalent dirige l’importation nucléaire des protéasomes
Comment les cellules gardent leurs salles de contrôle propres
À l’intérieur de chaque cellule, le noyau fait office de centre de commandement, rempli d’ADN et des protéines qui régulent l’activation ou la répression des gènes. Pour maintenir cette salle de contrôle en bon état de fonctionnement, les cellules s’appuient sur de puissants « destructeurs » moléculaires appelés protéasomes, qui décomposent les protéines usées ou défectueuses. Cet article révèle comment les cellules gèrent la tâche étonnamment délicate de faire traverser ces protéasomes encombrants par les passages étroits menant au noyau, au bon moment.
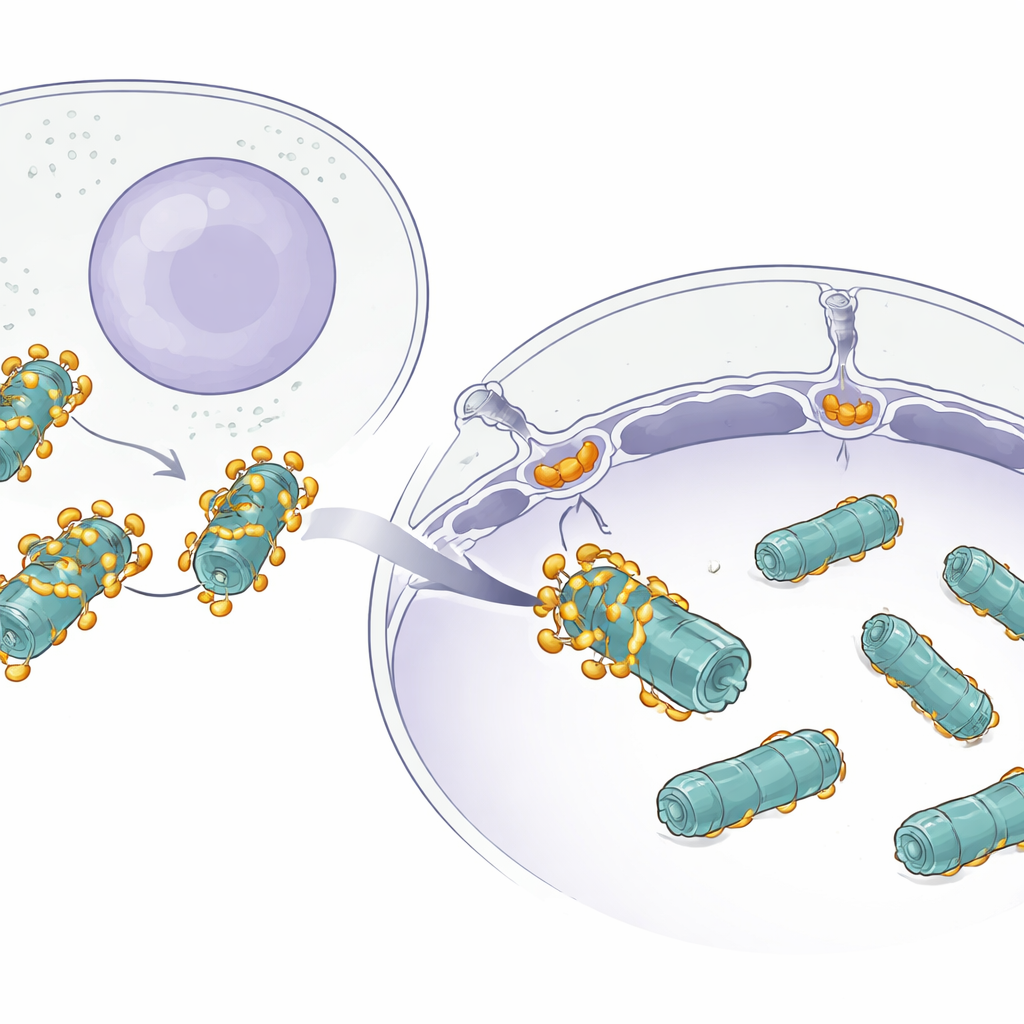
Le défi de déplacer de grosses machines
De nombreuses protéines transitent discrètement entre le cytoplasme et le noyau par d’imposantes portes de l’enveloppe nucléaire appelées pores nucléaires. Les petites protéines peuvent passer facilement, mais les grandes machines comme les protéasomes sont une autre affaire : ce sont des complexes massifs en forme de baril, composés de nombreuses pièces. Les chercheurs savaient déjà que les petits cargos utilisent des protéines d’aide appelées importines pour entrer dans le noyau, mais il restait obscur comment quelque chose d’aussi volumineux qu’un protéasome peut passer efficacement sans se coincer ni se perdre.
Un assistant polymorphe se précise
L’équipe s’est concentrée sur une petite protéine flexible appelée AKIRIN2, dont des travaux antérieurs avaient montré qu’elle est absolument nécessaire pour l’entrée des protéasomes dans le noyau. Les cellules qui se divisent sans AKIRIN2 ne peuvent pas importer les protéasomes dans le noyau et meurent rapidement parce que des protéines nucléaires endommagées s’accumulent. Grâce à une combinaison de méthodes — notamment un vaste scan mutationnel ayant modifié presque chaque acide aminé d’AKIRIN2, la cryo‑microscopie électronique haute résolution pour visualiser le complexe en 3D, et des tests biochimiques précis — les chercheurs ont cartographié les parties d’AKIRIN2 qui importent et leur rôle. Ils ont découvert un segment « en aile » jusque‑là méconnu et une région en hélice qui permet à AKIRIN2 de former des dimères (paires), deux éléments essentiels pour saisir les protéasomes et d’autres partenaires.
Construction d’une poignée de transport à plusieurs mains
Les images structurelles ont révélé que plusieurs copies d’AKIRIN2 s’agrègent d’un côté du protéasome comme autant de mains saisissant le même objet. Chaque paire d’AKIRIN2 se lie à des sites spécifiques à la surface externe du protéasome tout en interagissant avec différentes importines. Une importine, IPO9, se fixe à AKIRIN2 de manière inhabituelle, l’enveloppant et modifiant sa conformation au fur et à mesure de l’assemblage du complexe. D’autres importines, elles‑mêmes présentes en paires, reconnaissent de courts signaux d’entrée nucléaire portés par AKIRIN2. Parce que plusieurs molécules d’AKIRIN2 se trouvent sur le même protéasome, elles exposent collectivement de nombreux de ces signaux en même temps. Cette « poignée » multivalente permet à une cohorte d’importines de s’accrocher simultanément, fournissant au protéasome massif assez de force d’entraînement pour traverser le pore nucléaire.
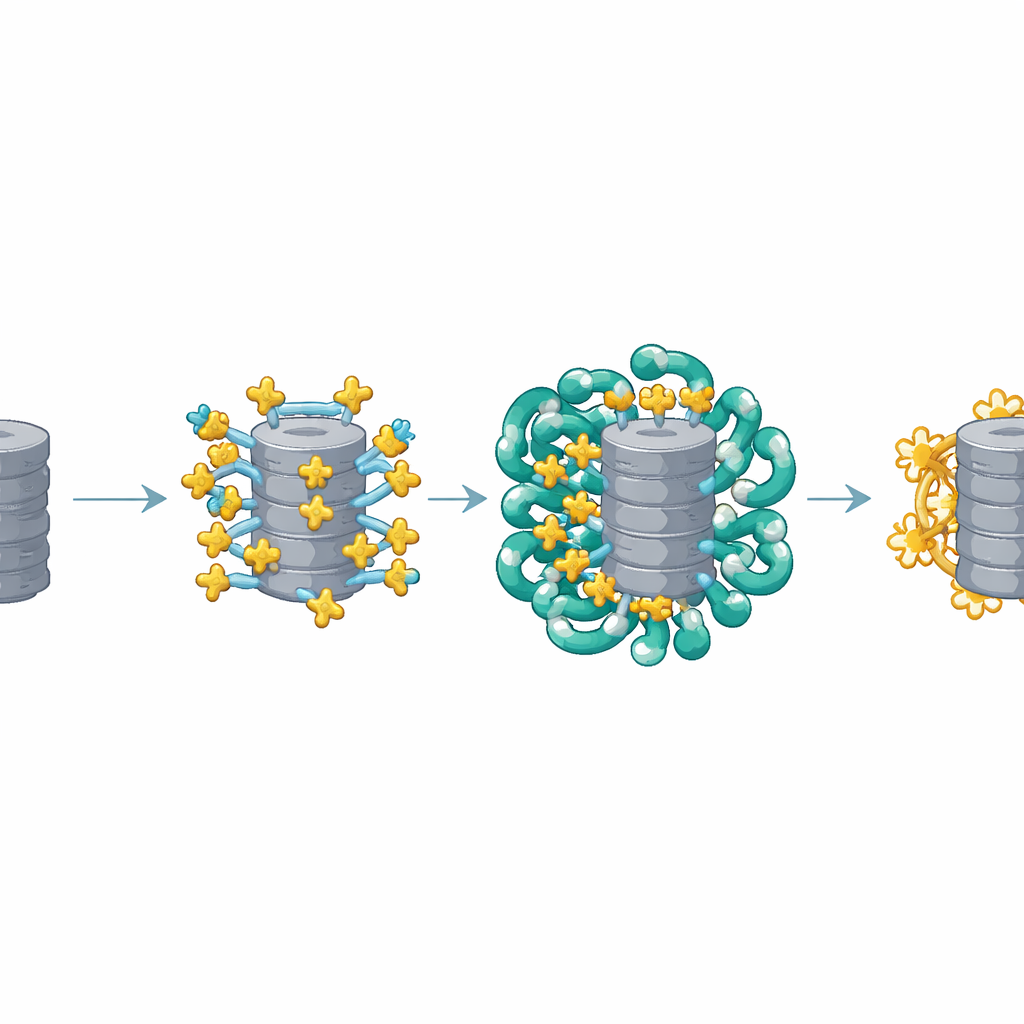
Un cycle d’assemblage et de libération astucieux
Des expériences de reconstitution dans un système épuré en éprouvette ont montré que les protéasomes n’entrent efficacement dans les noyaux que lorsque AKIRIN2 et les importines sont présentes ensemble. Plus il y a d’AKIRIN2, plus l’importation est forte et rapide. Une fois dans le noyau, la machinerie de transport doit être dégagée pour que les protéasomes puissent fonctionner. La cellule utilise ici une libération en deux étapes. Une petite protéine commutatrice appelée Ran, sous sa forme liée au GTP, détache la plupart des importines de leur cargo. AKIRIN2 et une partie d’IPO9 restent plus tenacement liés, mais le noyau dispose d’un plan B : les protéasomes nucléaires détruisent directement AKIRIN2, sans le marquer par l’ubiquitine comme c’est généralement le cas. Des mesures au cours du cycle cellulaire montrent qu’AKIRIN2 atteint un pic pendant la division cellulaire, lorsque de nouveaux noyaux se forment, puis décroît au début de la phase G1, cohérent avec ce nettoyage ciblé.
Pourquoi cela dépasse l’intérêt d’une seule protéine
Dans l’ensemble, ces résultats montrent qu’AKIRIN2 agit comme un échafaudage flexible qui rassemble de nombreuses importines sur un seul protéasome, transformant un problème de transport difficile en un effort de groupe coordonné. En concentrant des signaux d’entrée nucléaire sur un adaptateur plutôt que sur le protéasome lui‑même, les cellules peuvent contrôler quand et avec quelle intensité de grosses machines pénètrent dans le noyau sans repenser ces machines. Des stratégies basées sur des adaptateurs similaires semblent être utilisées pour d’autres grands assemblages protéiques, et même des virus exploitent des astuces apparentées pour envahir le noyau. Comprendre cette logique générale du transport enrichit notre compréhension de la manière dont les cellules maintiennent l’équilibre protéique dans leur compartiment le plus sensible et pourrait, à terme, ouvrir des pistes d’intervention lorsque la dégradation des protéines ou la fonction nucléaire dysfonctionnent.
Citation: Brunner, H.L., Kalis, R.W., Grundmann, L. et al. A multivalent adaptor mechanism drives the nuclear import of proteasomes. Nat Commun 17, 2359 (2026). https://doi.org/10.1038/s41467-026-69162-0
Mots-clés: transport nucléaire, protéasome, AKIRIN2, importine, dégradation des protéines