Clear Sky Science · fr
Une approche intégrative de biologie structurale révèle l’organisation dynamique du chaperon quaternaire R2SP
Comment les cellules construisent des machines moléculaires complexes
À l’intérieur de chaque cellule, de nombreuses protéines ne fonctionnent pas seules : elles doivent s’assembler en machines élaborées avant de pouvoir accomplir leur rôle. Réussir cette étape d’assemblage est essentiel pour une respiration, un mouvement et même une fertilité sains. Cet article examine l’un de ces assistants d’assemblage, une « équipe de construction » moléculaire nommée complexe R2SP, et montre comment il est organisé et comment il fonctionne. Comprendre R2SP est important car lorsque ses composants font défaut, de petites structures filiformes à la surface des cellules — les cils — ne bougent pas correctement, entraînant des troubles respiratoires chroniques et d’autres maladies.
Les équipes de construction cellulaires R2TP et R2SP
Les cellules s’appuient sur des équipes de protéines auxiliaires, appelées complexes chaperons, pour guider d’autres protéines vers les formes multipartites correctes. Une équipe étudiée de longue date, appelée R2TP, se trouve dans de nombreux tissus et aide à assembler de grandes machines telles que les usines de production d’ARN et les capteurs de dommages de l’ADN. R2SP est une cousine proche de R2TP : les deux s’articulent autour du même moteur en anneau formé de deux protéines partenaires, RUVBL1 et RUVBL2, qui consomment la molécule d’énergie ATP. Ce qui diffère, ce sont les adaptateurs accessoires qui connectent les clients à ce moteur. R2TP utilise des adaptateurs appelés RPAP3 et PIH1D1, tandis que R2SP utilise SPAG1 et PIH1D2. Ces petites différences de pièces confèrent aux deux complexes des listes de clients différentes et relient en particulier R2SP à la construction des cils mobiles qui balaient le mucus et les fluides à la surface des tissus.
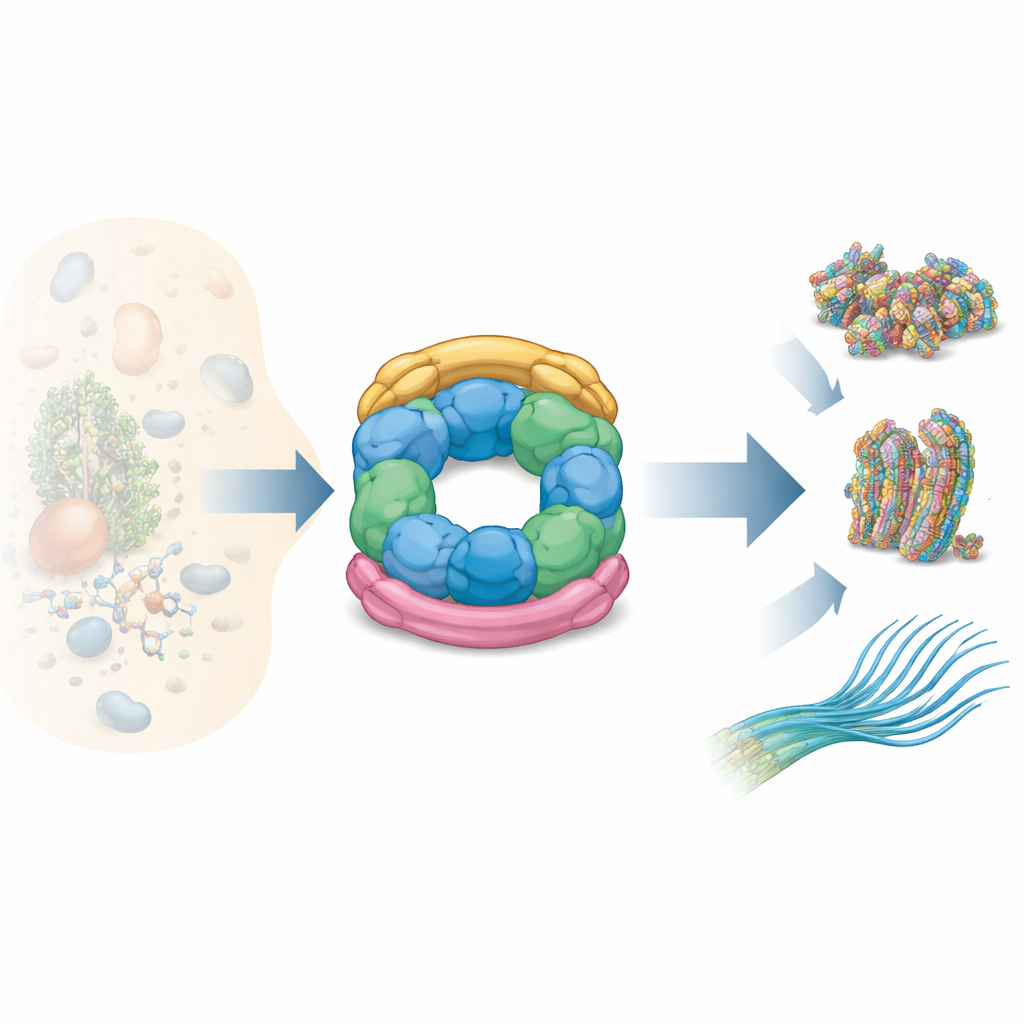
Comment les pièces de R2SP s’emboîtent
Les auteurs ont combiné plusieurs techniques structurelles — résonance magnétique nucléaire, cryo‑microscopie électronique et spectrométrie de masse après cross‑linking — avec des tests biochimiques pour cartographier la construction de R2SP. Ils ont montré que l’extrémité en queue de SPAG1 saisit l’anneau RUVBL1/RUVBL2 d’une manière qui ressemble à la liaison de RPAP3 dans R2TP, mais avec des ajustements clés de forme et de points de contact. Un second adaptateur, PIH1D2, se loge sous l’anneau et atteint également les domaines latéraux flexibles du moteur. Ces domaines latéraux agissent comme des bras articulés qui aident à transmettre les mouvements du noyau consommateur d’ATP vers les clients liés. Les données révèlent que SPAG1 et PIH1D2 ne s’attachent pas de manière indépendante : ils coopèrent, formant une unité couplée qui pince l’anneau par le haut et par le bas, stabilisant une architecture tridimensionnelle distinctive.
Un anneau dynamique qui change de vitesse
Au‑delà d’images statiques, l’équipe a étudié le comportement de R2SP. À l’aide de mesures d’interaction, ils ont constaté que le moteur RUVBL1/RUVBL2 peut exister soit comme un anneau simple, soit comme un double anneau empilé. Lorsque SPAG1 et PIH1D2 se lient, ils déplacent fortement cet équilibre en faveur de la forme en anneau simple et peuvent la décorer avec jusqu’à trois paires d’adaptateurs. Parallèlement, les adaptateurs augmentent nettement l’activité de consommation d’ATP du moteur et modifient la vitesse d’association/dissociation des molécules apparentées à l’ATP aux sites actifs. Comparés au système R2TP, SPAG1 et PIH1D2 favorisent différentes étapes de la libération du nucléotide, ce qui suggère que R2SP règle le cycle énergétique du moteur central de sa propre manière. Cet usage finement contrôlé de l’énergie serait ce qui alimente l’assemblage progressif des complexes clients nécessaires aux cils mobiles.
Une plate‑forme flexible pour construire les composants des cils
En intégrant toutes leurs contraintes structurelles dans un modèle unique, les auteurs proposent que R2SP fonctionne comme une plate‑forme flexible à nombreux bras. La queue de SPAG1 s’ancre fermement au sommet de l’anneau, tandis que ses autres régions et les deux domaines de PIH1D2 s’étendent vers le côté plus ouvert et semblable à un bras du moteur. C’est sur ce côté que les protéines clientes et les chaperons auxiliaires tels que HSP70 et HSP90 s’amarrent très probablement. Parce que jusqu’à trois unités SPAG1–PIH1D2 peuvent se fixer sur un même anneau et que les bras flexibles sont en mouvement constant, l’ensemble du complexe ressemble à une pieuvre dont les tentacules peuvent saisir plusieurs éléments clients à la fois, les coordonner et les transférer pour qu’ils soient assemblés en structures ciliaires plus grandes.
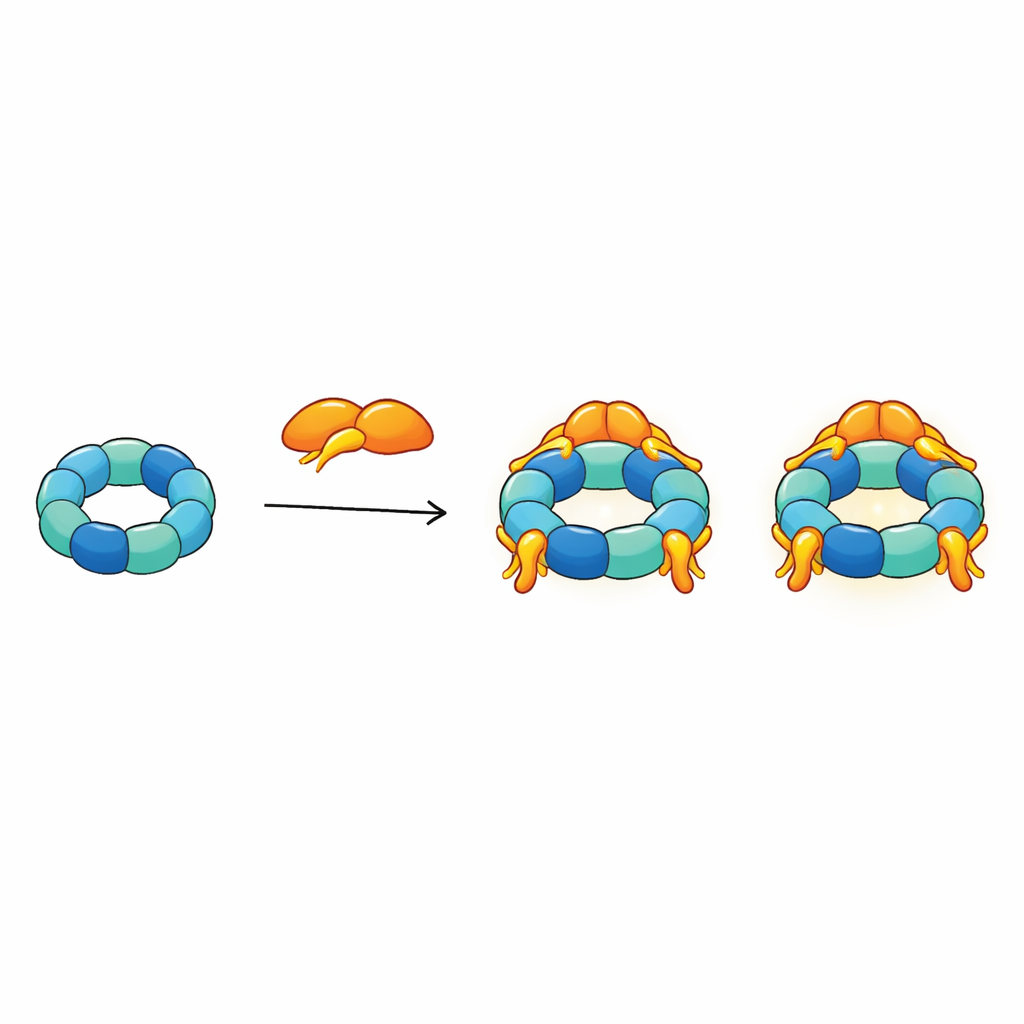
Ce que cela signifie pour la santé et la maladie
Pour les non‑spécialistes, le message principal est que R2SP est une version spécialisée d’une machine de construction cellulaire générale, reconfigurée par l’échange de seulement deux protéines adaptatrices. Cet échange modifie à la fois le contrôle du moteur central et la façon dont les clients sont positionnés, expliquant pourquoi R2SP se concentre sur la fabrication de pièces pour les cils mobiles tandis que R2TP sert d’autres usines cellulaires. Des défauts de SPAG1 sont déjà connus pour provoquer la dyskinésie ciliaire primaire, un trouble marqué par des infections chroniques et des problèmes de fertilité. En révélant la disposition détaillée et les principes de fonctionnement de R2SP, cette étude jette les bases pour comprendre comment des mutations spécifiques perturbent l’assemblage des cils et pourrait éventuellement guider des traitements ciblés visant à restaurer ou moduler cette équipe de construction moléculaire cruciale.
Citation: Santo, P.E., Chagot, ME., Gizardin-Fredon, H. et al. An integrative structural biology approach reveals the dynamic organization of the R2SP quaternary chaperone complex. Nat Commun 17, 2605 (2026). https://doi.org/10.1038/s41467-026-69157-x
Mots-clés: chaperons moléculaires, assemblage de complexes protéiques, cilia mobiles, biologie structurale, RUVBL1 RUVBL2