Clear Sky Science · fr
Base structurelle de la traduction mitochondriale efficace médiée par TACO1
Maintenir la bonne marche des centrales énergétiques cellulaires
Les mitochondries sont souvent qualifiées de centrales électriques de nos cellules parce qu’elles produisent la molécule énergétique ATP. Pour cela, elles doivent assembler un petit mais indispensable ensemble de protéines à l’aide de leurs propres usines spécialisées, appelées mitoribosomes. Cette étude révèle comment une protéine aide-ménagère peu connue, TACO1, ajuste finement ces machines afin qu’elles continuent de fonctionner sans à-coups, en particulier lorsqu’elles rencontrent des segments « difficiles » dans la chaîne protéique qui tendent à provoquer des blocages.
Des usines d’énergie avec leur propre matériel
Contrairement à la majorité de la synthèse protéique, qui a lieu dans le milieu aqueux de la cellule, la fabrication des protéines mitochondriales se déroule sur des mitoribosomes ancrés à la membrane interne de la mitochondrie — la même membrane qui accueille de nombreuses enzymes productrices d’énergie. En utilisant la cryo‑microscopie électronique de pointe sur des mitochondries humaines intactes, les auteurs ont obtenu des instantanés quasi atomiques de ces mitoribosomes dans leur environnement naturel. Ils ont constaté que tous les mitoribosomes saisis étaient attachés à la membrane interne et positionnés de façon à ce que les chaînes protéiques nouvellement synthétisées puissent être directement acheminées vers un insertase membranaire, une sorte de fente moléculaire qui enfourne les protéines fraîchement synthétisées dans la membrane où elles sont nécessaires à la production d’énergie. 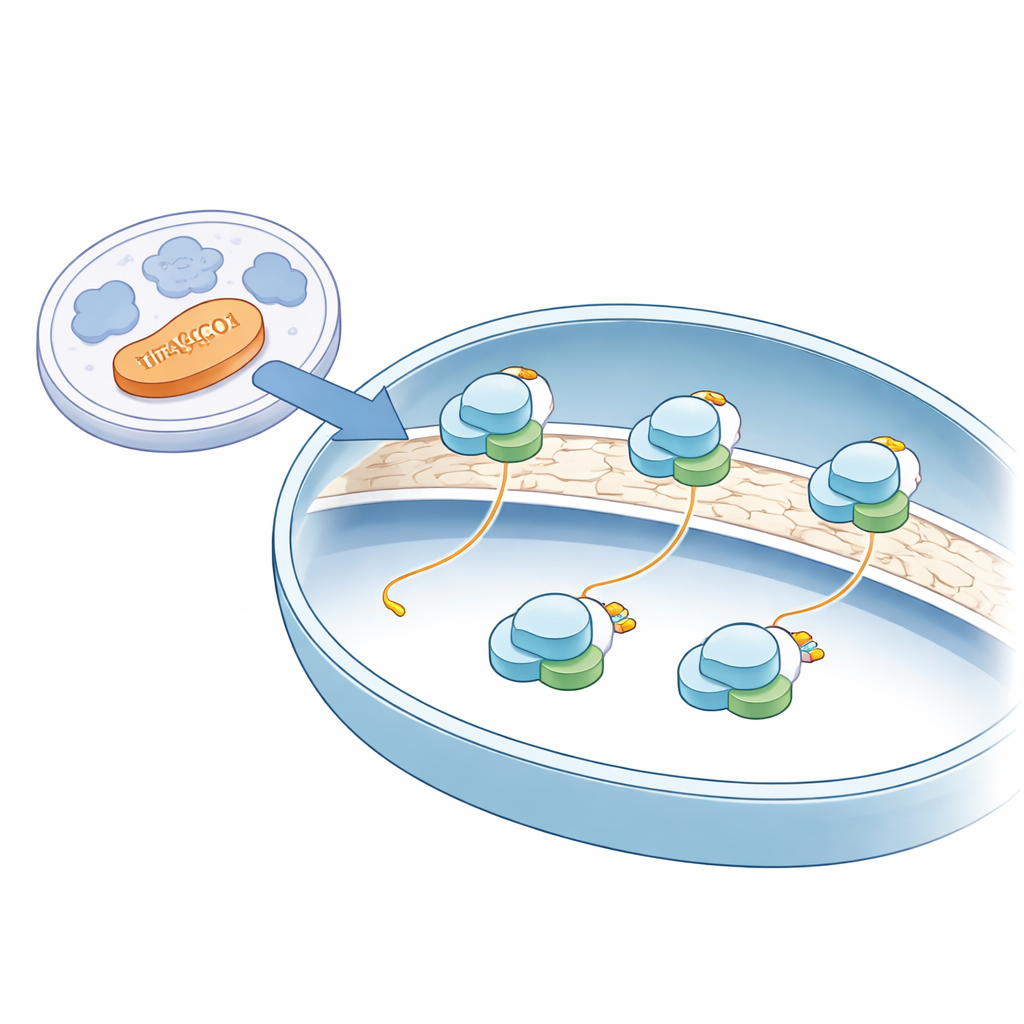
Un assistant caché se précise
Parmi les composants ribosomiques, les brins d’ARN et les chaînes protéiques en croissance, les chercheurs ont remarqué une zone de densité supplémentaire qui n’avait jamais été observée dans des préparations antérieures plus artificielles. En affinant soigneusement leurs cartes et en comparant les formes aux structures protéiques prédites, ils ont identifié ce constituant mystérieux comme étant TACO1, une protéine déjà liée aux maladies mitochondriales humaines mais dont le rôle physique restait obscur. Les images ont révélé que TACO1 se niche à côté de la partie du ribosome où arrive le prochain ARNt porteur d’acide aminé (le site A), établissant des contacts à la fois avec l’ARN ribosomique et plusieurs protéines ribosomiques. Ce positionnement permet à TACO1 d’agir presque comme un renfort, soutenant l’ARNt entrant pendant que le ribosome forme une nouvelle liaison pour allonger la chaîne protéique.
Éviter les embouteillages sur la chaîne d’assemblage protéique
La synthèse des protéines progresse selon un cycle : un facteur d’élongation (mtEF‑Tu) apporte un ARNt chargé, le ribosome le vérifie et l’utilise, puis le facteur part pour permettre l’étape suivante. Les auteurs ont découvert que TACO1 se lie à peu près dans la même région utilisée par mtEF‑Tu, et que les deux facteurs ne peuvent pas occuper le ribosome simultanément. Dans des cellules normales, de nombreux mitoribosomes apparaissaient dans un état où le nouvel ARNt est entièrement en place et l’élongation progresse. Lorsqu’ils ont examiné des mitochondries de cellules dépourvues de TACO1, ils ont observé une accumulation de ribosomes bloqués dans un état antérieur où mtEF‑Tu est encore attaché et le nouvel ARNt n’est pas totalement stabilisé. Des expériences biochimiques ont confirmé que, sans TACO1, mtEF‑Tu persiste plus longtemps sur les ribosomes en cours de traduction active, et les grandes et petites sous‑unités sont plus susceptibles de se dissocier — signes d’une traduction arrêtée ou défaillante. 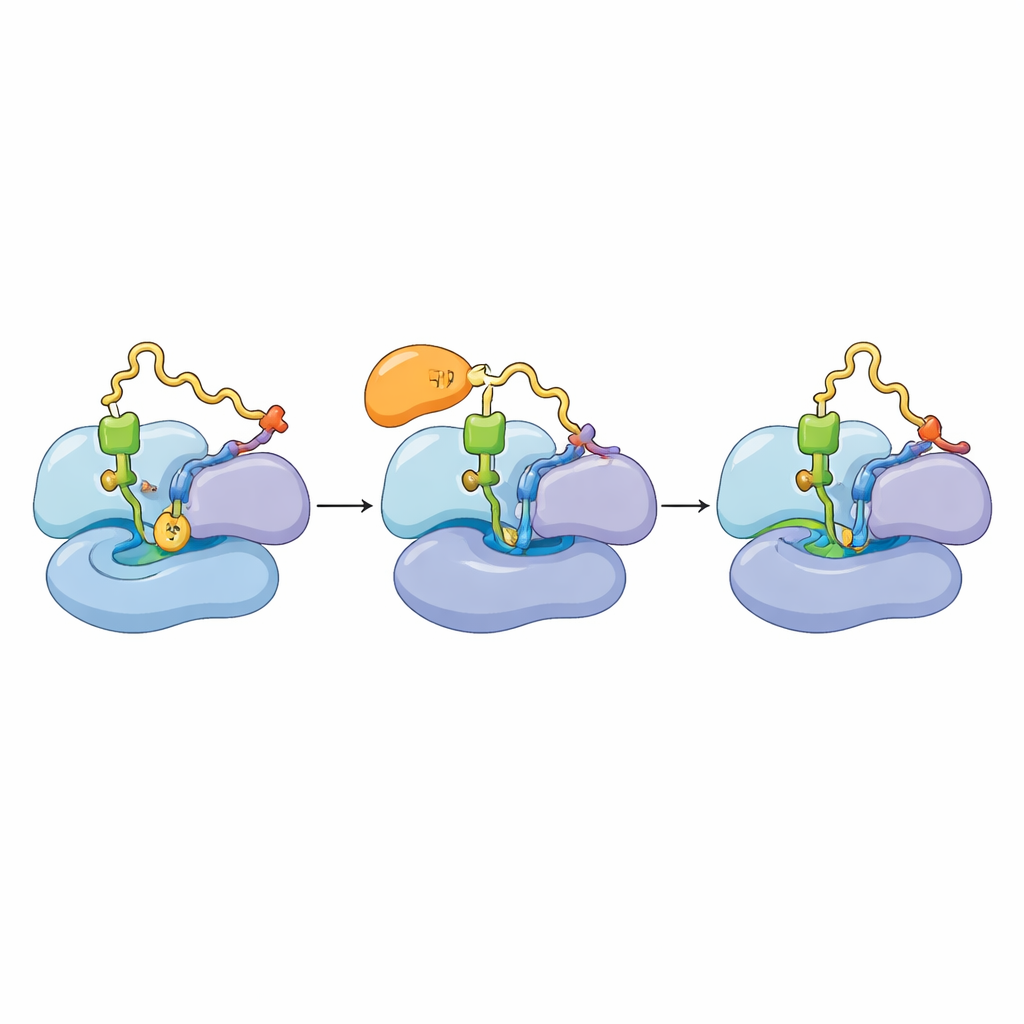
Pourquoi certains segments protéiques posent tant de problèmes
Une des fonctions majeures de TACO1 semble être d’aider le ribosome à franchir des séquences riches en proline, qui ralentissent naturellement la formation de liaisons en raison de la structure cyclique rigide de la proline. Des travaux antérieurs ont montré que TACO1 est crucial pour la production de la sous‑unité 1 de la cytochrome c oxydase, un composant central de la chaîne respiratoire qui contient un motif rare de triple proline, et que sa perte provoque l’effondrement de ce complexe énergétique et un trouble neurologique humain appelé syndrome de Leigh. Chez les bactéries et dans le principal système cytoplasmique de la cellule, d’autres facteurs auxiliaires remplissent une fonction anti‑blocage similaire, mais les mitochondries n’ont pas ces facteurs conventionnels. Ce nouvel apport structural montre que TACO1 a évolué comme une solution spécifique aux mitochondries : en écartant mtEF‑Tu, en stabilisant l’ARNt entrant et en soutenant la formation de la liaison, il aide le mitoribosome à dépasser ces segments de séquence difficiles au lieu de s’arrêter net.
Une stratégie ancienne aux implications contemporaines pour la santé
Au-delà des cellules humaines, des protéines apparentées à TACO1 se retrouvent chez de nombreuses bactéries et autres organismes, et certaines de ces versions bactériennes ont désormais été montrées elles aussi capables de soulager les blocages ribosomiques. Cette conservation suggère que l’utilisation d’un facteur de type TACO1 pour secourir des ribosomes lents ou coincés est une stratégie ancienne pour maintenir l’efficacité de la synthèse protéique. Pour l’homme, ces travaux fournissent une explication visuelle et concrète de la raison pour laquelle des mutations de TACO1 peuvent gravement compromettre la production d’énergie et le système nerveux, et laissent entrevoir que moduler TACO1 ou ses apparentés pourrait un jour permettre d’ajuster la traduction mitochondriale — soit pour traiter des maladies mitochondriales, soit pour cibler des bactéries nuisibles qui dépendent de systèmes de secours contre l’arrêt similaires.
Citation: Wang, S., Brischigliaro, M., Zhang, Y. et al. Structural basis of TACO1-mediated efficient mitochondrial translation. Nat Commun 17, 2521 (2026). https://doi.org/10.1038/s41467-026-69156-y
Mots-clés: traduction mitochondriale, TACO1, mitoribosome, arrêt du ribosome, syndrome de Leigh