Clear Sky Science · fr
Mécanisme moléculaire de l’importation de phosphate par le transporteur bactérien PstSCAB
Pourquoi les minuscules nutriments comptent pour nous
Chaque cellule vivante, des neurones humains aux bactéries du sol, fonctionne grâce au phosphore. Cet élément aide à stocker l’énergie, à construire l’ADN et à maintenir l’intégrité des membranes cellulaires. Pourtant, dans l’environnement, le phosphate assimilable — la forme de phosphore que les cellules peuvent réellement importer — est souvent rare. De nombreuses bactéries pathogènes dépendent d’une machine moléculaire ultra-efficace, nommée transporteur PstSCAB, pour récupérer le phosphate lorsque celui-ci se fait rare. Comprendre précisément le fonctionnement de cette machine n’est pas seulement une question de science fondamentale ; cela pourrait ouvrir des voies pour neutraliser des infections en privant les bactéries de ce nutriment vital.
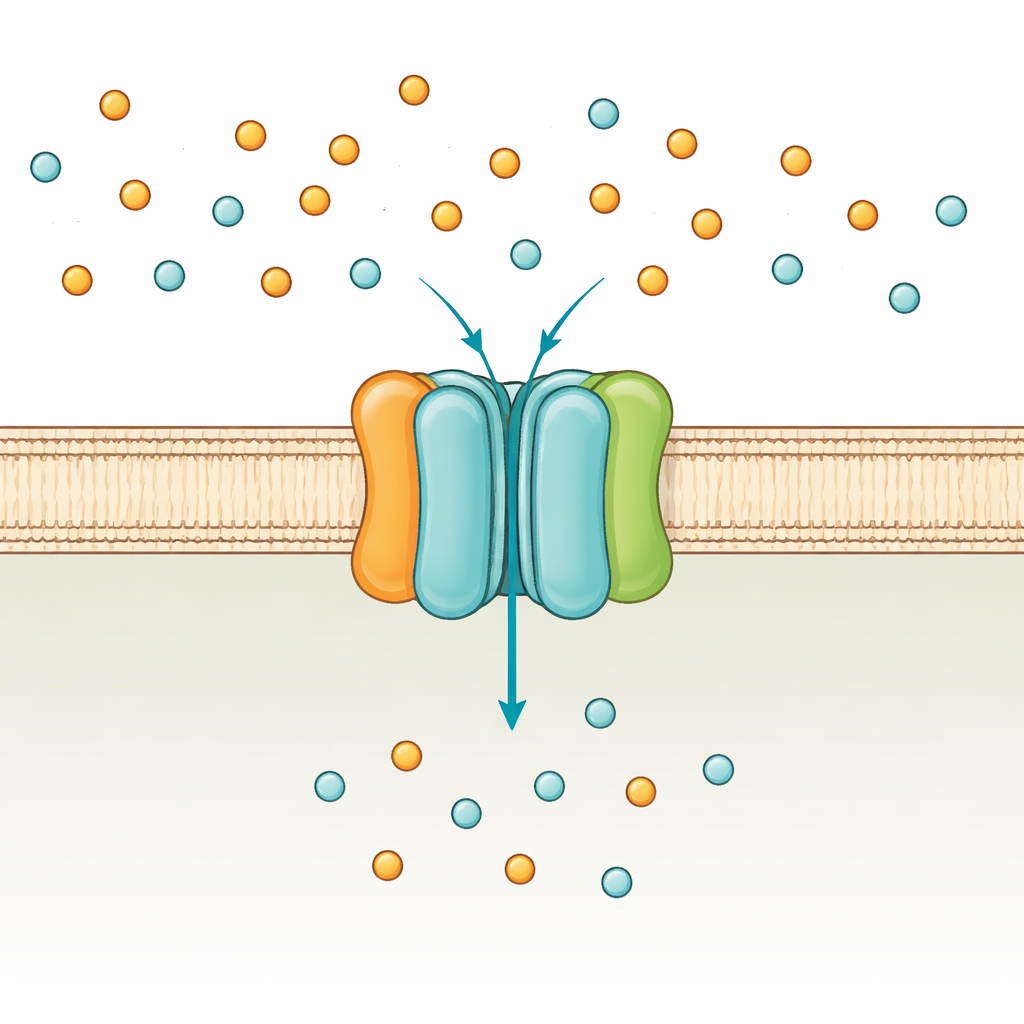
Le gardien du phosphate de la cellule
Des bactéries comme Escherichia coli utilisent deux voies principales pour absorber le phosphate : un système à faible affinité qui opère lorsque le phosphate est abondant, et le système à haute affinité PstSCAB qui s’active en cas de pénurie. PstSCAB est situé dans la membrane cellulaire et est alimenté par l’ATP, la monnaie énergétique universelle de la cellule. Il est composé de cinq éléments : deux sous-unités intégrées à la membrane (PstA et PstC) qui forment le passage, une protéine soluble « attrapeuse » située à l’extérieur de la membrane (PstS) qui saisit le phosphate, et une paire de sous-unités internes (PstB) qui consomment l’ATP pour propulser le transport. Parce que ce système participe aussi à la régulation de nombreux gènes liés à la virulence bactérienne, des mutations dans PstSCAB peuvent affaiblir des pathogènes responsables d’infections urinaires, de septicémies chez les animaux d’élevage et de tuberculose.
Capturer la machine en action
Jusqu’à présent, les scientifiques n’avaient que des vues partielles de PstSCAB, principalement de la seule protéine attrapeuse PstS. Dans cette étude, les chercheurs ont utilisé la cryo‑microscopie électronique à haute résolution pour visualiser l’ensemble du transporteur à plusieurs étapes clés de son cycle de fonctionnement. Ils ont reconstitué les protéines bactériennes dans des « nanodisques » membranaires artificiels et les ont congelées si rapidement que les molécules furent piégées en plein mouvement. En ajustant finement les protéines et en ajoutant ou en retirant l’ATP, ils ont obtenu des structures de trois états principaux : une forme de repos tournée vers l’intérieur sans la protéine attrapeuse attachée, un état pré‑translocation où PstS chargé de phosphate s’amarre au complexe membranaire, et un intermédiaire catalytique lié à l’ATP dans lequel le phosphate est retenu à l’intérieur du transporteur.
Comment les changements de forme déplacent le phosphate
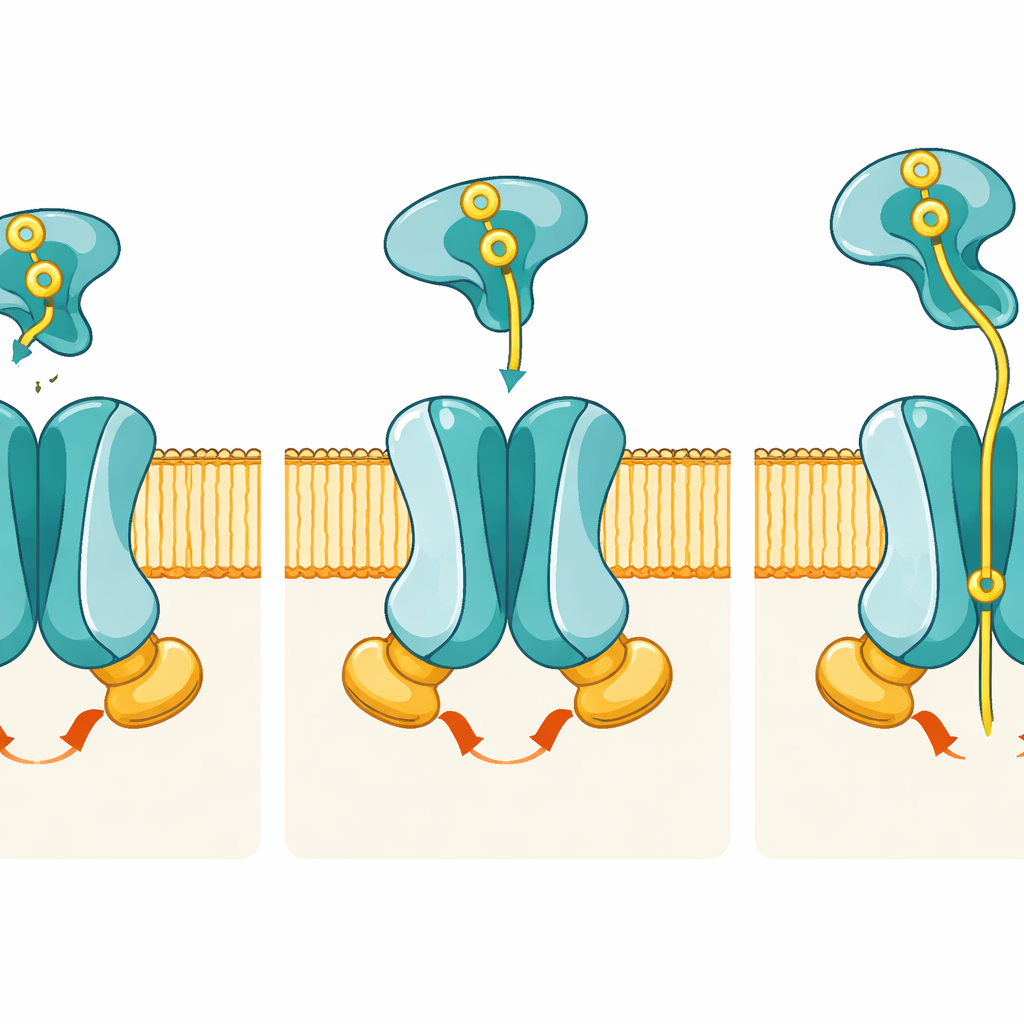
Les images révèlent comment des changements de conformation coordonnés déplacent le phosphate de l’extérieur vers l’intérieur de la cellule. À l’état de repos, le conduit formé par PstA et PstC n’est ouvert que vers l’intérieur de la cellule ; le côté extérieur est scellé par un ensemble de résidus « portiers », ce qui empêche l’entrée du phosphate depuis l’extérieur. Lorsque PstS chargé de phosphate s’amarre dans l’état pré‑translocation, il se loge entre des boucles flexibles de PstA et PstC mais, de manière frappante, les sous‑unités membranaires changent à peine de forme. Le véritable basculement survient lorsque PstS commence à ouvrir ses deux lobes pour relâcher le phosphate et, en coordination, les deux sous‑unités PstB se rapprochent pour fixer l’ATP. Cette fixation d’ATP clampant PstB en dimère tire sur des hélices de liaison dans PstA et PstC, retournant l’ensemble du pore en une conformation tournée vers l’extérieur qui expose une poche spécifique de liaison au phosphate vers l’extérieur.
Une poche sur mesure pour le phosphate
Dans la structure tournée vers l’extérieur et liée à l’ATP, les auteurs observent une densité au milieu de la région membranaire correspondant à un ion phosphate. Cet ion est soutenu par des acides aminés chargés positivement — en particulier deux arginines, l’une provenant de PstA et l’autre de PstC — qui jouent le rôle de « doigts » moléculaires saisissant le phosphate chargé négativement. Des simulations informatiques montrent que le phosphate reste solidement lié dans cette poche sur des microsecondes, et des expériences génétiques confirment son importance : lorsque ces résidus clés sont mutés, le transporteur hydrolyse toujours l’ATP mais importe très mal le phosphate. Cette séparation entre « où l’énergie est dépensée » et « où la cargaison est reconnue » met en lumière la précision avec laquelle la machine est réglée pour le phosphate.
Des instantanés structurels à la promesse médicale
Pris ensemble, les structures et les tests biochimiques de soutien décrivent un cycle complet : PstS capture le phosphate à l’extérieur, s’amarre au transporteur tourné vers l’intérieur, puis — couplé à la fixation et à la dégradation de l’ATP par PstB — déclenche un basculement qui place le phosphate dans la poche membranaire puis enfin dans l’intérieur cellulaire. Après l’hydrolyse de l’ATP, la machine revient à l’état de repos, prête pour un nouveau cycle. Pour un lecteur non spécialiste, le message clé est que nous disposons maintenant d’un plan à l’échelle atomique montrant comment de nombreuses bactéries survivent en environnements pauvres en phosphate et régulent leur virulence. Cette carte détaillée peut guider la conception de médicaments, d’anticorps ou de peptides qui bloquent le transporteur ou son protein attrapeur, transformant potentiellement cette porte d’entrée nutritionnelle essentielle en une cible thérapeutique vulnérable.
Citation: Xiao, H., Li, S., Qi, R. et al. Molecular mechanism of phosphate import by the bacterial PstSCAB transporter. Nat Commun 17, 2294 (2026). https://doi.org/10.1038/s41467-026-69153-1
Mots-clés: transport du phosphate, absorption des nutriments par les bactéries, transporteur ABC, PstSCAB, cibles antibactériennes