Clear Sky Science · fr
Perspectives moléculaires sur le transporteur de polysaccharides capsulaires Wza-Wzc
Comment les bactéries portent une armure invisible
Les bactéries pathogènes se protègent souvent par un manteau riche en sucres, ou capsule, qui les aide à échapper à notre système immunitaire et à résister à des conditions hostiles. Cette étude révèle, au niveau atomique, comment un élément clé de la machinerie chez des bactéries intestinales courantes assemble et exporte cette armure sucrée. Comprendre ce processus pourrait ouvrir la voie à de nouveaux antibiotiques et vaccins qui dépouillent les agents pathogènes de leur bouclier protecteur plutôt que d’essayer uniquement de les tuer.
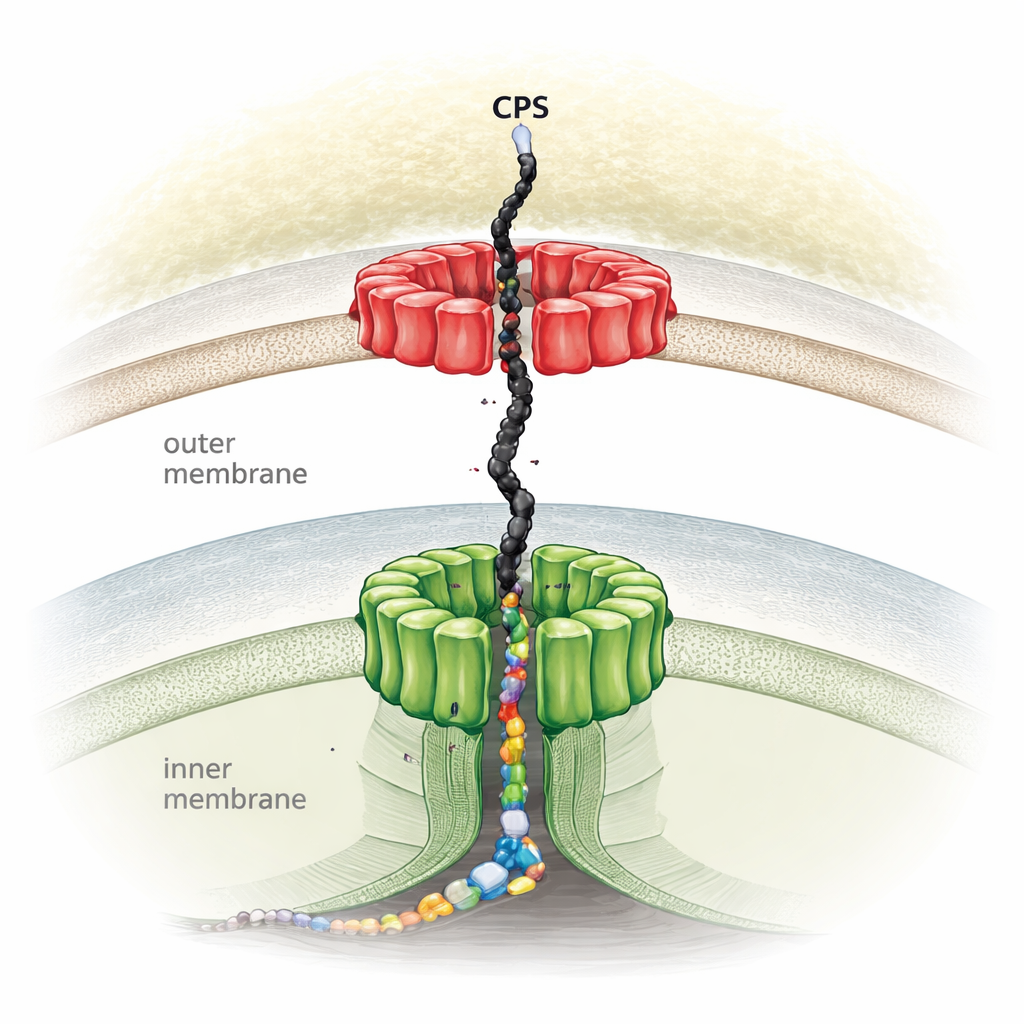
Le bouclier sucré des germes dangereux
De nombreuses bactéries nocives se couvrent de polysaccharides capsulaires — de longues chaînes ramifiées de sucres qui forment une couche externe épaisse. Cette capsule les aide à échapper aux attaques immunitaires, à résister aux antibiotiques et à former des biofilms résistants. Les travaux se concentrent sur Escherichia coli, un organisme modèle bien étudié qui utilise une voie répandue dite dépendante de Wzx/Wzy pour assembler ces chaînes de sucres. Dans cette voie, de petites unités répétées de sucres sont d’abord construites à l’intérieur de la cellule, basculées à travers la membrane interne, reliées entre elles en longs polymères, puis poussées vers l’extérieur pour former la capsule. Bien que les chercheurs connaissaient le nom des principaux acteurs protéiques, il manquait une image complète de la manière dont ils s’assemblent en une machine unique traversant l’ensemble de l’enveloppe bactérienne.
Révélation d’un tunnel moléculaire en pleine longueur
À l’aide de la cryo-microscopie électronique à haute résolution, les auteurs ont résolu la structure tridimensionnelle complète du complexe Wza-Wzc — la machinerie d’exportation centrale des sucres capsulaires chez E. coli K12. Ils ont découvert que huit copies de chaque protéine s’assemblent pour former un canal continu et haut qui s’étend de la membrane interne à la membrane externe, reliant l’espace périplasmique aqueux entre elles. Wza se loge dans la membrane externe sous la forme d’une bague rigide faisant office de sortie, tandis que Wzc forme une tour flexible ancrée dans la membrane interne. Ensemble, elles créent un tunnel d’environ 250–360 angströms de long, assez large pour guider un polymère de sucre volumineux et flexible depuis son site de synthèse à la membrane interne jusqu’à la surface cellulaire sans qu’il ne diffuse ni ne fuie. Des mutations aux points de contact clés entre Wza et Wzc ont complètement bloqué la production de capsule, confirmant que ce complexe conjoint est essentiel à l’exportation.
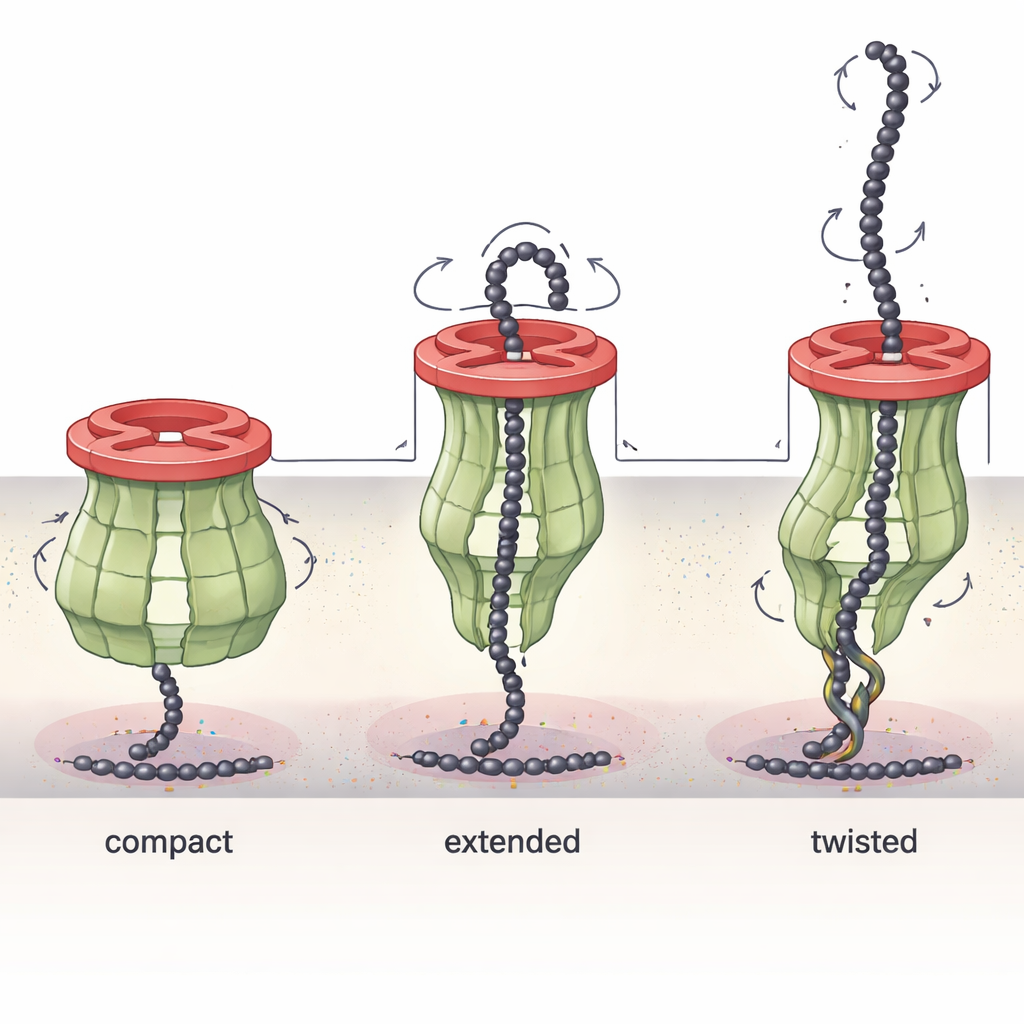
Un moteur changeant de forme qui extirpe les sucres
La partie Wzc du complexe s’est révélée remarquablement dynamique. En capturant plusieurs « instantanés » structuraux sous différentes conditions chimiques, les chercheurs ont montré que les longs bras périplasmiques de Wzc peuvent se plier, se tordre et s’allonger comme des leviers mécaniques. Dans un état, le canal est compact et hermétiquement fermé ; dans d’autres, Wzc a pivoté et s’est étiré, modifiant subtilement la largeur et la forme du tunnel. Dans certaines conformations, les bras obstruent partiellement le canal ou contactent Wza moins étroitement, et dans des cas extrêmes un seul anneau de Wzc peut engager deux anneaux de Wza simultanément. Ces observations soutiennent un modèle dans lequel Wzc agit un peu comme un palan moléculaire : ses mouvements de torsion et d’allongement aident à tirer la chaîne de sucre en croissance loin de la membrane interne et à l’alimenter dans le pore de la membrane externe, tout en coordonnant l’assemblage et le démontage de l’ensemble de la machine.
Une plate-forme d’atterrissage détectrice de sucres
Un autre mystère concernait la manière dont la machinerie reconnaît les bons blocs sucrés parmi les nombreux glucides présents dans et autour de la cellule. Wzc contient un domaine en « jellyroll » positionné juste au-dessus de la membrane interne dont le rôle était resté énigmatique. Des comparaisons structurelles avec des protéines connues pour lier des sucres, combinées à des tests biochimiques sur des séries de glucides purifiés, ont révélé que ce domaine peut reconnaître des motifs sucrés spécifiques semblables à ceux trouvés dans la capsule d’E. coli. La suppression de la région jellyroll réduisait fortement, mais n’abolissait pas totalement, la production de capsule, ce qui suggère qu’elle sert de plate-forme d’atterrissage capturant les unités de sucre récemment basculées et les guidant vers une plateforme de polymérisation formée par Wzc conjointement avec l’enzyme Wzy, qui assemble les unités en une longue chaîne.
Coordonner croissance, exportation et réinitialisation
Enfin, l’étude relie ces caractéristiques structurelles à un système de contrôle biochimique fondé sur la phosphorylation — l’ajout réversible de groupes phosphate à une queue riche en tyrosine sur Wzc. Lorsque Wzc est fortement phosphorylé, il existe principalement sous forme d’unités lâches et individuelles. À mesure que des phosphates sont retirés par une enzyme partenaire, les domaines kinase de Wzc s’assemblent en un octamère, réarrangeant ses bras pour qu’ils puissent engager Wza et entourer la polymérase Wzy. À mesure que la chaîne de capsule croît et est tirée à travers le tunnel, de nouvelles torsions et extensions de Wzc contribuent probablement à libérer le polymère fini dans Wza pour l’exportation. Une fois la sécrétion achevée, Wzc se re-phosphoryle, ce qui provoque la dissociation du complexe et réinitialise le système pour un nouveau cycle de production de capsule.
Pourquoi cela compte pour la lutte contre les infections
En termes simples, ce travail montre, presque boulon après boulon, comment les bactéries construisent une conduite moléculaire qui enfile de longues chaînes de sucres de l’intérieur vers l’extérieur de la cellule, où elles forment une cape protectrice. En cartographiant la structure et les mouvements du complexe Wza-Wzc, et en identifiant des éléments de reconnaissance des sucres et de contrôle, l’étude met en lumière plusieurs points faibles que de futurs médicaments ou vaccins pourraient cibler. Perturber cette machinerie d’exportation ne tuerait pas nécessairement les bactéries directement, mais pourrait les dépouiller de leur armure, les rendant bien plus vulnérables à nos défenses immunitaires et aux antibiotiques existants.
Citation: Yuan, B., Sieben, C., Raj, P. et al. Molecular insights into the capsular polysaccharide transporter Wza-Wzc complex. Nat Commun 17, 1436 (2026). https://doi.org/10.1038/s41467-026-69136-2
Mots-clés: capsule bactérienne, sécrétion de polysaccharides, complexe Wza-Wzc, structure cryo-EM, cibles antimicrobiennes