Clear Sky Science · fr
Thérapie bactérienne conçue supprimant Escherichia coli entérohémorragique par compétition métabolique et extinction de la virulence
Bactéries amicales comme médicament vivant
Les intoxications alimentaires causées par certaines souches d’Escherichia coli peuvent provoquer bien plus qu’un simple malaise d’estomac. Certaines souches dites entérohémorragiques d’E. coli (EHEC) libèrent des toxines puissantes susceptibles d’entraîner une insuffisance rénale, en particulier chez les enfants, et les antibiotiques classiques peuvent en réalité aggraver la situation. Cette étude explore un type de traitement différent : utiliser un probiotique modifié et un sucre présent dans le lait maternel, encapsulés dans des microcapsules intelligentes, pour évincer les bactéries dangereuses et mettre en sourdine leur comportement nocif sans perturber le reste de l’écosystème intestinal.
Pourquoi certaines E. coli sont si dangereuses
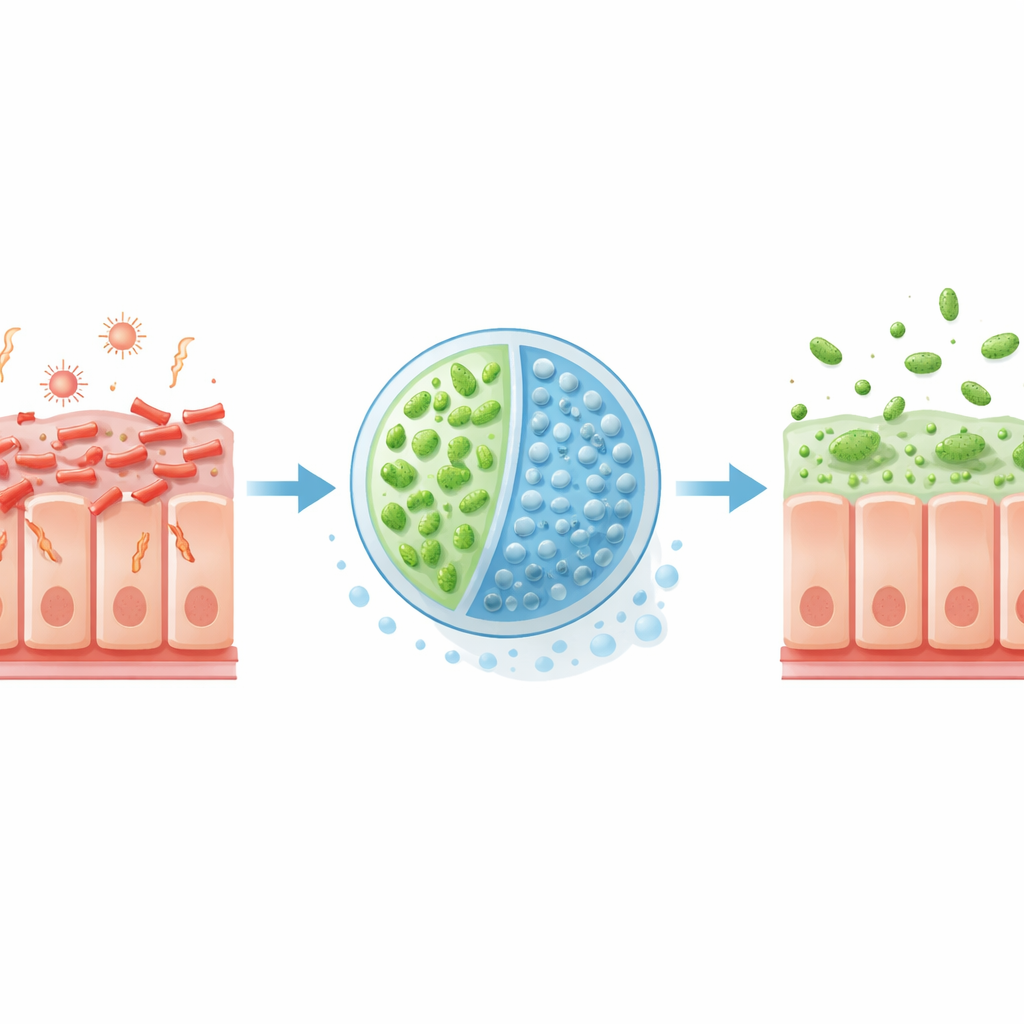
L’EHEC est un germe d’origine alimentaire que l’on contracte souvent via de la viande insuffisamment cuite ou des produits contaminés. Une fois dans l’intestin, il s’attache fermement aux cellules intestinales et injecte des protéines qui remodèlent la surface cellulaire, creusant des ancrages qui aident la bactérie à s’accrocher et à se propager. Parallèlement, l’EHEC produit des toxines de Shiga, qui peuvent pénétrer dans la circulation sanguine et endommager les vaisseaux, menant parfois à une affection potentiellement mortelle appelée syndrome hémolytique et urémique. Parce que de nombreux antibiotiques stressent ces bactéries et déclenchent encore plus de libération de toxines, les médecins disposent de peu d’options sûres au‑delà des soins de soutien, ce qui rend hautement souhaitables des approches nouvelles et ciblées.
Reprogrammer un probiotique pour affamer et désarmer l’EHEC
Les chercheurs se sont tournés vers Escherichia coli Nissle 1917, une souche probiotique utilisée de longue date, et l’ont reconfigurée en un microbe thérapeutique nommé EcN3. Ils ont doté EcN3 de gènes supplémentaires lui permettant de dégrader plus efficacement un acide sucre, l’acide glucuronique, que l’EHEC préfère comme source de nourriture dans le gros intestin. Ils ont aussi conféré à EcN3 une enzyme qui scinde le sucre du lait maternel 2′‑fucosyllactose en deux parties : lactose et fucose. Le lactose agit comme un « interrupteur » interne qui active le système amélioré d’utilisation des nutriments d’EcN3, l’aidant à capter l’acide glucuronique et à priver l’EHEC de ce carburant. Le fucose, quant à lui, sert de signal qui incite l’EHEC à réduire l’expression de gènes de virulence clés, diminuant sa capacité à former des adhérences fortes et à causer des dommages.
Capsules intelligentes qui libèrent la thérapie au bon endroit
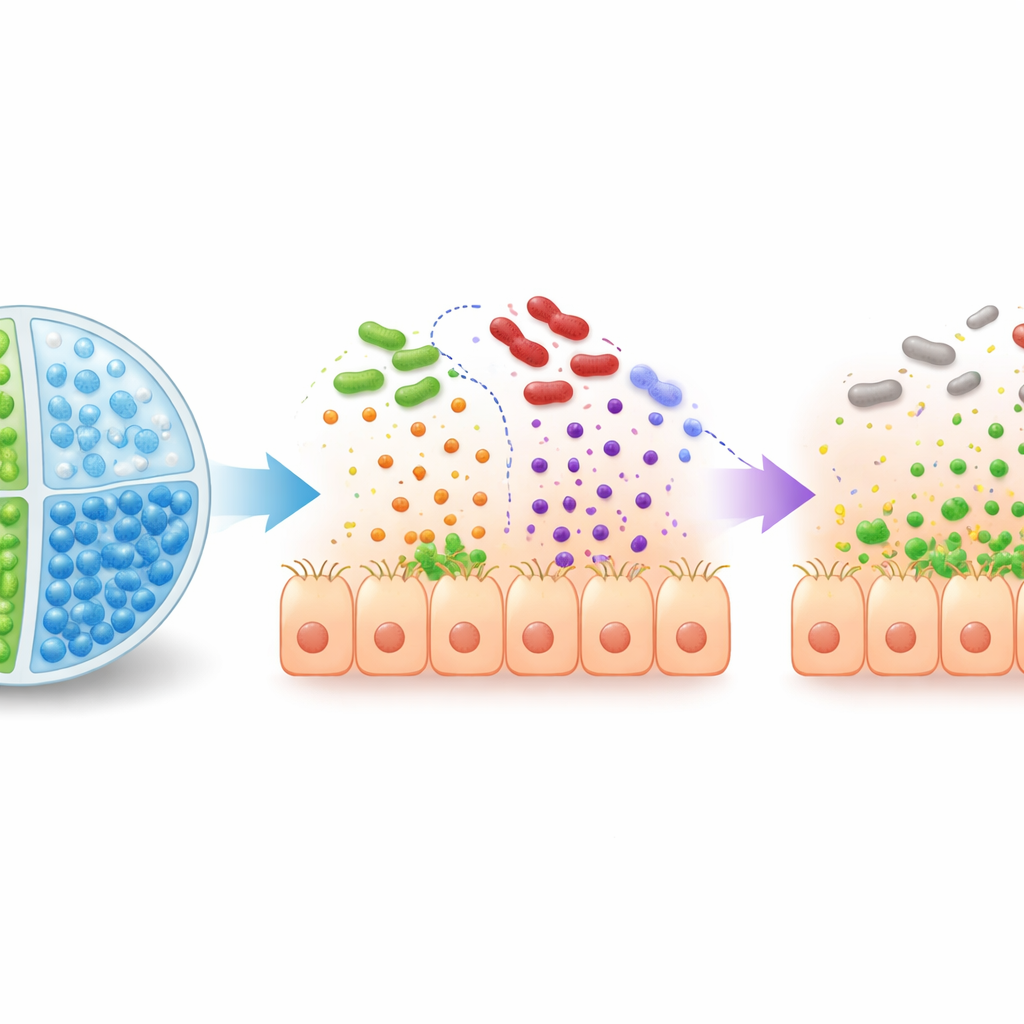
Administrer simplement des bactéries modifiées et du sucre dans l’intestin ne suffit pas : l’acide gastrique peut tuer le probiotique, et d’autres microbes risquent de consommer le sucre avant qu’il n’atteigne le côlon. Pour résoudre ce problème, l’équipe a construit des microsphères multicompartmentales — de minuscules billes en gel d’alginate avec deux chambres internes séparées. Une chambre contient EcN3 et l’autre contient le 2′‑fucosyllactose, les maintenant séparés jusqu’à ce que les billes atteignent le gros intestin. Ces microcapsules résistent à la dégradation dans un fluide simulant l’estomac mais se dissolvent dans des conditions semblables à celles du côlon, libérant à la fois la bactérie modifiée et le sucre précisément là où ils sont nécessaires. Chez la souris, le système encapsulé a permis une meilleure survie d’EcN3 et une activation plus forte de ses gènes modifiés que l’administration des mêmes composants sans capsules.
Tester la protection chez des modèles animaux
L’équipe a testé sa stratégie sur des lapins nouveau‑nés infectés par l’EHEC et sur des souris infectées par Citrobacter rodentium, un pathogène étroitement apparenté qui reproduit de nombreux aspects de la maladie humaine. Lorsqu’ils ont été traités après l’infection avec EcN3 plus 2′‑fucosyllactose, les animaux présentaient moins de pathogènes dans l’intestin, une expression réduite des gènes d’adhésion des bactéries et moins de lésions tissulaires intestinales — le tout sans augmentation de la production de la toxine de Shiga. En prévention, la combinaison libre (non encapsulée) fonctionnait mal car le sucre était rapidement consommé par le microbiote existant. En revanche, lorsque EcN3 et le 2′‑fucosyllactose ont été délivrés ensemble dans des microsphères à double compartiment, tant les lapins que les souris ont montré une colonisation pathogène fortement réduite, une maladie plus légère et une meilleure survie.
Aider les bonnes bactéries et la barrière intestinale à récupérer
En utilisant le séquençage de l’ADN pour profiler le microbiote intestinal, les scientifiques ont constaté que l’infection perturbait l’équilibre microbien normal, augmentant Citrobacter nuisible tout en affaiblissant des groupes bénéfiques. Le traitement par microcapsules modifiées a non seulement réduit les niveaux de pathogènes mais aussi restauré la communauté vers un état plus sain, augmentant en particulier les espèces de Lactobacillus connues pour soutenir la santé intestinale. Les mesures de la fonction de la barrière intestinale racontent une histoire similaire : les animaux ayant reçu la thérapie encapsulée présentaient une expression plus élevée de gènes liés au mucus et aux jonctions serrées, des couches de mucus protectrices plus épaisses et moins de fuite d’un traceur fluorescent de l’intestin vers la circulation sanguine, indiquant des parois intestinales plus étanches et moins enflammées.
Un aperçu des futurs soins des infections sans antibiotiques
Globalement, ce travail démontre une stratégie ciblée et à deux volets contre une infection alimentaire notoirement difficile à traiter. En combinant un probiotique modifié qui concurrence pour la nourriture et détecte un signal sucré bénin avec des microcapsules qui délivrent les deux composants au côlon, la thérapie affaiblit l’EHEC, réduit ses effectifs et protège l’intestin sans recourir aux antibiotiques traditionnels. Bien que des études de sécurité et des essais cliniques supplémentaires soient nécessaires, l’approche illustre comment des médicaments vivants et des matériaux intelligents pourraient un jour offrir des moyens précis et compatibles avec le microbiome pour gérer des infections intestinales sévères et réduire la dépendance aux médicaments conventionnels.
Citation: Ma, G., Liu, R., Li, X. et al. Engineered bacterial therapy suppresses Enterohemorrhagic Escherichia coli through metabolic competition and virulence silencing. Nat Commun 17, 2307 (2026). https://doi.org/10.1038/s41467-026-69126-4
Mots-clés: probiotiques modifiés, thérapie des infections intestinales, EHEC, microbiote, microsphères pour délivrance de médicaments