Clear Sky Science · fr
Un dopant chrome dynamique favorise l’activation de l’eau interfaciale sur l’oxyde de spinelle de cobalt pour une évolution de l’oxygène efficace en milieu acide
Pourquoi cette recherche compte pour l’énergie propre
Produire de l’hydrogène à partir de l’eau pourrait alimenter l’industrie et les transports sans émissions de carbone, mais les dispositifs les plus efficaces aujourd’hui dépendent de métaux précieux rares et coûteux. Cette étude examine comment un matériau peu coûteux et conçu avec soin, à base de cobalt et de chrome, peut remplacer ces métaux dans l’un des aspects les plus difficiles du fractionnement de l’eau : la formation d’oxygène en conditions acides, telles qu’utilisées dans les électrolyseurs à membrane échangeuse de protons commerciaux (PEMWE). 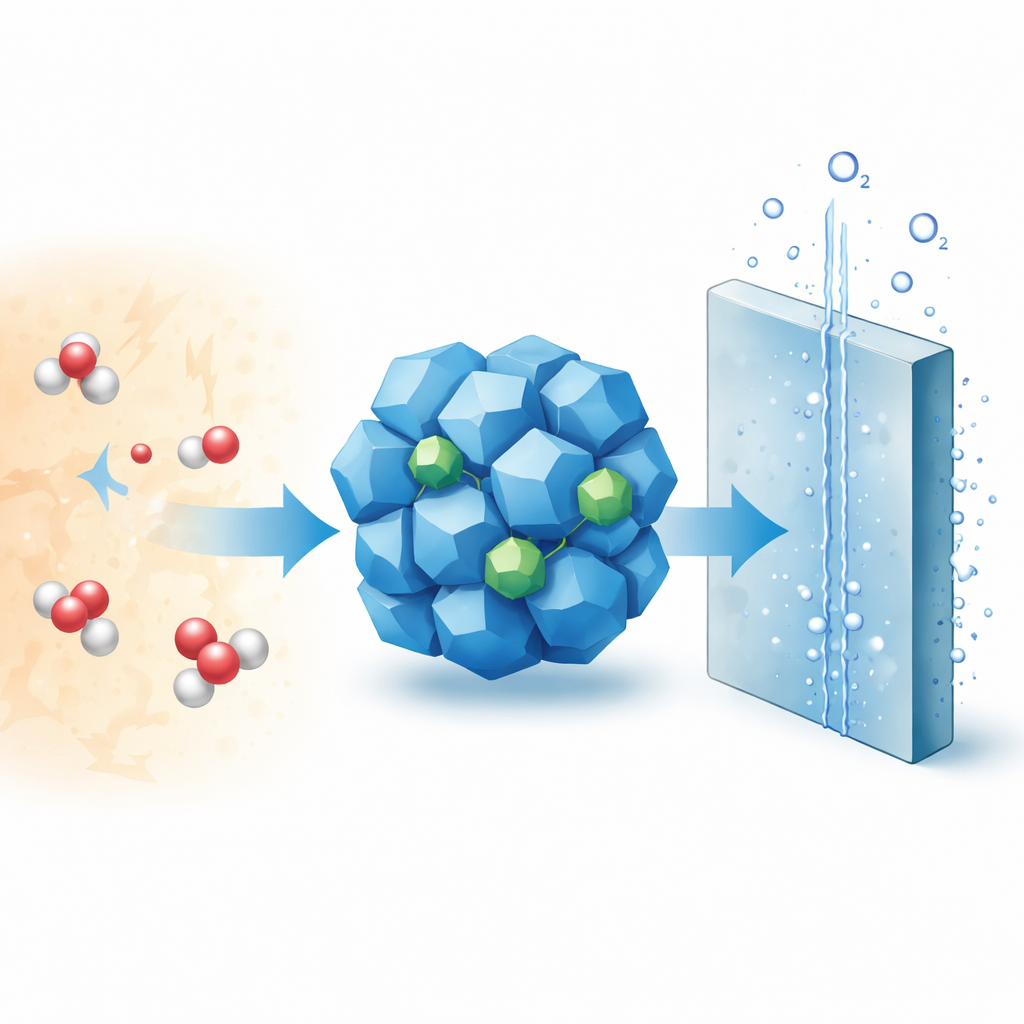
Le défi de produire de l’oxygène à partir de l’eau
Les PEMWE modernes sont attrayants car ils peuvent convertir rapidement l’électricité solaire ou éolienne en hydrogène, même lorsque l’apport d’énergie fluctue. Cependant, du côté production d’oxygène de ces dispositifs, la réaction est lente et sévère. Elle se déroule en milieu acide et implique le transfert étroitement couplé de protons et d’électrons. Aujourd’hui, cette étape est généralement assurée par des catalyseurs à base d’oxydes d’iridium et de ruthénium — des métaux rares et onéreux. L’oxyde de cobalt (Co3O4) est apparu comme une alternative prometteuse, mais en milieu acide il a tendance à corroder : les atomes de cobalt se dissolvent dans le liquide, la surface se sur‑oxyde en formes instables et le catalyseur se désagrège progressivement.
Un ajustement intelligent : ajout d’atomes de chrome
Les auteurs montrent qu’introduire une petite quantité de chrome dans l’oxyde de spinelle de cobalt modifie à la fois la structure électronique interne du solide et la mince couche d’eau à sa surface. Ils synthétisent de petites nanoparticules uniformes d’oxyde de cobalt dopé au chrome (Cr‑Co3O4) et confirment, par diffraction et microscopie électronique, que le matériau conserve la structure spinelle d’origine. Des techniques spectroscopiques avancées révèlent que les atomes de chrome s’insèrent dans des positions tétraédriques spécifiques du réseau et sont dispersés en atomes isolés plutôt qu’en particules d’oxyde de chrome séparées. Ce positionnement crée un environnement local chrome‑oxygène‑cobalt qui abaisse légèrement la charge moyenne des atomes de cobalt, les rendant moins susceptibles à la sur‑oxydation.
Meilleure performance en conditions acides sévères
Testé en acide sulfurique, le catalyseur dopé au chrome nécessite beaucoup moins de surtension que l’oxyde de cobalt non dopé pour atteindre le même courant, ce qui indique qu’il accélère la production d’oxygène. Il surpasse également les oxydes commerciaux de ruthénium et d’iridium à densités de courant élevées et, ce qui est crucial, maintient son activité pendant au moins 160 heures, tandis que les autres catalyseurs se dégradent. Les mesures électriques montrent que le transfert de charge à l’interface entre le catalyseur dopé et le liquide est plus facile. Intégré dans un dispositif complet d’électrolyse PEM, le Cr‑Co3O4 utilisé côté oxygène, associé à un catalyseur standard au platine côté hydrogène, fonctionne de manière stable pendant plus de 750 heures à un courant pertinent pour l’industrie, démontrant une durabilité pratique.
Comment le chrome reconfigure la couche d’eau
Pour aller au‑delà des simples chiffres de performance, les chercheurs sondent l’évolution de la surface du catalyseur et des molécules d’eau voisines pendant le fonctionnement. Des mesures in situ aux rayons X et en Raman montrent que dans l’oxyde de cobalt pur, les atomes de cobalt deviennent fortement sur‑oxydés à haut potentiel, précurseur d’une dégradation structurelle. Dans le matériau dopé, en revanche, l’état d’oxydation du cobalt reste presque constant tandis que le chrome évolue progressivement, indiquant que le chrome sert de « tampon » d’électrons protégeant le cobalt. Des mesures sensibles à la surface révèlent en outre que, sous potentiel de fonctionnement, les atomes de chrome lient de plus en plus des groupes hydroxyle (OH). Ces hydroxyles de surface modifient la structure de la couche d’eau en contact avec l’électrode : la spectroscopie infrarouge montre que les réseaux de liaisons hydrogène s’affaiblissent et que la fraction de molécules d’eau plus mobiles, dites « libres », augmente. Comme ces molécules d’eau se dissocient plus facilement, la réaction qui transforme l’eau en oxygène s’accélère. 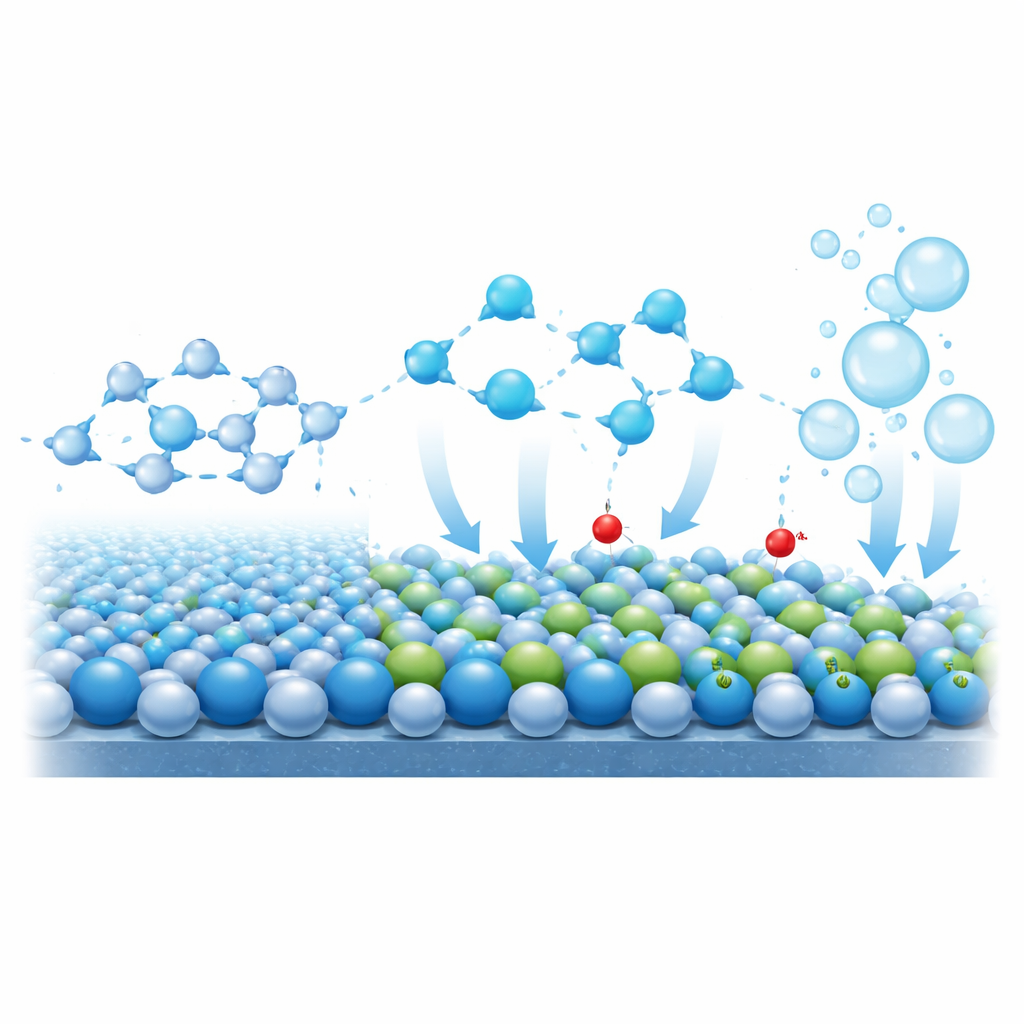
Relier théorie et expérience
Des simulations informatiques étayent ce tableau. Les calculs montrent que le chrome préfère les mêmes sites du réseau identifiés expérimentalement et a tendance à donner de la densité électronique vers le cobalt voisin. L’énergie requise pour cliver une molécule d’eau à la surface dopée est plus faible que sur l’oxyde de cobalt pur, en particulier lorsqu’un hydroxyle est déjà présent sur le site de chrome, ce qui reflète la constatation expérimentale que les surfaces riches en hydroxyles sont plus actives. Les simulations indiquent également qu’extraire un atome de cobalt de la surface dopée demande plus d’énergie, expliquant la meilleure résistance à la dissolution. Les diagrammes énergétiques globaux de la réaction confirment que l’étape la plus difficile de la séquence de formation d’oxygène devient plus simple une fois le chrome introduit.
Ce que cela signifie pour les futurs dispositifs de fractionnement de l’eau
Dans l’ensemble, ces résultats montrent qu’une petite quantité du bon dopant peut modifier de façon spectaculaire le comportement à la surface d’un catalyseur, tant des électrons que des molécules d’eau. En utilisant le chrome pour stabiliser le cobalt et favoriser une couche d’eau facilement activable et faiblement liée, l’équipe crée un catalyseur robuste, sans métal précieux, qui rivalise avec les oxydes de métaux nobles en conditions acides exigeantes. Pour le lecteur non spécialiste, l’essentiel est que l’ingénierie atomique intelligente — quelques atomes de chrome bien placés — peut permettre à des matériaux abordables d’accomplir le travail difficile de scinder l’eau, rapprochant la production d’hydrogène vert à grande échelle d’une application pratique.
Citation: Wu, L., Zhao, B., Huang, W. et al. Dynamic chromium dopant promotes interfacial water activation on cobalt spinel oxide for efficient oxygen evolution in acid. Nat Commun 17, 2598 (2026). https://doi.org/10.1038/s41467-026-69124-6
Mots-clés: hydrogène vert, électrolyse de l’eau, réaction d’évolution de l’oxygène, catalyseur à base d’oxyde de cobalt, eau interfaciale