Clear Sky Science · fr
Un phosphaalumène(3) isolable capable d’activer de petites molécules via des modes de réactivité uniques
Briser des liaisons robustes avec un nouvel outil chimique
Les chimistes recherchent sans cesse des moyens de convaincre des molécules récalcitrantes de réagir. De nombreuses substances courantes, du dihydrogène au dioxyde de carbone, sont remarquablement stables, ce qui rend leur transformation difficile. Cet article décrit une molécule nouvellement conçue, à base d’aluminium et de phosphore, capable de se lier à ces partenaires réticents et de rompre leurs liaisons. Comprendre et contrôler ce type d’activation de liaison pourrait un jour aider à convertir des gaz‑résidus en matières premières, ou offrir des voies plus douces et économes en métaux pour fabriquer des produits fins et des matériaux.
Une liaison sur mesure entre aluminium et phosphore
Au cœur de l’étude se trouve un type rare de connexion entre deux éléments des groupes principaux : l’aluminium et le phosphore. Les chercheurs ont synthétisé une molécule, appelée « 3 » dans l’article, dans laquelle ces deux atomes partagent une liaison double serrée. Pour empêcher ce couple réactif de se décomposer, ils l’ont entouré d’un cadre organique encombrant qui le protège des réactions accidentelles. Par deux voies synthétiques différentes, ils ont obtenu ce complexe sous forme isolable et ont fait croître des cristaux simples adaptés à la diffraction aux rayons X, confirmant que le phosphore est lié à l’aluminium par une liaison courte de type double, tandis que chaque atome est soutenu par des ligands azotés environnants. Des calculs ont montré que les électrons sont inégalement partagés entre l’aluminium et le phosphore, rendant la liaison polarisée et prête à être attaquée par d’autres molécules.
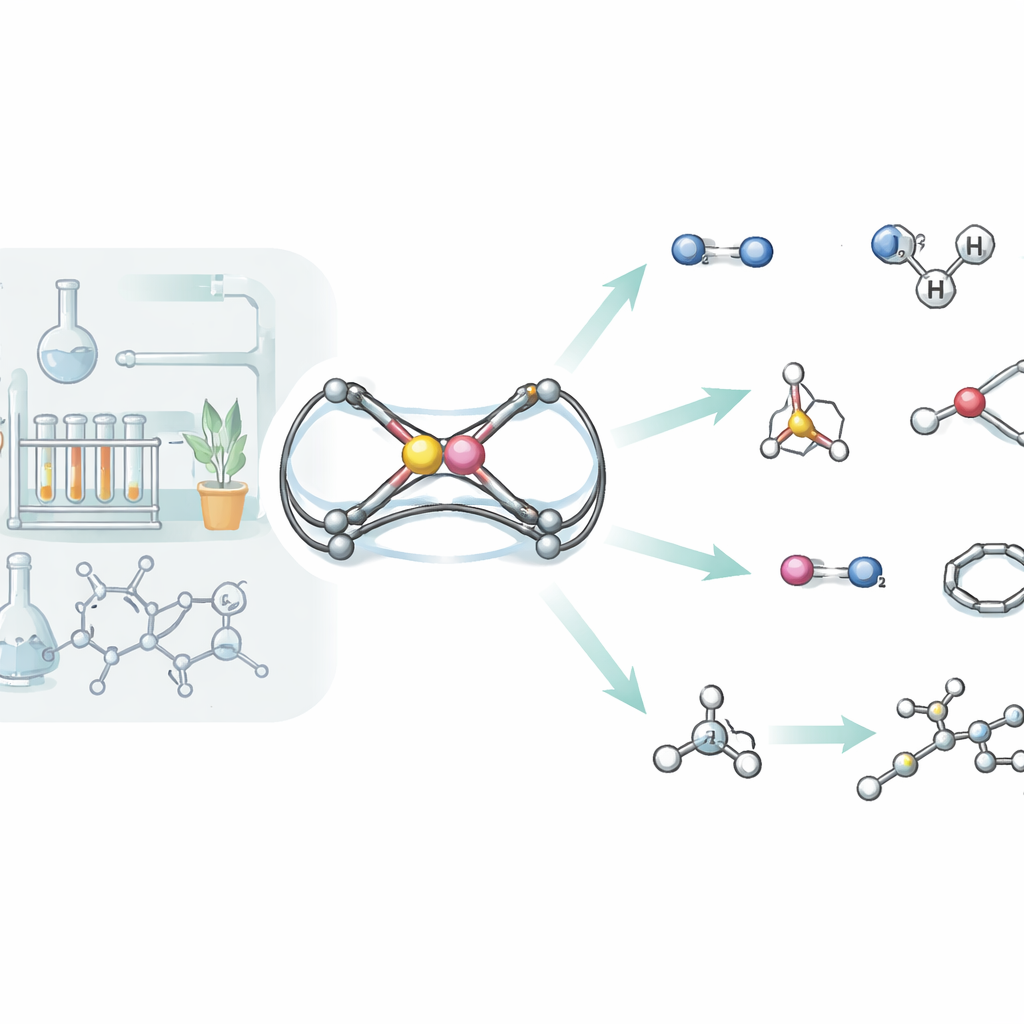
Comment la nouvelle molécule traite le dihydrogène
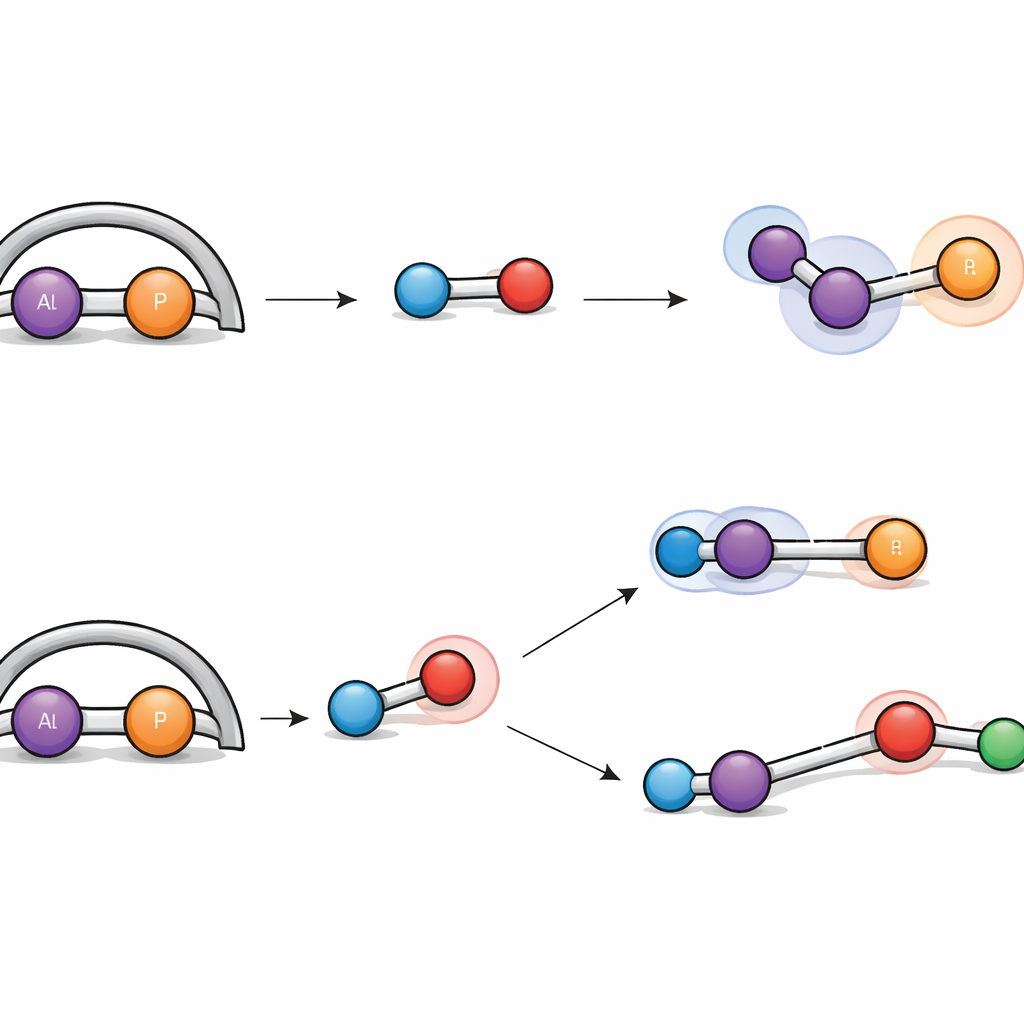
Le dihydrogène est notoirement difficile à scinder sans métaux précieux, et pourtant l’unité aluminium‑phosphore parvient à le faire. Exposé à l’hydrogène dans des conditions douces, le complexe réagit selon deux voies distinctes. Dans une voie, la liaison H–H s’additionne simplement sur la liaison double aluminium–phosphore, la transformant en deux liaisons simples et fixant un atome d’hydrogène sur chaque atome. Dans l’autre, la molécule d’hydrogène est dissociée de manière coopérative par l’aluminium et un atome d’azote voisin, un comportement rappelant les « paires acide‑base frustrées » qui activent l’hydrogène sans catalyseurs métalliques classiques. Des simulations détaillées ont retracé les deux voies, montrant que leurs barrières énergétiques sont similaires, ce qui explique pourquoi les deux produits se forment côte à côte.
Démonter une galerie de petites molécules
L’hydrogène n’est que le début. L’équipe a testé systématiquement la réactivité de leur échafaudage aluminium‑phosphore envers un large éventail de petites molécules, incluant le phosphore blanc, les isocyanures, le dioxyde de carbone, l’oxyde d’azote, l’azide de triméthylsilyle, les dimères de sélénium, les silanes, les amines, le styrène et des alcynes simples. Dans nombre de ces réactions, la liaison Al=P d’origine est complètement rompue, les deux atomes se retrouvant incorporés dans des structures cage ou en anneau plus grandes qui incluent des fragments de la molécule entrante. Par exemple, le phosphore blanc (P4) est ouvert puis reconstruit en une cage aluminium‑phosphore, tandis que le dioxyde de carbone s’insère à deux reprises pour former un cycle à six membres reliant l’aluminium et le phosphore par deux nouvelles liaisons carbone‑oxygène. Avec les silanes et les amines, la molécule se comporte plutôt comme une double liaison classique : l’unité Si–H ou N–H entrante s’additionne proprement sur Al=P, démontrant à nouveau le caractère « π » de cette liaison inhabituelle.
Pourquoi l’architecture environnante est importante
Une des leçons clés de ce travail est que le cadre volumineux et riche en azote autour de l’unité Al=P n’est pas qu’un simple échafaudage : il oriente la manière et le lieu où les réactions ont lieu. En comparant leurs résultats avec des systèmes aluminium‑phosphore antérieurs, plus instables, les auteurs montrent que de petits changements dans les ligands de soutien inversent l’équilibre entre différentes voies, comme l’addition simple sur la double liaison versus des ruptures de liaison plus élaborées et la formation d’anneaux. Des analyses sophistiquées de la distribution électronique ont révélé une forte polarisation de la liaison Al=P et mis en évidence comment les atomes d’azote voisins peuvent coopérer avec l’aluminium, en particulier lors de l’activation de l’hydrogène. L’encombrement stérique — la mise en concurrence spatiale de grands groupes — oriente également les molécules entrantes vers un site réactif ou un autre.
Ce que cela signifie pour la chimie future
Pour un non‑spécialiste, la liste de réactifs de cette étude peut sembler lointaine, mais le message sous‑jacent est clair : en réglant finement à la fois la liaison et la forme autour d’éléments des groupes principaux, les chimistes peuvent concevoir des outils agiles qui rivalisent avec ou complètent les catalyseurs métalliques traditionnels. Ce complexe aluminium‑phosphore isolable non seulement se conserve en bouteille, mais s’attaque aussi à un large éventail de petites molécules difficiles dans des conditions douces, scindant l’hydrogène, réarrangeant le phosphore blanc et capturant le dioxyde de carbone. L’étude montre que des modifications subtiles de la « poignée » d’une molécule peuvent rediriger profondément sa réactivité, offrant un plan pour concevoir des catalyseurs futurs capables de convertir des molécules simples et stables en produits plus précieux avec précision et efficacité.
Citation: Cha, Y., Yang, Z., Zhuang, X. et al. An isolable phosphaalumene(3) capable of small molecule activation via unique modes of reactivity. Nat Commun 17, 2390 (2026). https://doi.org/10.1038/s41467-026-69118-4
Mots-clés: activation de petites molécules, chimie des éléments principaux, liaison double aluminium‑phosphore, paire acide‑base frustrée, mécanismes d’activation de liaisons