Clear Sky Science · fr
Mécanisme d’inhibition des β−1,3-glucanes synthases fongiques par des antifongiques triterpénoïdes
Pourquoi il est crucial d’arrêter les infections fongiques
Les infections fongiques tuent discrètement plus d’un million de personnes chaque année et menacent les cultures et les écosystèmes à l’échelle mondiale. Les médecins disposent déjà d’une liste restreinte d’antifongiques, et certains champignons dangereux évoluent pour leur échapper. Cette étude révèle, au niveau moléculaire, comment une nouvelle classe d’antifongiques se fixe et désactive une enzyme clé que les champignons utilisent pour construire leur paroi protectrice. Comprendre ce processus offre une feuille de route pour concevoir de meilleurs traitements capables de déjouer les champignons résistants.
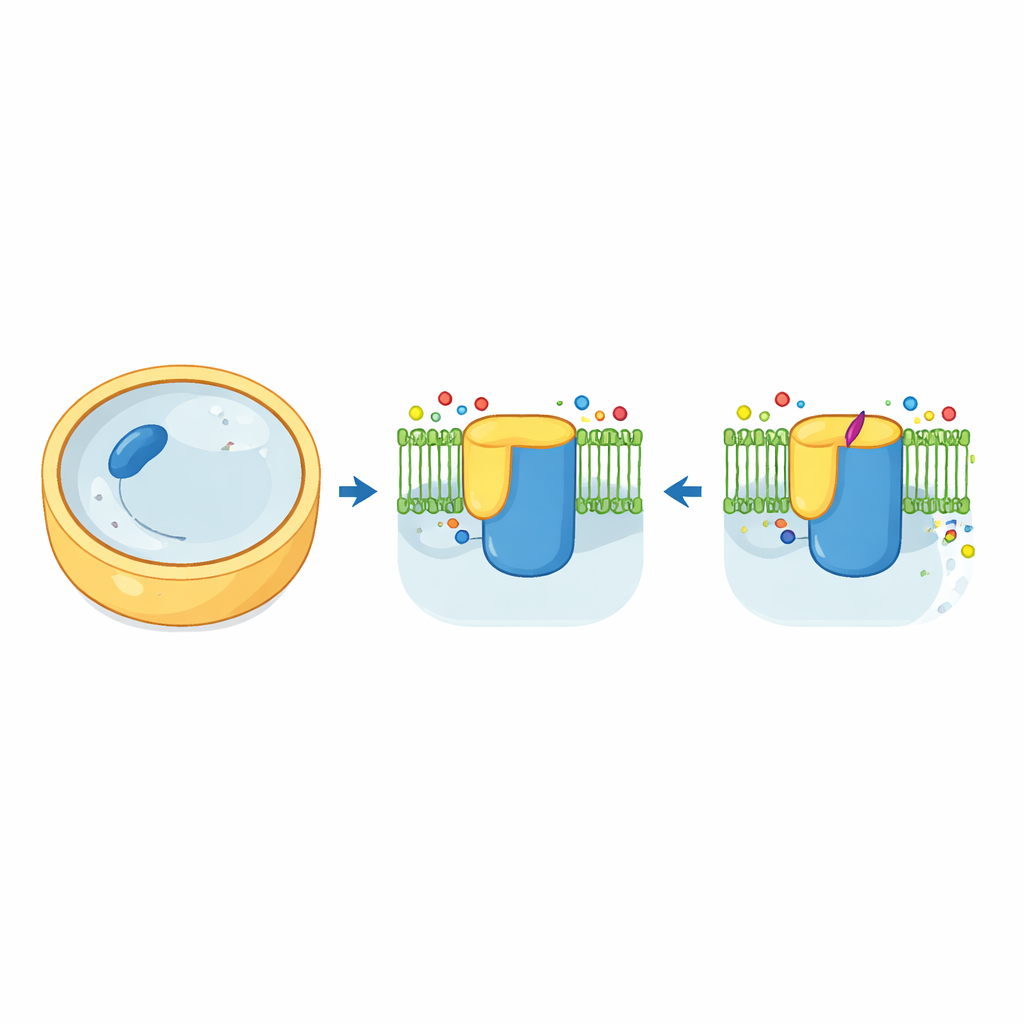
Le fabricant de briques de la paroi fongique
Les cellules fongiques sont entourées d’une paroi résistante composée en grande partie d’un polymère glucidique appelé bêta-1,3-glucane. L’enzyme qui synthétise et exporte ce polymère, connue sous le nom de bêta-1,3-glucane synthase, fonctionne comme un fabricant de briques couplé à un tapis roulant. Chez la levure de boulanger, cette machinerie est constituée de deux versions très similaires, Fks1 et Fks2, chacune intégrée dans la membrane cellulaire et contrôlée par une petite protéine auxiliaire nommée Rho1. À l’aide de la cryo-microscopie électronique, les auteurs ont capturé des vues tridimensionnelles haute résolution de Fks1 et Fks2 dans leur forme native. Les structures révèlent un vaste « établi » cytosolique relié à une forêt d’hélices traversant la membrane, avec une cavité centrale qui sert vraisemblablement de tunnel par lequel la chaîne de glucane en croissance sort de la cellule.
Comment un produit naturel saisit l’enzyme
Les triterpénoïdes d’intérêt clinique, y compris le médicament oral ibrexafungerp, tirent leurs origines d’un composé naturel nommé enfumafungine. Jusqu’à présent, personne ne savait précisément où ces drogues se lient sur la glucane synthase. Les chercheurs ont résolu les structures de Fks1 et Fks2 liés à l’enfumafungine. De manière surprenante, le médicament ne s’insère pas dans le site actif où les unités de sucre sont liées entre elles. À la place, il se loge sur la portion externe d’une seule hélice membranaire appelée TM5, se trouvant dans la membrane à environ trois nanomètres du centre catalytique et près du probable canal de sortie du glucane. Des acides aminés clés de cette région embrassent le cœur hydrophobe du médicament et contactent sa queue acide, tandis que son appendice sucre effleure à peine la protéine — ce qui explique pourquoi les chimistes ont pu modifier cette partie sans perdre en puissance.
Des médicaments qui figent une machine en mouvement
À première vue, la conformation globale de l’enzyme avec ou sans enfumafungine paraît presque inchangée. La différence cruciale réside dans l’organisation des lipides environnants et la flexibilité de certaines hélices. Lorsque le médicament se lie, une chaîne latérale aromatique proche pivote pour serrer l’enfumafungine en place et, avec un autre résidu, stabilise un lipide ordonné à côté du médicament. Des lipides supplémentaires de type stérol deviennent soigneusement arrangés autour d’un ensemble d’hélices horizontales qui contribuent à définir le trajet d’exportation du glucane. Ces lipides agissent comme des cales et des supports, bloquant les hélices et l’entrée du canal dans une configuration « basale » particulière. Des tests génétiques montrent que modifier de nombreux points de contact pour le médicament ou ces stérols affaiblit la liaison du médicament ou détruit la fonction de l’enzyme, et des mutations à ces sites correspondent à des mutations de résistance connues chez des agents pathogènes humains et végétaux.
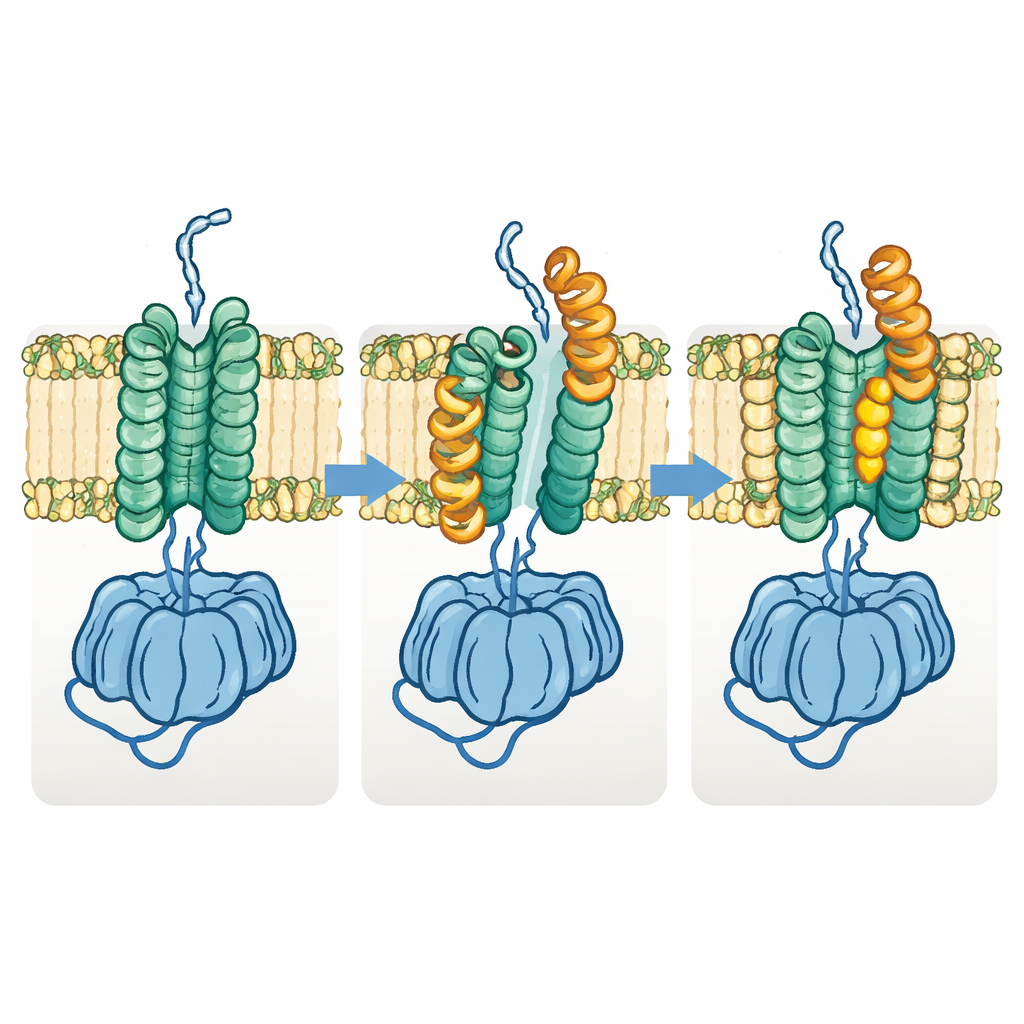
Un changement de forme nécessaire pour le transport du polymère
L’équipe a également découvert une forme distincte « ouverte » de Fks1. Dans cet état, une moitié de la région membranaire se décale latéralement et des hélices horizontales clés basculent vers l’extérieur, écartant l’espace entre les deux faisceaux membranaires et élargissant le tunnel apparent du glucane. La comparaison de nombreuses structures suggère que l’enzyme alterne entre les états basal et ouvert pendant son fonctionnement normal : l’état basal prépare et initie la formation du polymère, tandis que l’état ouvert permet à la chaîne en croissance de se déplacer latéralement à travers la membrane vers l’extérieur. Lorsque les auteurs ont conçu des liaisons disulfure destinées à verrouiller l’enzyme de façon permanente dans l’un ou l’autre état, les deux variantes ont en grande partie perdu leur activité, soutenant l’idée que ce changement de forme est essentiel à la fonction.
Ce que cela implique pour les futurs antifongiques
En montrant que l’enfumafungine et des drogues apparentées n’agissent pas en bloquant la poche catalytique mais en remodelant l’environnement membranaire local et en figeant la glucane synthase dans son état basal, cette étude révèle un mode d’action de médicament non conventionnel. Elle démontre aussi que Fks1 et Fks2 partagent des structures et des réponses aux médicaments presque identiques, expliquant pourquoi les deux doivent être pris en compte pour lutter contre la résistance. Plus largement, le travail met en lumière comment de petites molécules peuvent contrôler des protéines membranaires « non pharmacologiques » en se liant à des surfaces peu profondes et en recrutant des lipides, offrant un cadre conceptuel pour concevoir la prochaine génération d’antifongiques qui restent efficaces même lorsque les champignons évoluent.
Citation: You, ZL., Sun, L., Wang, LX. et al. Inhibition mechanism of the fungal β−1,3-glucan synthases by triterpenoid antifungal drugs. Nat Commun 17, 2347 (2026). https://doi.org/10.1038/s41467-026-69114-8
Mots-clés: médicaments antifongiques, paroi cellulaire fongique, glucane synthase, résistance aux médicaments, cryo-microscopie électronique