Clear Sky Science · fr
Structures Cryo-EM des intermédiaires d’assemblage portail-col du bactériophage T4 révèlent un mécanisme de rétention du génome viral
Comment un virus retient son ADN sous pression
Le bactériophage T4 est un virus qui infecte la bactérie E. coli et compacte son ADN si étroitement dans sa tête que la pression intérieure peut être cinq à sept fois supérieure à celle d’une bouteille de champagne. Pourtant, l’ADN ne fuit pas pendant que le virus termine la construction du reste de son corps. Cette étude révèle, en détail moléculaire, comment T4 résout ce problème en utilisant une minuscule double porte qui fonctionne comme une sas pour son matériel génétique.
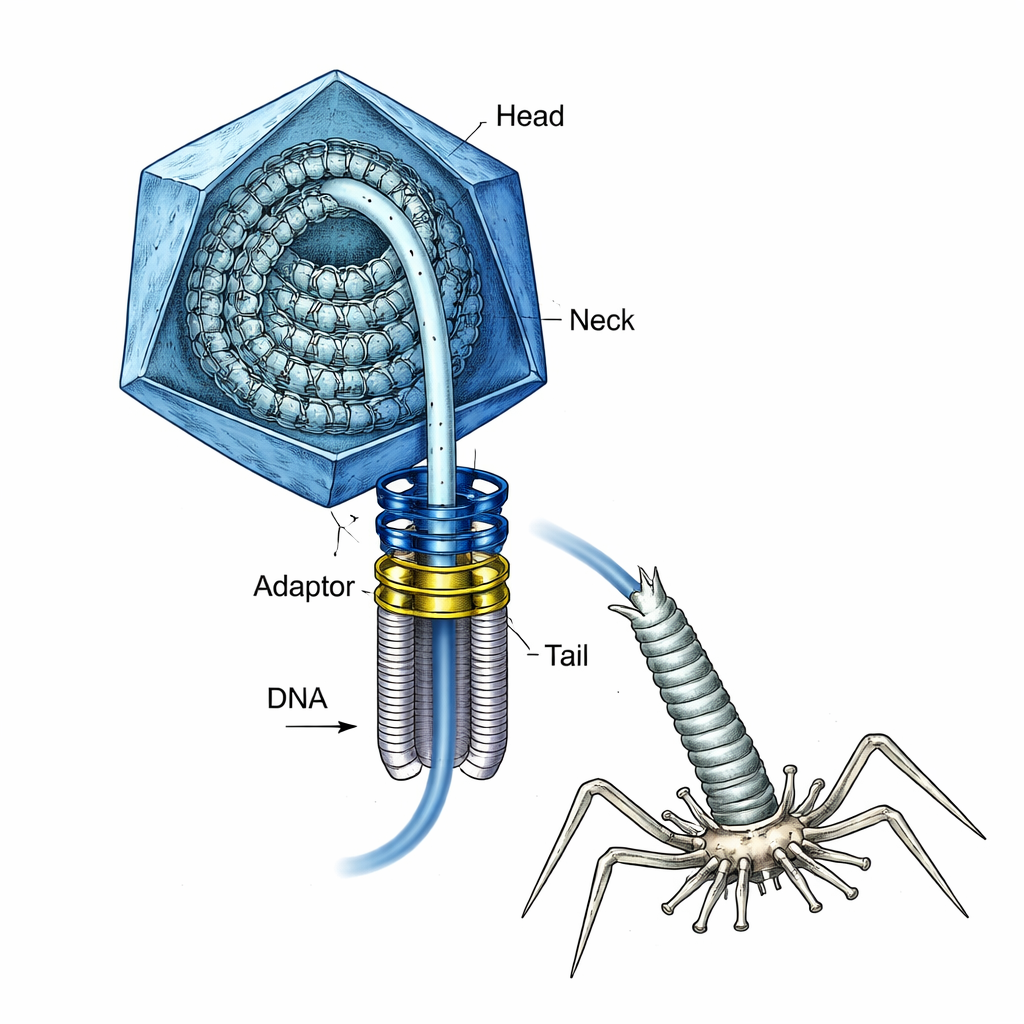
Le virus avec un ressort chargé à l’intérieur
T4 a longtemps été un cheval de bataille de la biologie moléculaire, et il sert aussi de modèle pour concevoir de futurs vaccins et vecteurs de délivrance génique. Lors de l’assemblage, le virus construit d’abord une coque protéique vide, ou tête, et un « portail » annulaire spécial à un sommet. Un moteur moléculaire puissant enroule ensuite l’ADN dans la tête à travers ce portail jusqu’à ce que la tête soit « pleine ». À ce stade, le moteur doit se détacher, un col et une queue doivent être attachés, puis l’ADN doit plus tard être injecté dans une bactérie — le tout sans permettre à l’ADN pressurisé de jaillir prématurément. La manière dont le virus maintenait cet ADN fortement contraint en sécurité pendant ces transitions n’était pas bien comprise.
Reconstruire le col en laboratoire
Les chercheurs ont recréé des éléments clés de T4 dans des bactéries et les ont mélangés de façon contrôlée pour observer comment le col — le connecteur entre la tête et la queue — s’assemble. Deux protéines virales, nommées gp13 et gp14, ont été produites séparément. Isolées, elles flottaient comme unités simples, mais ensemble elles s’emboîtaient en anneaux empilés formant un tunnel central pour le passage de l’ADN. À la surprise des scientifiques, une troisième protéine apparaissait dans ces préparations : Hfq, une protéine bactérienne bien connue qui aide généralement à contrôler l’ARN et l’activité génique chez E. coli. La spectrométrie de masse a confirmé que Hfq se liait spécifiquement à gp14, suggérant que le virus emprunte cette protéine de l’hôte comme composant de son col.
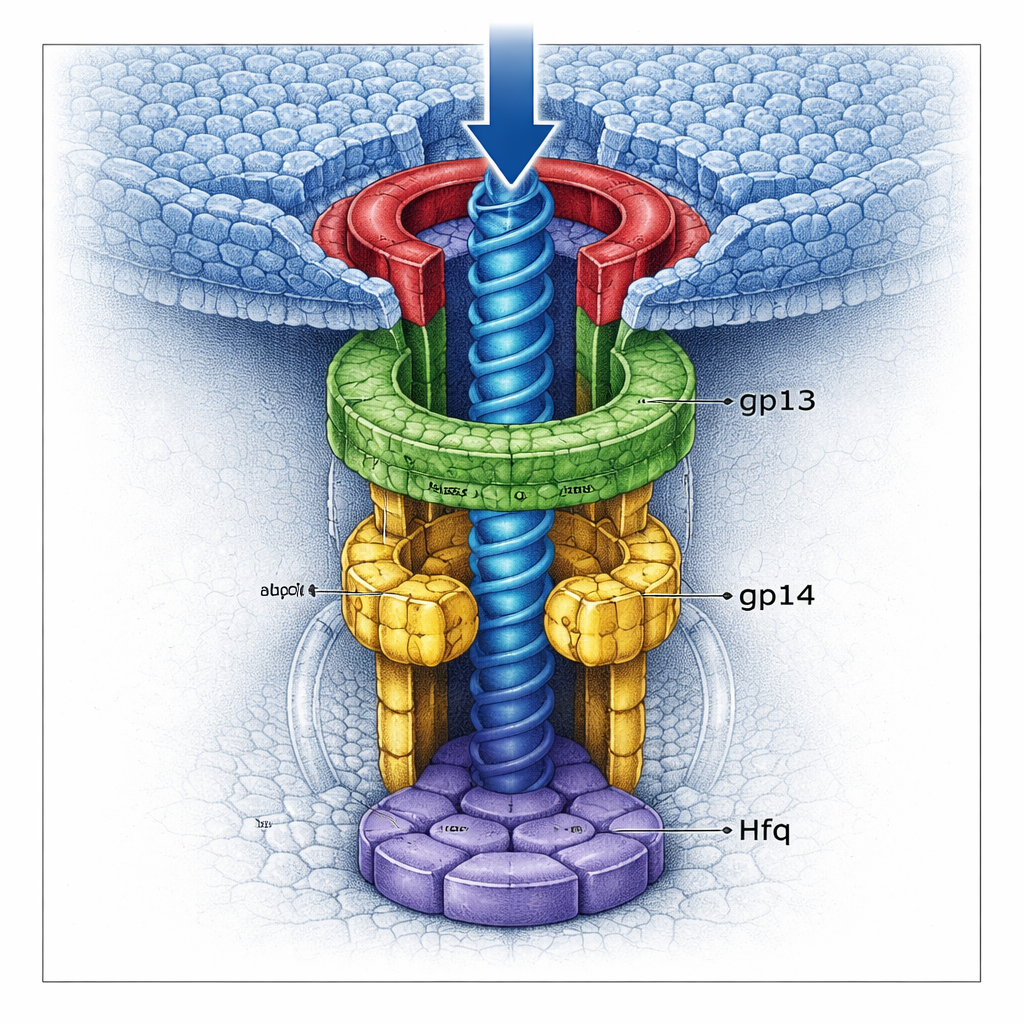
Une double porte qui verrouille le génome
Grâce à la cryo‑microscopie électronique à haute résolution, l’équipe a visualisé plusieurs variantes du complexe de col à détail quasi atomique. Ils ont trouvé que gp13 forme un large anneau qui s’adapte au portail, tandis que gp14 se positionne en dessous sous forme d’un hexamère, créant un canal plus étroit. Crucialement, chaque sous‑unité de gp14 apporte une longue boucle qui bascule vers le milieu du tunnel. Ensemble, six de ces « boucles‑bouchons » forment une porte serrée capable d’attraper le dernier segment d’ADN lorsqu’il tente de sortir de la tête. Sous gp14, la protéine Hfq détournée s’assemble en son propre hexamère, bouchant le bas du canal comme une seconde porte. En présence de Hfq, la structure gp13–gp14 est plus complète et rigide, et les portes combinées rétrécissent encore le tunnel, rendant la fuite d’ADN beaucoup moins probable.
Chronologie, prévention des erreurs et un auxiliaire emprunté
L’étude montre aussi que ce système n’est pas qu’un bouchon statique ; c’est une séquence soigneusement chorégraphiée de changements de conformation. Une fois la tête pleine, la pression interne pousse le portail dans une nouvelle conformation qui expose des sites de liaison pour gp13. Un col préassemblé gp13–gp14–Hfq vient alors s’amarrer sur le portail. Gp13 se plie, se relève et se verrouille à la fois sur le portail et sur la coque externe, tissant solidement le col dans la tête. Durant cette étape, les boucles‑bouchons de gp14 et le bouchon Hfq maintiennent l’ADN en place. Hfq joue un second rôle en tant que facteur de contrôle qualité : en occupant des surfaces clés de gp14, il empêche gp14 de se lier au portail au mauvais endroit, ce qui éviterait un assemblage erroné du col. Ce n’est que lorsque la queue préfabriquée arrive qu’une protéine de l’extrémité de la queue, gp15, forme une liaison encore plus forte avec gp14, délogeant Hfq et ouvrant la voie à une libération contrôlée de l’ADN dans la queue.
Pourquoi cela importe au‑delà d’un seul virus
Simplement dit, T4 utilise un verrou à deux portes pour retenir un puissant « ressort » d’ADN pendant qu’il termine de construire le reste du virus. La première porte est constituée de sa propre protéine de col, gp14, et la seconde porte est empruntée à la protéine Hfq de l’hôte, que le virus utilise temporairement puis rejette. Cette double porte garantit qu’à peine d’ADN est perdu et que le virus final est pleinement infectieux. Comme de nombreux grands virus compactent leurs génomes sous des pressions extrêmes similaires et partagent une architecture apparentée, ce travail suggère que des systèmes de verrouillage comparables, et même le détournement temporaire de protéines de l’hôte, pourraient être répandus. Comprendre ces mécanismes pourrait orienter la conception de vecteurs viraux plus sûrs en médecine et indiquer de nouvelles façons de bloquer des virus nuisibles en ciblant leurs « verrous » génomiques.
Citation: Han, L., Mao, Q., Zhu, J. et al. Cryo-EM structures of bacteriophage T4 portal-neck assembly intermediates reveal a viral genome retention mechanism. Nat Commun 17, 1964 (2026). https://doi.org/10.1038/s41467-026-69107-7
Mots-clés: bactériophage T4, assemblage viral, cryo‑microscopie électronique, conditionnement du génome, interaction hôte–virus