Clear Sky Science · fr
Base structurale de la pause lors de l’initiation de la transcription chez Mycobacterium tuberculosis
Comment les interrupteurs génétiques d’un germe peuvent s’enrayer
Mycobacterium tuberculosis, la bactérie responsable de la tuberculose, doit en permanence activer et désactiver des gènes pour survivre dans l’environnement hostile de l’organisme. Les travaux décrits dans cet article s’immiscent dans l’une des premières étapes de ce contrôle génétique, en capturant une « pause » fugace qui survient juste au moment où la cellule commence à transcrire l’ADN en ARN. Comprendre cette pause aide à expliquer comment le microbe décide de terminer l’activation d’un gène ou d’abandonner la tentative — et pourrait à terme révéler de nouvelles vulnérabilités exploitables par des antibiotiques.
Commencer le message à partir de l’ADN
Chez les bactéries, une grande machinerie protéique appelée ARN polymérase se déplace le long de l’ADN pour synthétiser de l’ARN, première étape vers la production de protéines. Pour démarrer, elle s’associe à des protéines d’aide appelées facteurs sigma qui la guident vers des sites de départ précis sur l’ADN et contribuent à ouvrir une petite « bulle » dans la double hélice. Pour Mycobacterium tuberculosis, l’un de ces facteurs, nommé sigma E, est particulièrement important lorsque la bactérie est soumise à des stress en dehors de sa membrane interne. Un autre facteur, CarD, stabilise la bulle d’ADN ouverte. Ensemble, ces éléments forment un complexe d’initiation qui produit les premiers nucléotides d’ARN avant soit de s’engager dans un message complet, soit d’abandonner et de relâcher de courts fragments d’ARN.
Une pause cachée à six ou sept bases
Des études biochimiques et en molécule unique avaient déjà suggéré que l’ARN polymérase marque souvent une pause très tôt, quand le nouvel ARN atteint seulement six ou sept nucléotides. Mais ces pauses sont extrêmement brèves et difficiles à observer directement, si bien qu’aucune structure haute résolution n’était disponible. Dans cette étude, les auteurs ont utilisé la cryo‑microscopie électronique pour figer et visualiser plusieurs variantes de la machinerie d’initiation de M. tuberculosis. Ils ont conçu des échafaudages ADN–ARN qui piègent le complexe quand l’ARN mesure six ou sept unités et ont résolu des structures pour trois états principaux : deux complexes d’initiation « classiques » et un complexe d’initiation distinct en pause.
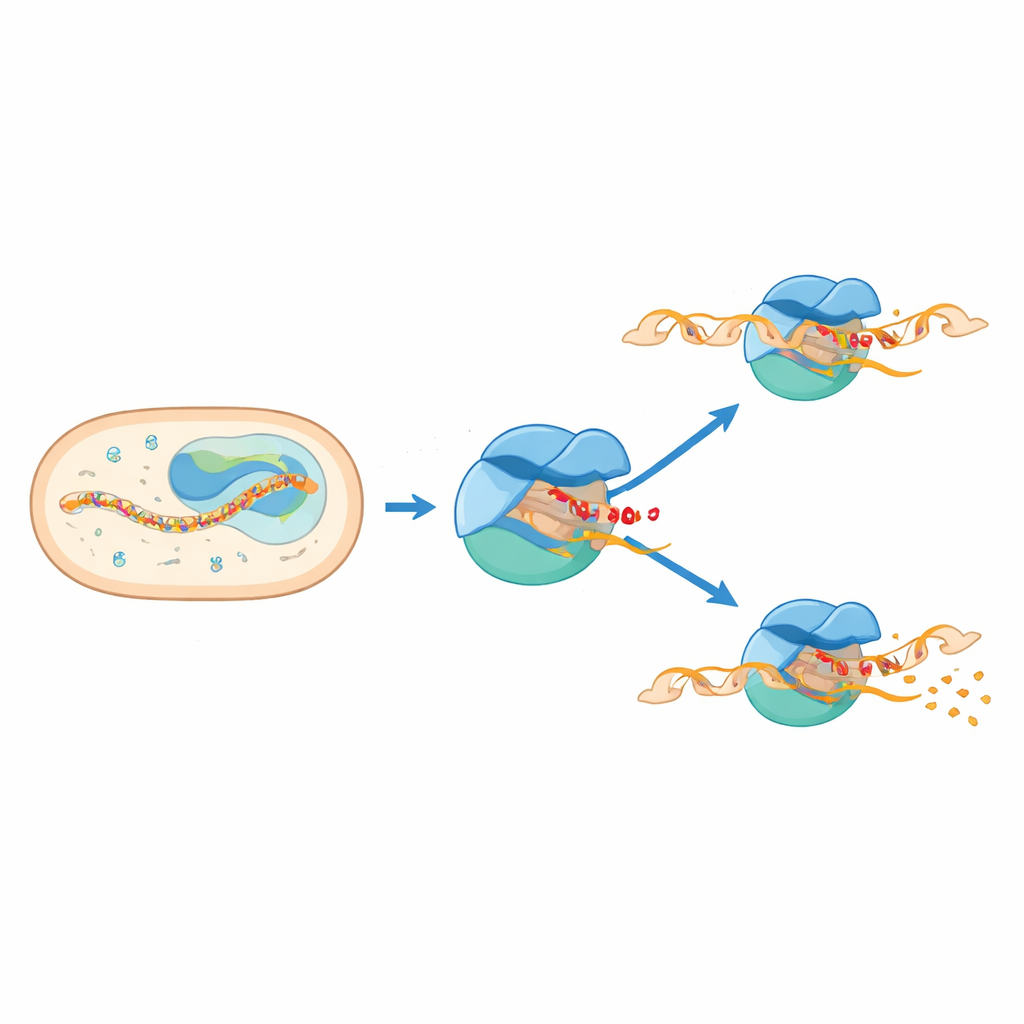
Quand deux parties de la machine se heurtent
Les structures montrent que la pause survient lorsque deux éléments de la machinerie cherchent à occuper le même espace. Un segment flexible de sigma E, connu sous le nom de région 3.2, s’avance dans le canal par lequel l’ARN en croissance doit passer pour sortir de l’enzyme. Lorsque l’ARN s’allonge jusqu’à six ou sept unités, son extrémité avant heurte cette boucle saillante. Cette collision force un mouvement de rotation d’un grand module au sein de l’ARN polymérase et déforme un élément structural clé nommé l’hélice pont. Parallèlement, l’ADN en amont du site actif est tiré vers l’intérieur et partiellement déroulé, produisant une bulle « écrasée » et coudée. Ces mouvements conjugués verrouillent le complexe dans un état de pause, à mi‑avancée, qui emmagasine une contrainte mécanique.
Un assistant métamorphe stabilise la bulle
CarD, le facteur accessoire, joue en réalité un rôle plus polyvalent qu’on ne le pensait. Dans le complexe d’initiation non en pause, CarD s’insère dans le sillon mineur d’un brin d’ADN au bord de la bulle, contribuant à maintenir la bulle ouverte pour permettre à l’ARN polymérase de commencer la synthèse. Dans le complexe en pause, CarD se repositionne pour embrasser le brin non matriciel opposé de l’ADN, travaillant de concert avec sigma E pour serrer plus fortement la bulle écrasée. Des essais biochimiques montrent que CarD favorise la transcription dépendante de sigma E et influence la quantité d’ARN accumulant au stade de six à sept unités. Ces résultats suggèrent que CarD stabilise à la fois l’état ouvert initial et aide le complexe en pause à éviter un effondrement prématuré.
Un point de contrôle entre échec et engagement
En comparant des structures haute résolution obtenues sur de l’ADN partiellement pré‑ouvert avec des structures de moindre résolution assemblées sur de l’ADN entièrement apparié, les auteurs montrent que les mêmes conformations de pause de base apparaissent dans des conditions plus naturelles. Ils proposent que la collision entre l’ARN en croissance et la boucle sigma 3.2 crée un point de contrôle chargé en énergie à six‑sept nucléotides d’ARN. À partir de cet état en attente, le complexe peut emprunter deux trajectoires principales : relâcher le court ARN et se réinitialiser — une tentative avortée — ou utiliser la contrainte emmagasinée pour se libérer de la région promotrice et entrer dans une production d’ARN stable et soutenue. Le repositionnement de CarD et l’assouplissement de l’emprise du facteur sigma sur l’ADN en amont semblent orienter cette décision.
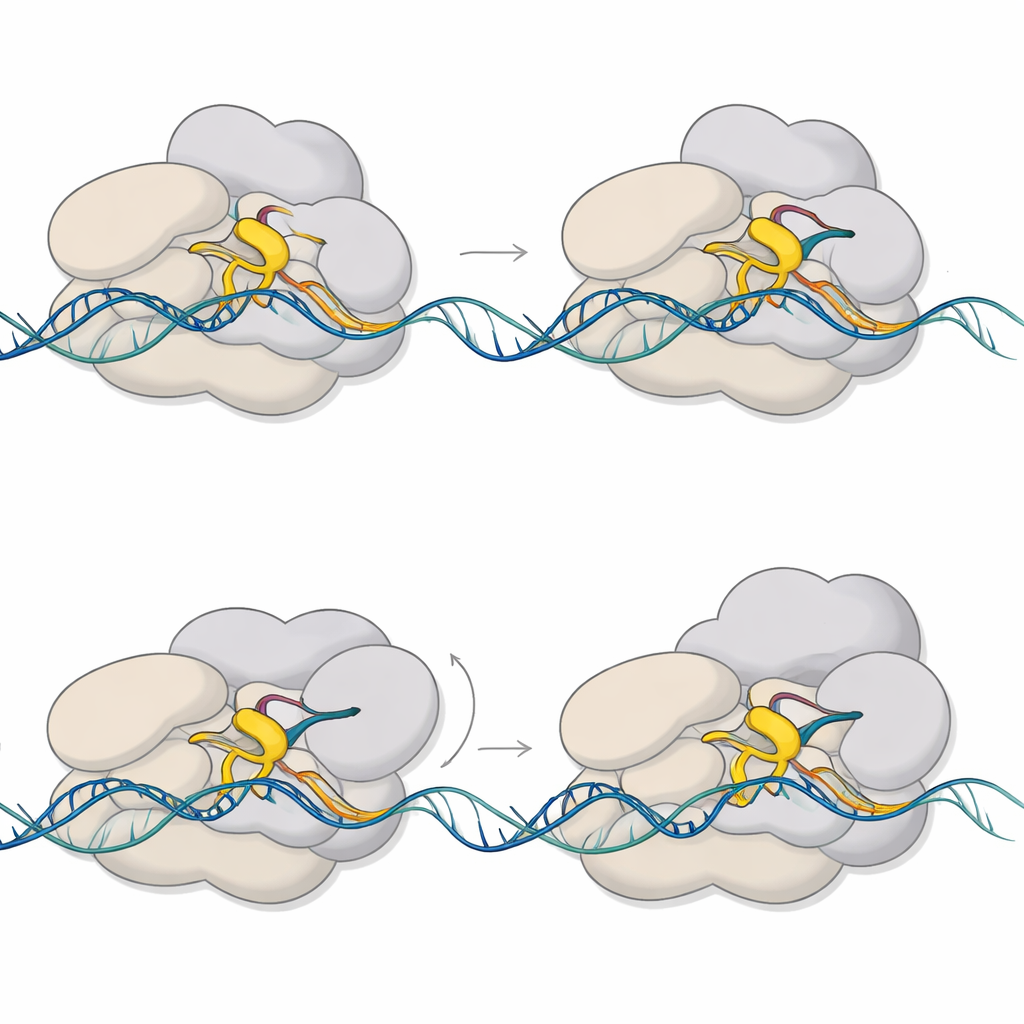
Pourquoi c’est important pour la tuberculose
Pour un lectorat non spécialiste, le message clé est que la bactérie de la tuberculose n’active pas simplement des gènes comme on allume une lampe. Elle hésite à une longueur d’ARN minuscule, utilisant une brève pause mécanique comme point de décision entre abandonner ou s’engager dans l’activation complète d’un gène. Ce travail capture cette pause en détail atomique, montrant comment une petite boucle mobile, un noyau qui pivote et une bulle d’ADN remodelée créent ensemble un point de contrôle contrôlable. Parce que sigma E et CarD sont centraux dans la réponse au stress de M. tuberculosis, ces découvertes pourraient éventuellement aider à concevoir des médicaments qui bloquent cette étape précoce et affaiblissent la capacité de la bactérie à s’adapter et à survivre.
Citation: Zheng, L., Xu, K. Structural basis of pausing during transcription initiation in mycobacterium tuberculosis. Nat Commun 17, 2197 (2026). https://doi.org/10.1038/s41467-026-69104-w
Mots-clés: initiation de la transcription, pause de l’ARN polymérase, Mycobacterium tuberculosis, facteurs sigma, cryo‑EM