Clear Sky Science · fr
Les ILC1 CD127+ du tissu adipeux induits par une péritonite aiguë expriment PD-L1 et atténuent l’inflammation chez la souris
Pourquoi la graisse abdominale peut aider à combattre une infection mortelle
Lorsque des bactéries s’échappent d’un intestin déchiré dans l’abdomen, l’organisme peut basculer dans un état potentiellement létal appelé septicémie. Cette étude révèle un allié inattendu dans cette lutte : un ensemble particulier de cellules immunitaires nichées dans la graisse abdominale qui migrent tôt lors de l’infection et agissent comme un frein intégré contre l’inflammation incontrôlée. Mieux comprendre le fonctionnement de ces cellules pourrait inspirer de nouveaux traitements qui calment les infections dangereuses sans supprimer complètement le système immunitaire.
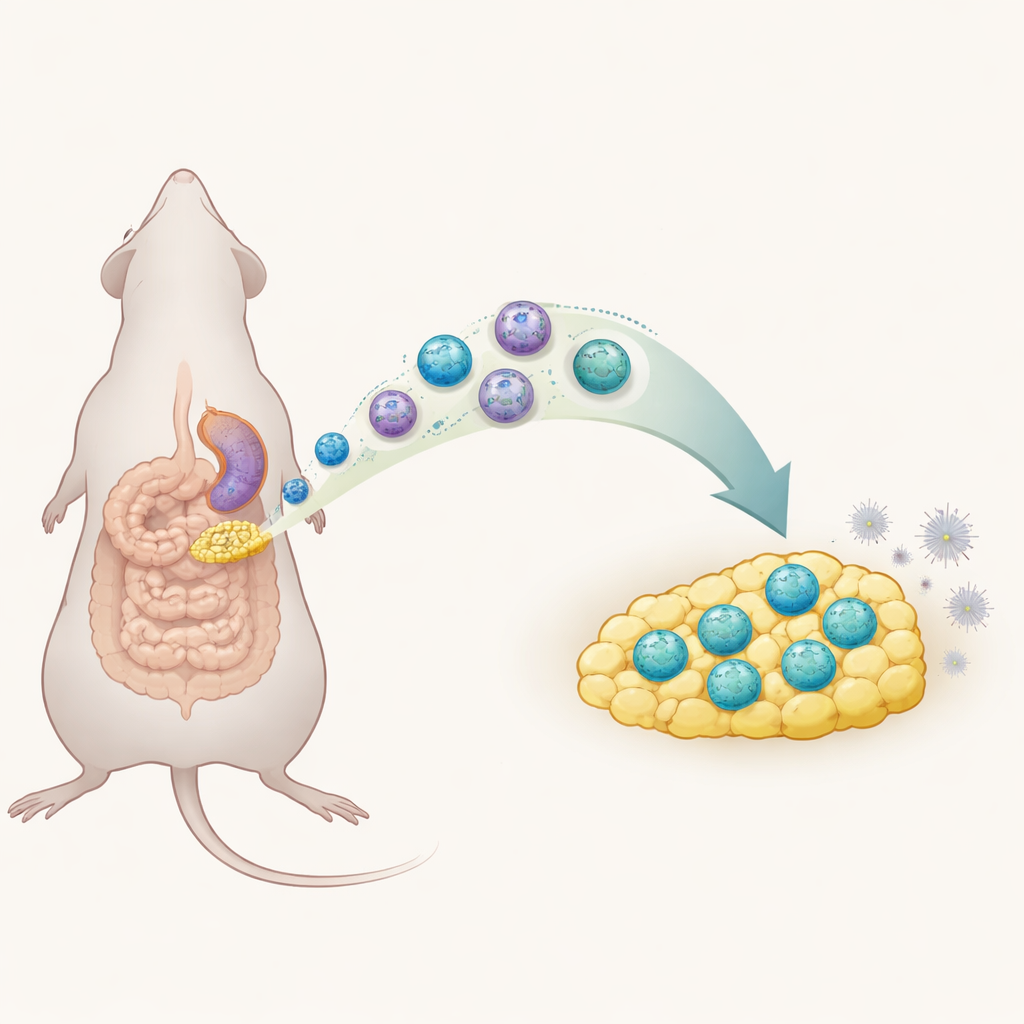
Une fuite dangereuse dans l’abdomen
La péritonite survient lorsque la paroi de l’abdomen s’enflamme, le plus souvent parce que des bactéries s’échappent d’un intestin perforé. Si cette tempête inflammatoire initiale n’est pas maîtrisée, les patients peuvent développer une septicémie, qui tue encore environ une personne sur cinq malgré les soins modernes. Les médecins peuvent traiter l’infection par chirurgie et antibiotiques, mais ils disposent de peu d’outils pour orienter la réaction immunitaire propre du corps afin d’éviter une suractivation nuisible. La graisse qui recouvre les intestins, appelée tissu adipeux mésentérique, est connue pour affluer vers les sites de lésion intestinale, ce qui suggère qu’elle joue un rôle actif dans cette réponse immunitaire précoce.
Gardiens cachés dans la graisse abdominale
Ces dernières années, les scientifiques ont découvert les « cellules lymphoïdes innées », des sentinelles immunitaires réactives présentes dans de nombreux tissus. Un sous‑type, appelé ILC1, aide normalement à déclencher des réactions inflammatoires puissantes. Dans cette étude chez la souris, les chercheurs ont utilisé un modèle chirurgical standard de péritonite pour étudier le comportement de ces cellules dans la graisse mésentérique. Ils ont constaté que, six heures après la lésion, ce tissu était encombré de signaux inflammatoires et d’un afflux d’ILC1, tandis que d’autres types cellulaires apparentés changeaient à peine. Ce calendrier coïncidait avec le pic de gravité chez les animaux, suggérant que les ILC1 étaient étroitement liés à la phase inflammatoire précoce dans l’abdomen.
Des cellules voyageuses qui changent de nature
Pour aller plus loin, l’équipe a utilisé un profilage cellulaire à la cellule unique pour subdiviser la population d’ILC1. Dans des conditions normales, la plupart des ILC1 de la graisse abdominale n’exprimaient pas la molécule CD127 à leur surface. Lors d’une péritonite aiguë, toutefois, un nouveau groupe d’ILC1 CD127‑positifs est apparu et s’est amplifié. Ces arrivants produisaient moins de l’efficace signal inflammatoire interféron‑gamma que leurs homologues CD127‑négatifs, ce qui les distinguait par une moindre agressivité. Les scientifiques ont montré que nombre de ces cellules ne se contentaient pas de se diviser sur place : des ILC1 de la rate migraient par la circulation sanguine vers la graisse mésentérique, guidés en partie par un signal chimique d’orientation appelé CXCL10 et par son récepteur CXCR3. Une fois dans la graisse, elles modifiaient leurs marqueurs de surface, acquérant CD127 et adoptant ce profil plus calme et plus régulateur.
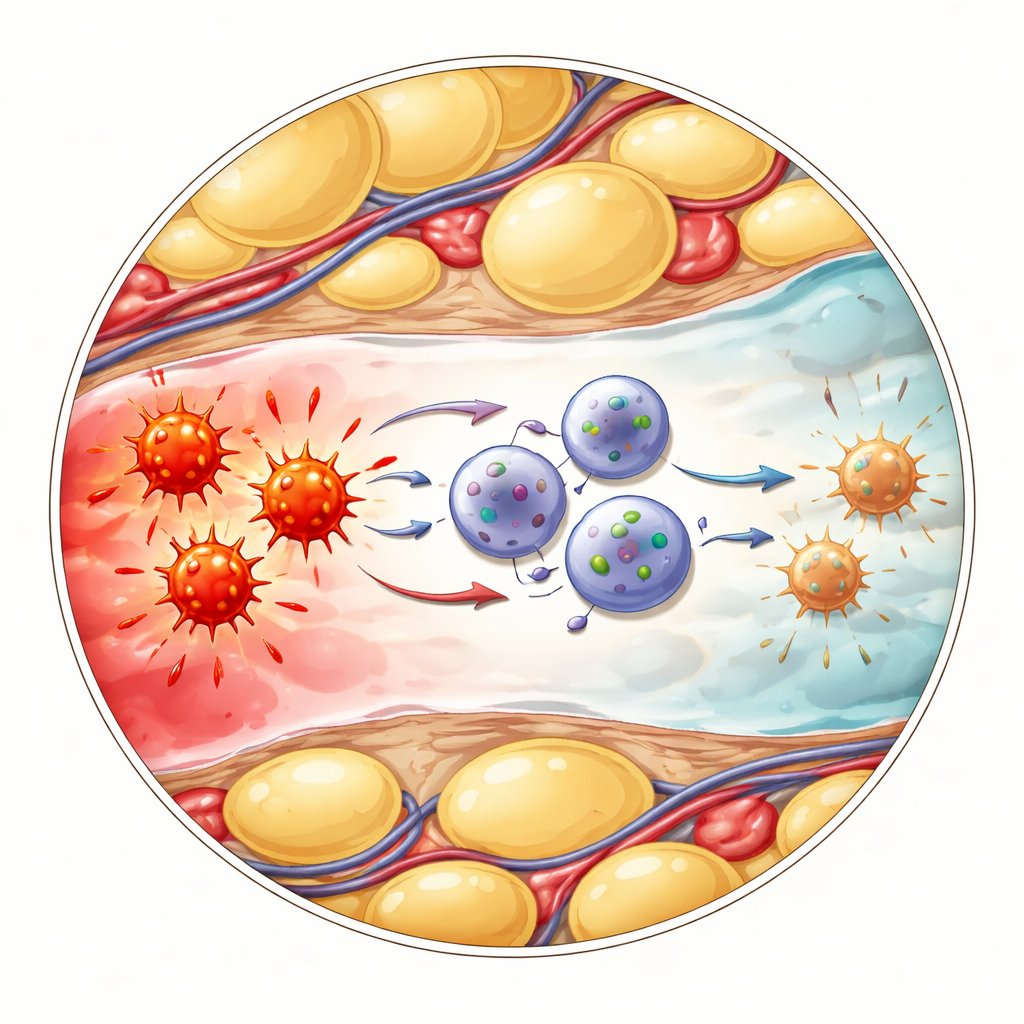
Comment les cellules apaisantes dialoguent avec les cellules enflammées
La question suivante était de savoir comment ces ILC1 modifiés refroidissaient l’inflammation. Les chercheurs se sont concentrés sur un autre groupe immunitaire, les cellules T gamma‑delta, qui réagissent rapidement au danger et peuvent libérer de grandes quantités de la molécule d’alarme TNF. Les analyses à la cellule unique suggéraient que les ILC1 CD127‑positifs et les cellules T gamma‑delta interagissaient via une voie de « frein » bien connue impliquant les protéines de surface PD‑L1 et PD‑1. Dans la graisse abdominale enflammée, les ILC1 récemment arrivés augmentaient fortement PD‑L1, tandis que les cellules T gamma‑delta voisines affichaient un niveau élevé de PD‑1. Lorsque l’équipe bloqua PD‑1 par des anticorps, les cellules T gamma‑delta produisirent davantage de TNF, confirmant que ce contact limite habituellement leur production inflammatoire. De même, des souris génétiquement incapables de produire des ILC1 présentèrent une maladie plus sévère, des marqueurs inflammatoires plus élevés et une production accrue de TNF par les cellules T gamma‑delta — des effets qui pouvaient être atténués en bloquant directement le TNF.
Ce que cela signifie pour les traitements futurs
En rassemblant ces éléments, les auteurs proposent un axe « rate‑vers‑graisse abdominale » : peu après la fuite bactérienne dans l’abdomen, des ILC1 quittent la rate, se dirigent vers le tissu adipeux mésentérique et s’y transforment en cellules riches en CD127 et PD‑L1 qui réduisent la production de TNF par les cellules T gamma‑delta. Plutôt que d’attiser l’inflammation, ces ILC1 spécialisés agissent comme des pacificateurs locaux, empêchant l’inflammation de déraper et contribuant possiblement à éviter que la péritonite n’évolue vers une septicémie mortelle. À long terme, des médicaments qui renforcent ou imitent ce circuit régulateur dans la graisse abdominale pourraient offrir une nouvelle façon de traiter les infections sévères — en réglant la réponse immunitaire pour qu’elle reste suffisante pour combattre les germes, sans mettre le patient en danger par une réponse excessive.
Citation: Nagata, R., Akama, Y., Goncalves, P. et al. Acute peritonitis-induced adipose CD127+ ILC1s express PD-L1 and ameliorate inflammation in mice. Nat Commun 17, 2391 (2026). https://doi.org/10.1038/s41467-026-69100-0
Mots-clés: péritonite, cellules lymphoïdes innées, tissu adipeux mésentérique, régulation immunitaire, septicémie