Clear Sky Science · fr
Réutiliser les récepteurs nucléaires pour former des condensats liquides sensibles aux ligands et réguler les gènes
Transformer les hormones en commutateurs cellulaires à la demande
Nos cellules captent en permanence des signaux comme les hormones et les vitamines et les traduisent en actions, par exemple en activant ou en réprimant des gènes. Cette étude montre comment des scientifiques peuvent exploiter ce langage naturel pour construire des « commutateurs » synthétiques qui répondent aux signaux corporels réels et qui peuvent même former de petites gouttelettes liquides à l’intérieur des cellules pour amplifier l’activité génique. De tels commutateurs contrôlés par les hormones pourraient un jour permettre de concevoir des thérapies géniques plus intelligentes, des biosenseurs précis ou des médicaments vivants étroitement liés à la physiologie du patient.
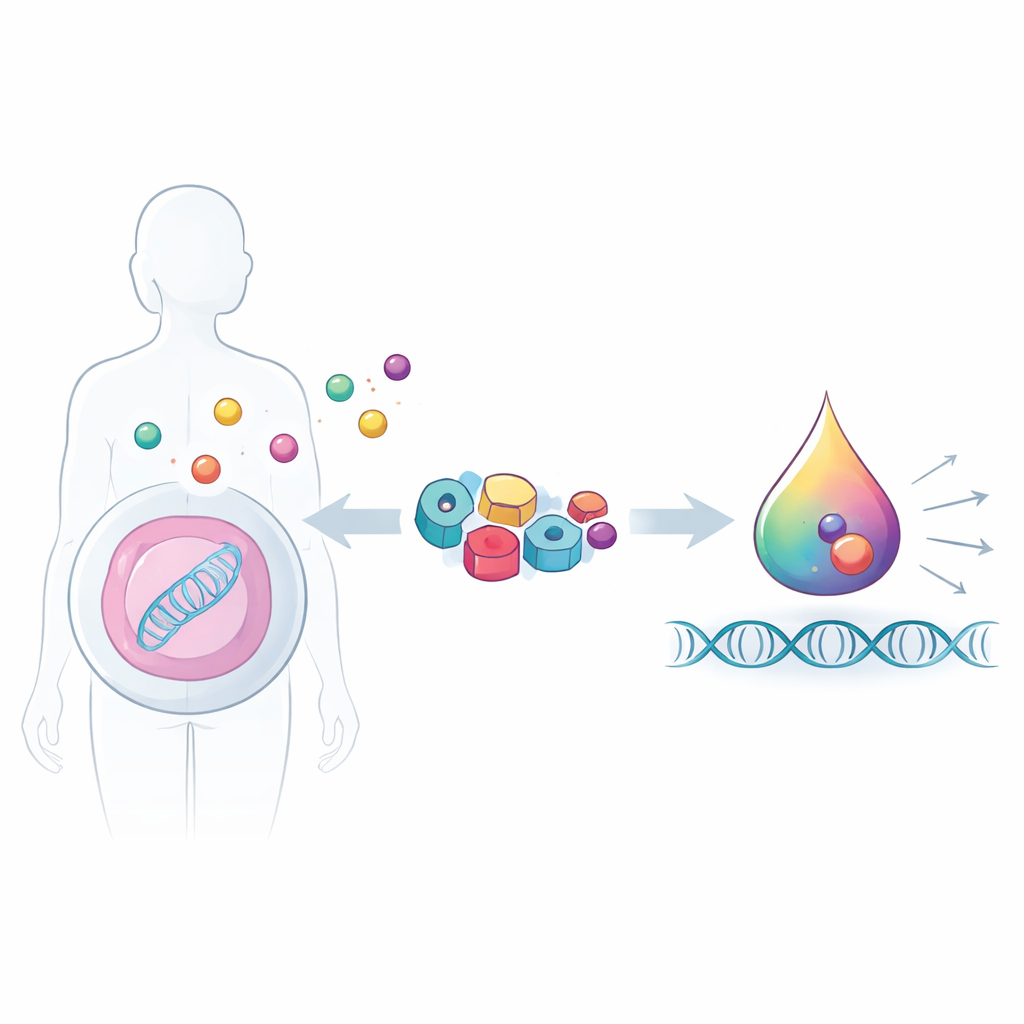
Utiliser les lecteurs de signaux endogènes de la cellule
Les hormones et molécules apparentées sont détectées par une famille de protéines appelées récepteurs nucléaires, qui siègent dans la cellule et contrôlent l’expression génique en réponse à des signaux tels que l’hormone thyroïdienne, la vitamine D, l’œstrogène et le cortisol. Chaque récepteur possède une poche qui lie son hormone spécifique et une surface qui recrute des protéines auxiliaires, appelées coactivateurs, lorsque l’hormone est présente. Plutôt que de concevoir des éléments entièrement artificiels, les chercheurs ont réutilisé ces récepteurs naturels et un court fragment d’un coactivateur humain (un peptide TIF2) comme blocs modulaires. Ce choix permet à leurs commutateurs synthétiques de parler le même langage biochimique que l’organisme, facilitant leur intégration aux voies de signalisation existantes.
Construire des commutateurs chimiques marche/arrêt
L’équipe a d’abord montré que la liaison de l’hormone pouvait rapprocher, à la demande, deux fragments protéiques conçus. Ils ont fusionné la partie liant le ligand de plusieurs récepteurs nucléaires à une demi‑enzyme rapporteur scindée, et ont rattaché le peptide TIF2 à l’autre moitié. Dans des cellules humaines, l’ajout de l’hormone correspondante amenait les deux moitiés à se réunir, restaurant la fluorescence du rapporteur, tandis que le retrait ou le blocage de l’hormone rompait la connexion. En associant des récepteurs tant à leurs drogues activatrices (agonistes) qu’aux drogues bloquantes (antagonistes), ils ont construit des commutateurs à deux entrées qui pouvaient être activés par un composé et désactivés par un autre, parfois de manière répétée et en quelques minutes. Ils ont aussi utilisé cette stratégie pour déplacer des enzymes vers des emplacements précis dans la cellule, modifiant localement des niveaux chimiques sur commande.
Contrôler les gènes par contacts multipliés
Pour transformer ces commutateurs en régulateurs de gènes, les chercheurs les ont reliés à une plate‑forme de liaison à l’ADN basée sur CRISPR. Une protéine Cas9 « morte » était guidée vers des sites d’ADN choisis, tandis que le récepteur nucléaire portait un domaine d’activation génique puissant. Lors de l’ajout de l’hormone, le récepteur se fixait sur des segments TIF2 attachés à la dCas9, apportant l’activateur sur le gène cible. Un seul segment TIF2 produisait des effets modestes, mais en enchaînant de nombreuses copies, ils ont créé un point d’ancrage multivalent capable de recruter de nombreux récepteurs simultanément. Cela a considérablement amplifié l’activation génique — jusqu’à des centaines de fois au‑dessus du niveau de base — et la réponse restait sensible dans des plages d’hormones proches de celles observées dans l’organisme. Les antagonistes pouvaient à nouveau réduire fortement cette activité, montrant un contrôle réversible et précis.
Créer des gouttelettes liquides qui turbo‑chargent l’expression
À mesure que le nombre de copies de TIF2 augmentait, l’équipe a observé un seuil net dans la performance, suggérant que les protéines pouvaient se condenser en gouttelettes. De nombreux régulateurs géniques naturels forment des « condensats » de type liquide qui concentrent la machinerie nécessaire à la transcription. Les chercheurs ont conçu volontairement des échafaudages qui regroupent de multiples motifs TIF2 à l’aide de peptides en hélice α enroulée (coiled‑coil), favorisant l’assemblage de plusieurs récepteurs au même endroit lorsque l’hormone est présente. Dans des cellules vivantes, cela produisait des gouttelettes sphériques et lumineuses se comportant comme des liquides : elles fusionnaient, récupéraient après photoblanchiment et pouvaient être dissoutes par des produits chimiques perturbant les faibles interactions protéiques. Fait important, les gouttelettes n’apparaissaient que sous des conditions multivalentes et hormonales appropriées, et les antagonistes pouvaient les faire disparaître, prouvant que la formation de gouttelettes était modulable chimiquement.
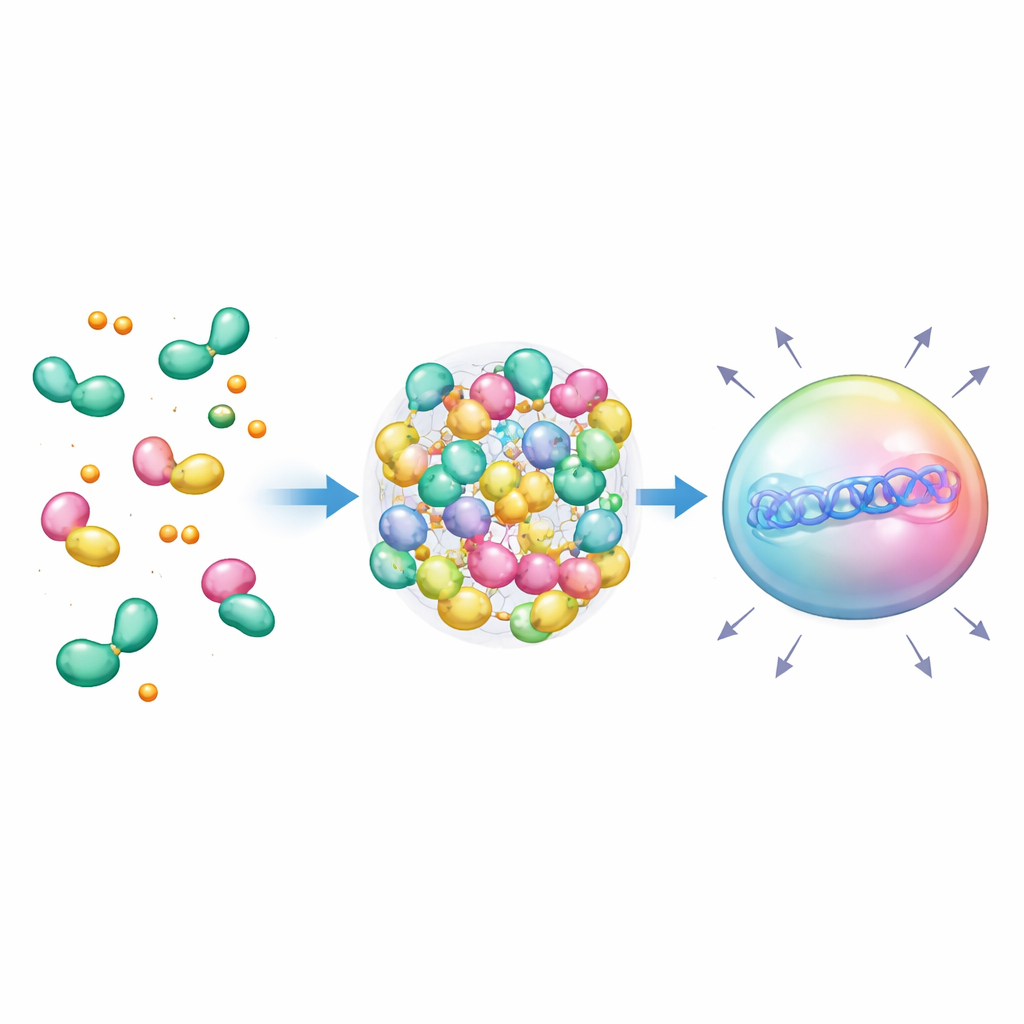
Des gouttelettes conçues vers des thérapies futures
En fusionnant ces gouttelettes contrôlées par les hormones aux outils CRISPR ciblant l’ADN, les auteurs ont créé des condensats nucléaires qui se positionnent directement au‑dessus de gènes spécifiques et amplifient massivement leur activité — même lorsqu’il n’existe qu’un seul site d’ancrage ADN. Comme les composants sont d’origine humaine et répondent à des signaux familiers tels que le cortisol et l’œstrogène, ces systèmes pourraient à terme être intégrés dans des circuits thérapeutiques réagissant automatiquement aux niveaux d’hormones du patient. Bien que des tests rigoureux soient nécessaires pour éviter les interférences avec les récepteurs endogènes, ce travail illustre un concept puissant : réutiliser les détecteurs hormonaux naturels et les condensats liquides comme commutateurs programmables pour détecter la chimie interne et induire des réponses géniques ciblées.
Citation: Rihtar, E., Fink, T., Ivanovski, F. et al. Repurposing nuclear receptors for ligand-responsive liquid condensate formation and gene regulation. Nat Commun 17, 2218 (2026). https://doi.org/10.1038/s41467-026-69099-4
Mots-clés: biologie synthétique, récepteurs nucléaires, signalisation hormonale, régulation des gènes, séparation de phase