Clear Sky Science · fr
Une stratégie synthétique combinatoire pour développer des vecteurs de livraison de protéines d’édition génomique ciblant la rétine de la souris
Nouveaux espoirs pour traiter la cécité héréditaire
De nombreuses formes de cécité héréditaire commencent par un seul gène défectueux dans les cellules photoréceptrices situées à l’arrière de l’œil. Les outils modernes d’édition génétique comme CRISPR peuvent, en principe, corriger ces erreurs, mais acheminer ces machines d’édition en toute sécurité dans les cellules adéquates a été un obstacle majeur. Cette étude décrit une nouvelle façon de transporter directement des éditeurs géniques puissants dans la rétine de souris en utilisant des particules de type lipidique spécialement conçues, ouvrant la perspective de traitements en une seule injection capables de restaurer la vision chez des personnes atteintes de maladies génétiques de l’œil.
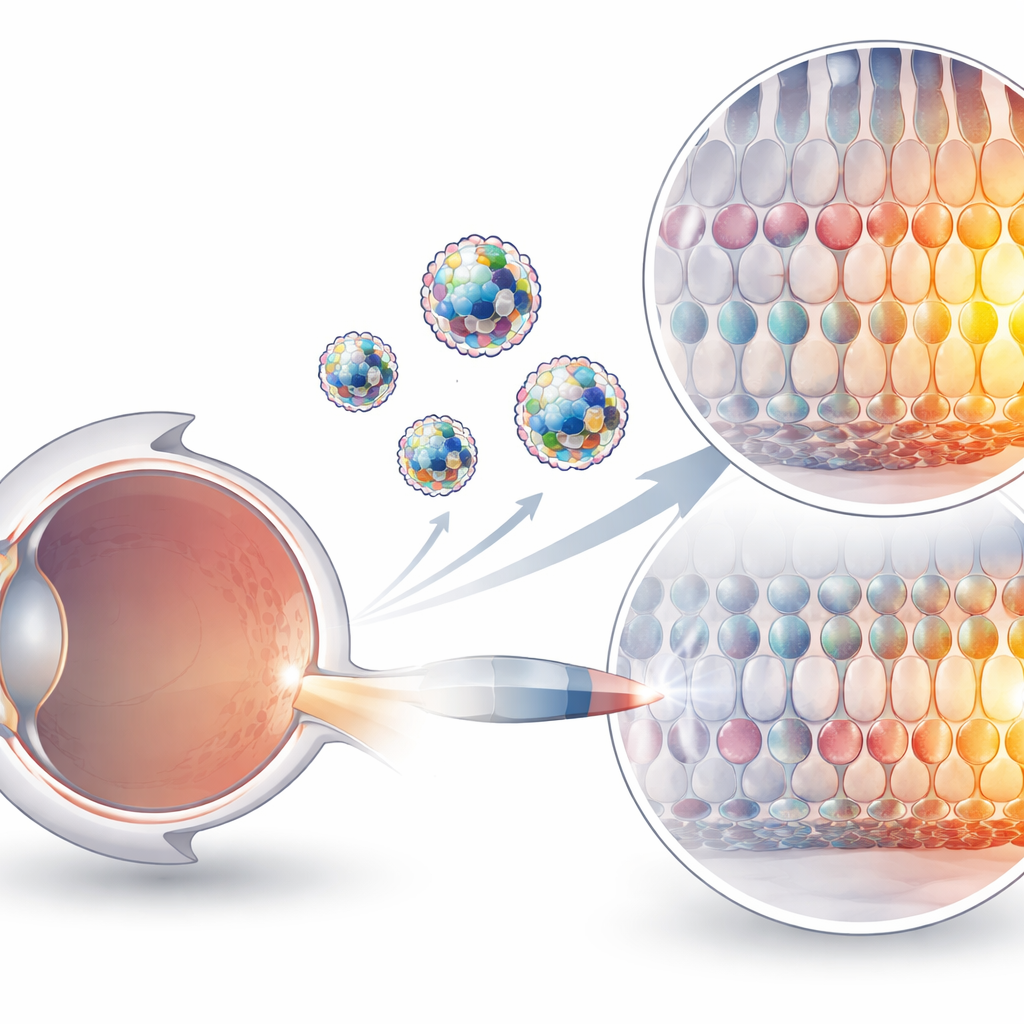
Pourquoi il est si difficile de livrer des éditeurs géniques
Les outils basés sur CRISPR peuvent désormais changer des lettres individuelles de l’ADN sans couper les deux brins, un progrès qui les rend attractifs pour traiter des troubles génétiques. Mais ces outils sont des complexes protéines–ARN volumineux, chargés électriquement et fragiles dans l’organisme. Les méthodes de livraison actuelles reposent largement sur des virus modifiés ou sur des particules qui transportent les plans génétiques de l’éditeur plutôt que l’éditeur lui-même. Les virus peuvent provoquer des réactions immunitaires et présentent des limites strictes de taille, tandis que l’administration d’ARN messager fonctionne très bien au niveau du foie mais reste inefficace dans de nombreux autres tissus, y compris l’œil. Injecter directement des complexes protéine–ARN préassemblés est conceptuellement plus propre et plus sûr, mais ils manquaient d’un véhicule approprié pour traverser les membranes cellulaires et atteindre leurs cibles.
Un navette inspirée d’un colorant pour les protéines
Les chercheurs se sont tournés vers un point de départ inattendu : le Coomassie Brilliant Blue, un colorant bleu profond couramment utilisé dans les laboratoires de biologie et déjà approuvé pour certaines interventions oculaires. Ce colorant se lie fortement à de nombreuses protéines. L’équipe a relié chimiquement des « têtes » Coomassie à des « queues » de type lipidique pour créer une famille de nouvelles molécules appelées lipidoïdes. En milieu aqueux, ces lipidoïdes ont tendance à s’agréger en particules, les parties huileuses étant enfouies à l’intérieur tandis que les groupes Coomassie sont exposés à l’extérieur, où ils peuvent accrocher des protéines. En faisant varier la longueur, le degré de ramification et la charge des queues, les scientifiques ont construit des dizaines de composés candidats conçus pour lier les protéines d’édition d’un côté et interagir avec les membranes cellulaires de l’autre.
Tester la livraison de protéines aux cellules oculaires
Pour savoir quelles conceptions fonctionnaient réellement, le groupe a d’abord utilisé une protéine test simple appelée Cre recombinase, qui inverse un interrupteur génétique passant de la fluorescence verte à rouge ou de rouge à verte dans des cellules et des souris génétiquement modifiées. Plusieurs lipidoïdes Coomassie ont transporté efficacement la Cre dans des cellules en culture, transformant une grande fraction des cellules du vert au rouge. Lorsqu’ils ont été injectés sous la rétine de souris rapporteurs, des composés sélectionnés ont déclenché des changements de couleur spectaculaires à la fois dans la couche pigmentaire qui soutient la vision et dans les photorécepteurs sensibles à la lumière, montrant que les protéines atteignaient les cellules mêmes les plus touchées dans de nombreuses maladies aveuglantes. Ces premières expériences ont également révélé que de subtiles modifications de la structure des lipidoïdes pouvaient modifier les types cellulaires ciblés, laissant entendre que des versions futures pourraient être adaptées à des couches rétiniennes particulières.
Renforcer l’édition génique et restaurer la vision
Ensuite, l’équipe a chargé son système d’un éditeur de base adénine, une variante affinée de CRISPR capable de corriger la mutation d’une seule lettre provoquant la perte de vision chez des souris rd12, un modèle d’une cécité infantile sévère. Pris isolément, le complexe protéine–ARN de l’éditeur pénétrait mal les cellules. Un lipidoïde, baptisé CBB11, améliora la livraison mais avait tendance à former des agrégats en solution. Pour le stabiliser, les chercheurs ont incorporé CBB11 dans de petits liposomes bien définis — des sphères creuses composées de plusieurs types de lipides, incluant des composants cliniquement utilisés dans des vaccins à ARN messager. Dans ces formulations, CBB11 à la surface du liposome saisissait la partie protéique de l’éditeur, tandis que d’autres lipides contribuaient à lier l’ARN guide, créant une enveloppe coopérative qui maintenait l’ensemble du complexe à l’extérieur de la particule.
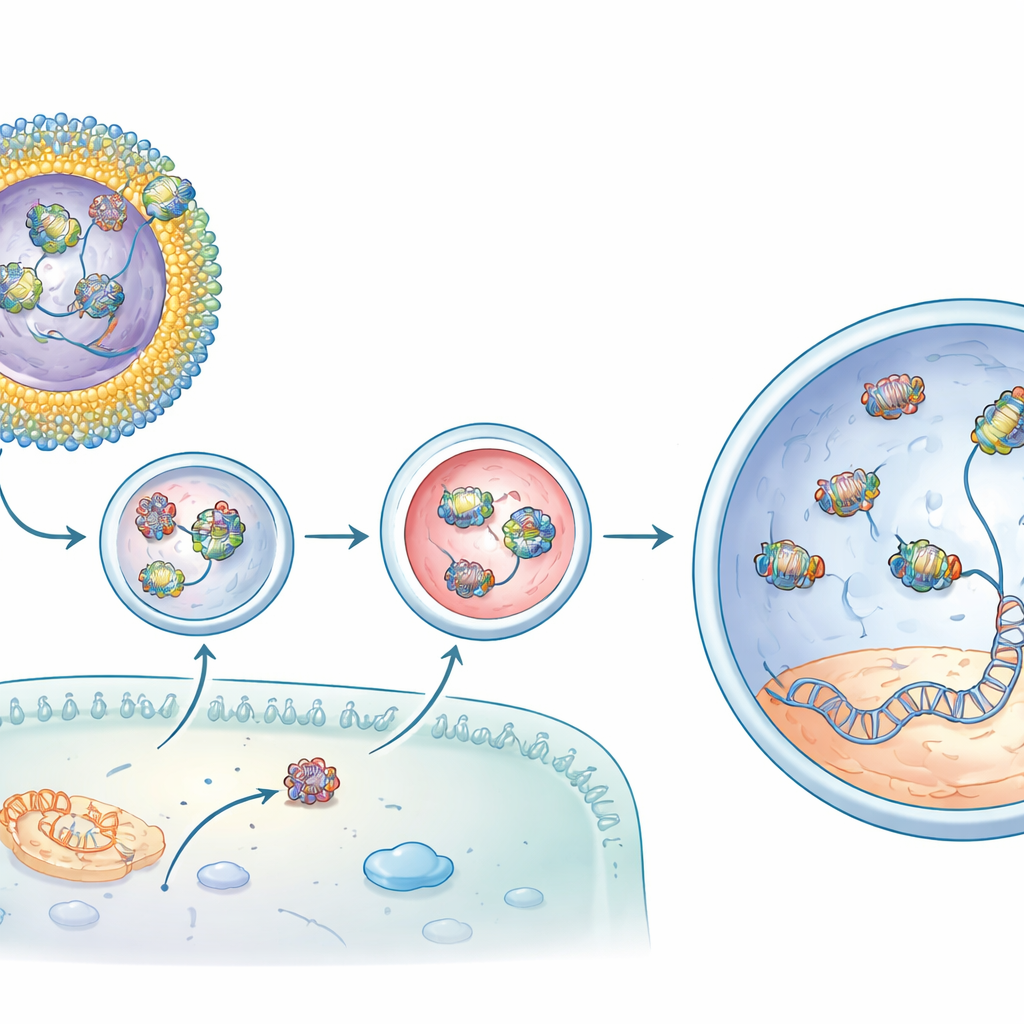
De la réparation moléculaire aux réponses à la lumière rétablies
Lorsque ces liposomes contenant CBB11 et portant l’éditeur de base ont été injectés sous la rétine des souris rd12, les résultats ont été saisissants. Comparée à l’injection de l’éditeur seul, la formulation optimisée a augmenté la correction d’ADN souhaitée dans le gène cible de plus d’un ordre de grandeur et a produit des niveaux encore plus élevés d’ARNm corrigé. L’analyse chimique a montré une récupération du pigment rétinien photosensible qui fait défaut dans la maladie. Plus convaincant encore, des enregistrements électriques des yeux des animaux ont révélé que leurs cellules en bâtonnets avaient retrouvé une grande partie de leur capacité à répondre à une lumière faible — jusqu’à environ les trois quarts du signal d’une souris normale dans les meilleurs cas. Les modifications hors cible ailleurs dans le génome étaient au niveau du bruit de fond, suggérant que l’édition était à la fois puissante et précise.
Ce que cela pourrait signifier pour les futures thérapies oculaires
Pour un non-spécialiste, le message clé est que les auteurs ont construit un « bus-navette » réutilisable pour les protéines d’édition génétique qui fonctionne directement dans l’œil vivant. En décorant des particules lipidiques sûres, de type vaccinal, avec un colorant capable d’accrocher les protéines, ils ont créé un système pouvant capter différents éditeurs à sa surface, les délivrer dans les cellules rétiniennes, corriger des mutations responsables de maladies et restaurer de façon mesurable la vision chez la souris après un seul traitement. Bien que des travaux supplémentaires soient nécessaires pour évaluer pleinement la sécurité, améliorer le ciblage et adapter la méthode à l’usage humain, cette plateforme ouvre la voie à de futurs médicaments de précision en une seule administration pour les maladies rétiniennes héréditaires et possiblement d’autres affections génétiques où une réparation localisée de l’ADN pourrait faire la différence entre la cécité et la vision.
Citation: Zhang, J., Hołubowicz, R., Smidak, R. et al. A combinatorial synthetic strategy for developing genome-editing protein-delivery agents targeting mouse retina. Nat Commun 17, 2479 (2026). https://doi.org/10.1038/s41467-026-69077-w
Mots-clés: thérapie génique rétinienne, édition de bases CRISPR, liposomes, transport de protéines, cécité héréditaire