Clear Sky Science · fr
Aperçus de la structure et de la modulation de TWIK-2 humain
Pourquoi cette minuscule porte de nos cellules compte
Au cœur de nos cellules, des portes microscopiques constituées de protéines contrôlent le passage d’atomes chargés, déterminant la manière dont les nerfs déclenchent des signaux, dont les vaisseaux sanguins se contractent et dont notre système immunitaire réagit. Une de ces portes, appelée TWIK-2, a été associée à l’hypertension pulmonaire et à une inflammation délétère, mais jusqu’ici les scientifiques savaient peu de choses sur sa construction ou sur la façon de la cibler par des médicaments. Cette étude révèle la structure détaillée de TWIK-2 humain, décrit son comportement électrique et esquisse comment on pourrait le viser pour développer de nouveaux anti‑inflammatoires.
Un canal discret aux fortes implications pour la santé
TWIK-2 appartient à une vaste famille de canaux potassiques de type « fuite » qui contribuent au potentiel de repos des cellules en laissant des ions potassium traverser la membrane cellulaire. Alors que d’autres membres de cette famille, comme les canaux TREK et TASK, ont été largement étudiés et liés à la douleur et à l’humeur, TWIK-2 est resté méconnu parce qu’il est difficile à enregistrer et s’exprime mal dans les systèmes de laboratoire standards. Pourtant, des études sur animaux et des études cellulaires ont relié TWIK-2 à l’hypertension pulmonaire, aux lésions pulmonaires aiguës, à la perte auditive et à l’activation d’un complexe immunitaire appelé l’inflammasome NLRP3, qui entraîne une inflammation dommageable dans la septicémie et d’autres pathologies. Comprendre le fonctionnement de TWIK-2 est donc essentiel tant pour la biologie fondamentale que pour la conception de thérapies ciblées.
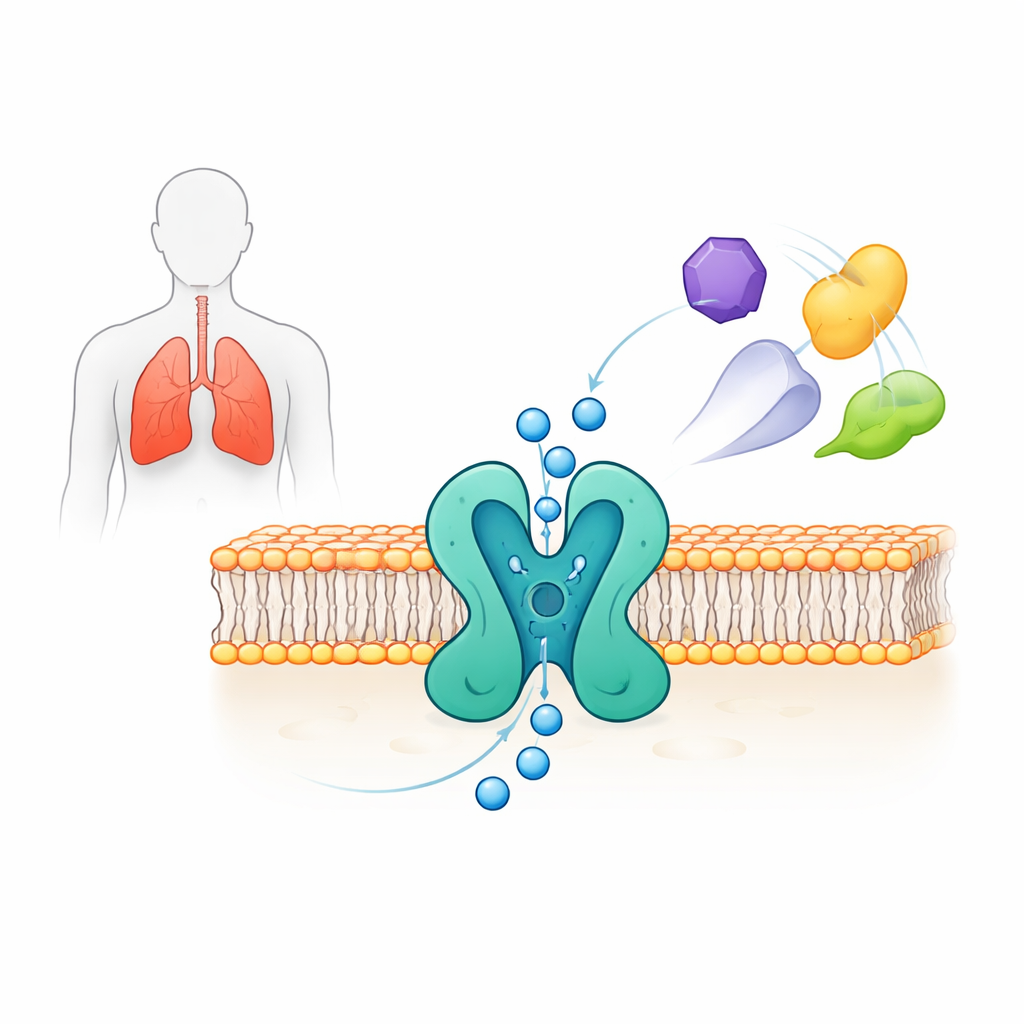
Voir la porte au niveau atomique
Les chercheurs ont exprimé la protéine TWIK-2 humaine en pleine longueur dans des lignées cellulaires humaines et ont utilisé la cryo‑microscopie électronique en particules uniques pour déterminer sa structure tridimensionnelle à une résolution d’environ 3,7 angströms. Le canal forme une assemblage en deux parties qui crée ensemble un pore central permettant le passage des ions potassium. Chaque moitié contient quatre segments transmembranaires et deux « hélices de pore » qui façonnent une région étroite appelée filtre de sélectivité, où le potassium est distingué des autres ions. Au‑dessus du pore, deux structures arquées en forme de « chapeau » créent deux voies d’entrée séparées pour les ions depuis l’extérieur de la cellule. La structure révèle aussi des asymétries subtiles entre les deux côtés du pore qui confèrent à TWIK-2 une organisation pseudo‑quadruple, caractéristique de cette famille de canaux.
Lipides dissimulés et un chemin ionique finement réglé
Le long du trajet de conduction ionique, l’équipe a cartographié comment les ions potassium se déplacent depuis l’intérieur de la cellule, à travers une « manchette » hydrophobe, jusqu’au filtre de sélectivité, puis sortent sous le chapeau. Le point le plus étroit reste suffisamment large pour que le potassium voyage en file indienne. Bien que la protéine ait été purifiée sans lipides ajoutés, les cartes cryo‑EM ont montré des densités tubulaires nichées près de la partie inférieure du pore et dans des poches latérales entre les hélices. Celles‑ci représentent probablement des lipides ou des queues de détergent restées associées à TWIK-2 lors de la purification, suggérant que des graisses membranaires naturelles peuvent se loger dans ces creux et modifier subtilement la conformation des hélices voisines. De tels déplacements, en particulier dans une hélice appelée M4 et dans les boucles du filtre de sélectivité, sembleraient régler si le canal est ouvert, fermé ou dans un état intermédiaire.
Explorer la porte par mutations et bloqueurs
Pour relier structure et fonction, les scientifiques ont utilisé un système de patch‑clamp automatisé pour mesurer les courants de cellules exprimant soit TWIK-2 normal, soit des variantes avec des acides aminés spécifiques modifiés. Ils ont constaté que TWIK-2 dépend fortement du potentiel électrique mais, contrairement à son cousin TWIK-1, est en grande partie insensible aux variations d’acidité externe. Des mutations sur deux thréonines conservées à la base du filtre de sélectivité ont rendu le canal plus rapidement activable et ont augmenté le courant, suggérant que ces sites agissent comme des charnières clés stabilisant l’état fermé. Des modifications à l’entrée et à la sortie du pore ont altéré la vitesse d’activation et d’inactivation du canal, révélant à quel point le trajet ionique est finement contrôlé. L’équipe a ensuite testé quatre petites molécules connues pour moduler des canaux apparentés. Deux d’entre elles, ML365 et NPBA, ont bloqué puissamment TWIK-2, tandis que les autres n’ont eu aucun effet. En comparant comment diverses mutations modifiaient la sensibilité aux médicaments, les auteurs en déduisent que ces composés se lient probablement juste sous le filtre de sélectivité et dans des cavités proches, et que différents médicaments utilisent des modes de liaison qui se chevauchent mais diffèrent par certains détails.
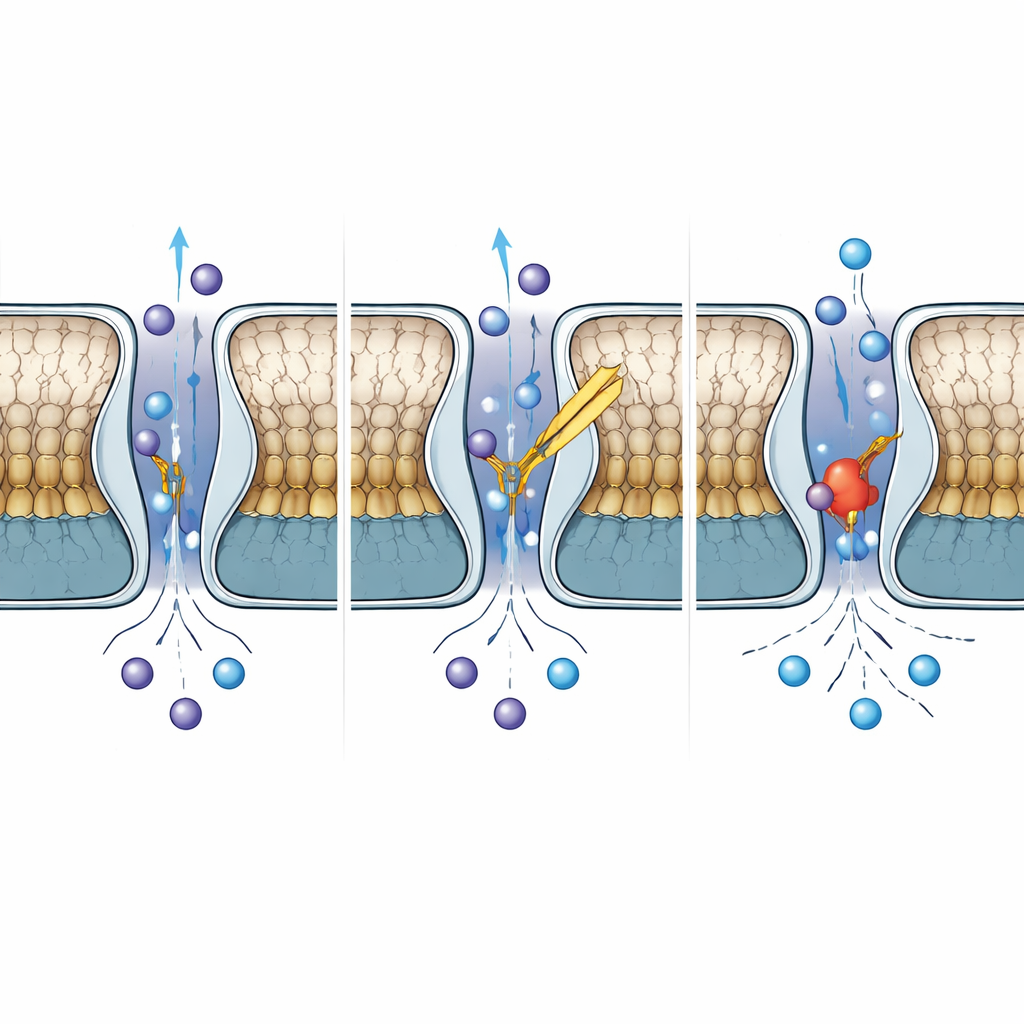
En quoi TWIK-2 diffère de ses proches parents
Bien que TWIK-2 partage plus de la moitié de sa séquence avec TWIK-1, leur comportement diverge sur des points importants. En comparant TWIK-2 avec des structures publiées de TWIK-1 à pH neutre et acide, les auteurs ont constaté que la région du chapeau de TWIK-2 ressemble à la forme inhibée par l’acide de TWIK-1, tandis que son filtre de sélectivité reste arrangé comme dans la forme conductrice et ouverte. Une histidine unique dans TWIK-1, connue pour détecter les protons et se rabattre dans le pore pour bloquer le passage des ions à faible pH, est remplacée par une tyrosine dans TWIK-2. Même lorsque l’équipe a réintroduit une histidine en ce positionnement dans TWIK-2, le canal n’est pas devenu sensible au pH, montrant que le contrôle par le pH dans ces canaux repose sur un réseau plus étendu de résidus et de mouvements, et non sur un seul acide aminé « interrupteur ».
De la structure aux thérapies futures
Dans l’ensemble, ce travail fournit la première image à haute résolution de TWIK-2 humain et cartographie comment des caractéristiques structurelles spécifiques influencent le flux ionique, la réponse à la tension et la sensibilité aux bloqueurs de petites molécules. La découverte que des composés existants peuvent inhiber sélectivement TWIK-2, associée à une plateforme de criblage automatisée robuste, ouvre la voie à des recherches à grande échelle pour identifier des médicaments plus sûrs et plus puissants. Parce que l’activité de TWIK-2 dans les cellules immunitaires a été liée à une inflammation incontrôlée, en particulier dans les poumons, de tels médicaments pourraient constituer la base de nouveaux traitements anti‑inflammatoires agissant en « diminuant » en douceur cette minuscule mais puissante porte de la membrane cellulaire.
Citation: Ma, Q., Hernandez, C.C., Navratna, V. et al. Insights into the structure and modulation of human TWIK-2. Nat Commun 17, 2201 (2026). https://doi.org/10.1038/s41467-026-69072-1
Mots-clés: canal potassique TWIK-2, canaux K2P à deux pores, structure d’un canal ionique par cryo-EM, modulateurs de canaux potassiques, inflammation pulmonaire