Clear Sky Science · fr
Protéomique spatiale monocellulaire du côlon et modèles murins relient la dysfonction mitochondriale à une carence en plasmocytes sécréteurs d’IgA dimérique dans la maladie de Crohn
Pourquoi les anticorps intestinaux sont importants dans la maladie de Crohn
La maladie de Crohn est surtout connue pour ses poussées douloureuses d’inflammation intestinale, mais bien avant que les symptômes n’apparaissent, des altérations subtiles peuvent affecter la façon dont le système immunitaire protège l’intestin. Cette étude pose une question simple mais essentielle : les personnes souffrant de la maladie de Crohn en rémission produisent‑elles toujours le bon type d’anticorps pour maintenir les microbes intestinaux sous contrôle pacifique ? En combinant des prélèvements de patients, un profilage tissulaire haute résolution, des analyses métaboliques et des modèles murins, les auteurs mettent au jour une faiblesse cachée du bouclier d’anticorps intestinal, liée à la production d’énergie cellulaire.
Un revêtement protecteur qui fait défaut
Nos intestins dépendent d’un anticorps spécial appelé IgA sécrétoire, libéré dans le mucus qui tapisse le tube digestif. L’IgA, notamment sous sa forme « double » appelée IgA dimérique, enrobe les bactéries et autres microbes, les maintenant à la surface plutôt que profondément dans les tissus. Dans ce travail, les chercheurs ont examiné des biopsies du côlon, du sang et des selles de personnes atteintes de la maladie de Crohn en rémission et de témoins non inflammatoires. Dans le tissu colique, les patients atteints de Crohn présentaient en réalité davantage de cellules B et de cellules productrices d’anticorps ainsi que des niveaux plus élevés de gènes et protéines liés à l’IgA. Pour autant, lorsque l’équipe a mesuré l’IgA dans les selles, ils ont observé l’effet contraire de ce à quoi on pourrait s’attendre : l’IgA sécrétoire dans la lumière intestinale était significativement réduite. 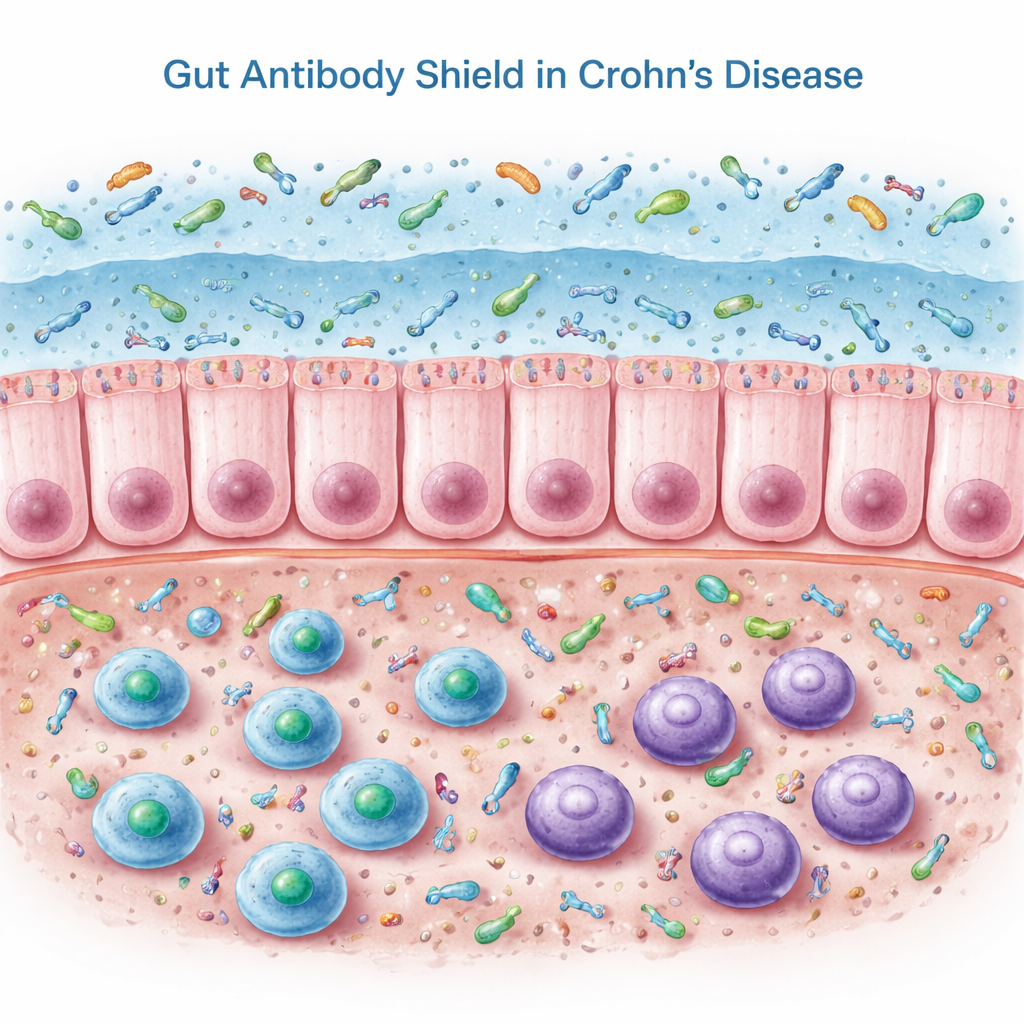
Bloquées à mi‑chemin : des cellules productrices d’anticorps qui ne parviennent pas à maturité complète
Les cellules qui sécrètent l’IgA — les plasmocytes — mûrissent normalement selon des étapes définies, depuis des précurseurs actifs et de courte durée de vie jusqu’à des spécialistes longévifs qui produisent de grandes quantités d’IgA dimérique. En utilisant la protéomique spatiale monocellulaire, qui cartographie de nombreuses protéines sur des cellules individuelles au sein du tissu intact, les auteurs ont pu distinguer des sous‑ensembles de plasmocytes immatures et pleinement matures dans le côlon. Chez les patients atteints de Crohn, les plasmablastes précoces et les plasmocytes immatures étaient augmentés, tandis que les plasmocytes les plus matures étaient réduits. Des analyses biochimiques ont confirmé que le rapport IgA dimérique/IgA monomérique était plus faible dans les côlons des patients atteints de Crohn, et chaque cellule productrice d’anticorps sécrétait en moyenne moins d’IgA dimérique. Lorsque l’équipe a isolé des cellules B mémoire commutées du côlon et les a induites en culture à devenir des plasmocytes, les cellules issues de patients de Crohn n’ont pas réussi à réguler à la hausse des marqueurs clés de maturation et ont produit moins d’IgA totale et dimérique, alors que la production d’IgG restait globalement normale. Cela suggère un blocage intrinsèque du programme de maturation spécifiquement pour les plasmocytes sécréteurs d’IgA.
Les centrales énergétiques sous tension
Pour comprendre ce qui provoque ce blocage, les chercheurs se sont penchés sur le métabolisme cellulaire. Ils ont constaté que les plasmocytes dans le tissu de Crohn exprimaient des niveaux plus élevés de CD38, une enzyme de la surface cellulaire qui consomme le NAD+, carburant central de la production d’énergie mitochondriale. Les gènes impliqués dans la phosphorylation oxydative mitochondriale — la principale voie par laquelle les cellules génèrent l’ATP à partir des nutriments — étaient largement régulés à la baisse dans le tissu colique des patients atteints de Crohn, et les profils métabolites plasmatiques étaient compatibles avec un déplacement loin d’une respiration mitochondriale efficace. Dans des expériences ex vivo, les plasmocytes dérivés de patients de Crohn consommaient peu de glucose, libéraient moins de lactate et présentaient une expression réduite des gènes d’énergie mitochondriale, indiquant un état métabolique « quiescent » ou affaibli. 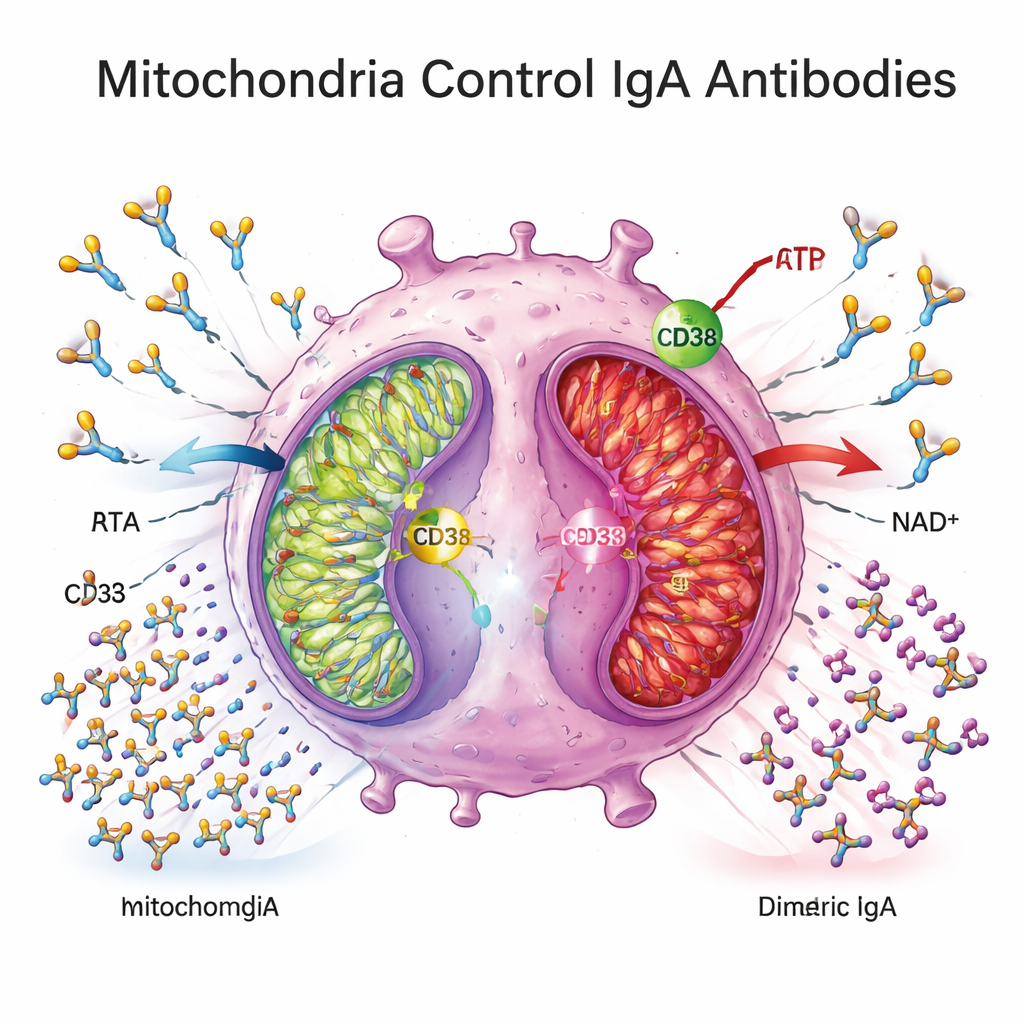
Indices venant des modèles murins et de l’alimentation
Les modèles murins apportent un soutien supplémentaire. Des souris porteuses d’une mutation mitochondriale définie qui altère le complexe V producteur d’ATP avaient moins de plasmocytes matures dans les tissus lymphoïdes associés à l’intestin, une expression réduite des marqueurs de plasmocytes dans le côlon et des niveaux plus faibles d’IgA monomérique et dimérique dans le tissu colique. À l’inverse, des souris saines nourries avec un régime sans glucose et riche en protéines, qui stimule l’activité mitochondriale dans le côlon, développaient davantage de cellules productrices d’IgA et une quantité accrue d’IgA fécale. Ces expériences complémentaires lient directement la performance mitochondriale à la capacité des plasmocytes à mûrir et à maintenir une barrière d’IgA robuste dans l’intestin.
Ce que cela signifie pour les personnes atteintes de la maladie de Crohn
Pris ensemble, les résultats dressent le tableau d’une maladie de Crohn qui, même en rémission clinique, s’accompagne d’une surabondance de cellules de la lignée B immatures dans le côlon et d’une pénurie de plasmocytes pleinement matures, énergétiquement exigeants, qui sécrètent l’IgA dimérique dans le mucus. L’intestin peut sembler calme, mais son bouclier d’anticorps est plus mince et moins efficace. En reliant ce défaut à une dysfonction mitochondriale — possiblement en partie provoquée par une activité CD38 accrue — l’étude suggère que des thérapies visant à restaurer le métabolisme énergétique cellulaire ou à ajuster la signalisation de CD38 pourraient aider à reconstruire la barrière d’IgA mucosale. Pour les patients, cela ouvre la perspective que des traitements futurs pourraient non seulement supprimer l’inflammation lorsqu’elle survient, mais aussi renforcer les défenses antérieures du tube digestif pour prévenir l’apparition des poussées.
Citation: Raschdorf, A., de Almeida, L.N., Solbach, P. et al. Colonic spatial single-cell proteomics and murine models link mitochondrial dysfunction to dimeric IgA-secreting plasma cell deficiency in Crohn’s disease. Nat Commun 17, 1590 (2026). https://doi.org/10.1038/s41467-026-69069-w
Mots-clés: Maladie de Crohn, anticorps intestinaux, IgA, mitochondries, immunité intestinale