Clear Sky Science · fr
Des myofibroblastes Tenascine C+ aggravent l’hyperplasie néointimale vasculaire en propageant les interactions nerf-macrophage chez la souris
Quand les vaisseaux sanguins se réparent de la mauvaise façon
Les interventions qui rouvrent des artères obstruées, comme l’angioplastie et le pontage, sauvent d’innombrables vies. Pourtant, elles laissent souvent un problème caché : avec le temps, le vaisseau traité peut cicatriser vers l’intérieur, se rétrécissant à nouveau et exposant de nouveau le patient au risque. Cette étude chez la souris révèle une conversation à trois surprenante entre cellules de soutien, nerfs et cellules immunitaires dans la paroi vasculaire qui alimente ce sur‑réparage néfaste, et met en lumière une molécule appelée tenascine C comme cible prometteuse pour rompre ce cycle.
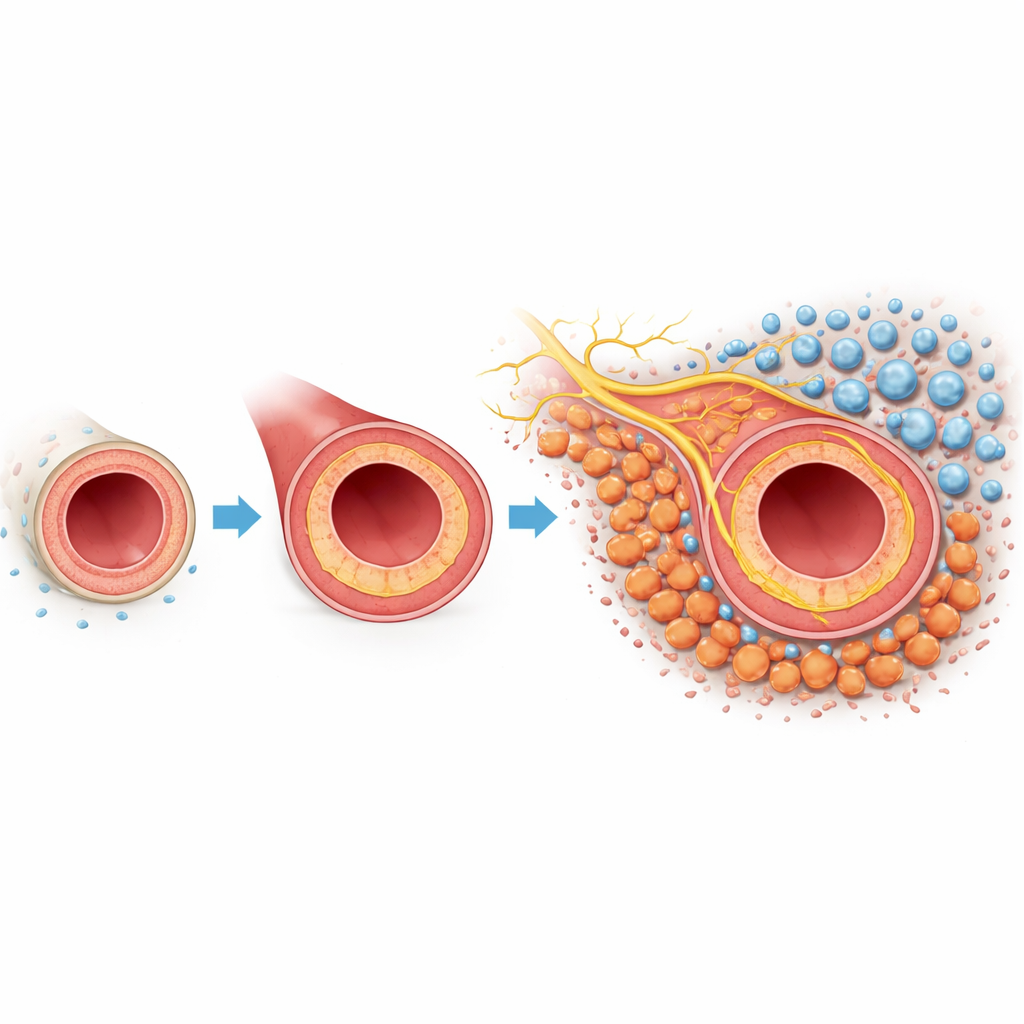
Un examen plus précis de la cicatrisation problématique des artères
Lorsqu’une artère est blessée ou manipulée pendant une opération, son revêtement intérieur peut repousser de façon trop agressive. Cette croissance vers l’intérieur, appelée hyperplasie néointimale, épaissit la paroi du vaisseau et rétrécit le canal de circulation sanguine. La couche la plus externe du vaisseau, l’adventice, contient des fibroblastes : des cellules de soutien qui maintiennent normalement la structure vasculaire. Dans ce modèle murin, où l’artère carotide a été partiellement ligaturée pour imiter une lésion, les chercheurs ont utilisé le profilage génétique unicellulaire et la cartographie spatiale pour recenser chaque type cellulaire majeur impliqué. Ils ont constaté que les fibroblastes étaient particulièrement abondants et modifiaient profondément leur comportement après la blessure, laissant penser que ces cellules pourraient jouer un rôle central dans la réponse cicatricielle.
L’émergence de cellules productrices de cicatrice riches en tenascine C
En plongeant plus profondément dans la population de fibroblastes, l’équipe a découvert un sous‑ensemble distinct n’apparaissant qu’après la lésion. Ces cellules portaient les caractéristiques de myofibroblastes : de hauts niveaux de la protéine contractile actine α-lisse et un autre marqueur nommé périostine — signes qu’elles étaient passées en mode formation de cicatrice. De façon cruciale, ce sous‑ensemble produisait aussi de grandes quantités de tenascine C, une protéine de matrice normalement rare dans les tissus adultes sains mais abondante en cas de maladie et de réparation tissulaire. Des expériences en laboratoire ont montré qu’exposer des fibroblastes adventitiels normaux au facteur de croissance transformant bêta ou à un excès de tenascine C les poussait à devenir ces myofibroblastes Tenascine C‑positifs. Les cellules sécrétaient alors encore plus de tenascine C, créant une boucle d’auto‑renforcement via une paire spécifique de récepteurs de surface, l’intégrine αvβ1, qui élargissait progressivement la population formatrice de cicatrice.
Les nerfs et les cellules immunitaires investissent le quartier
L’histoire ne s’est pas arrêtée à la formation de cicatrice. Grâce à l’imagerie 3D en montage entier et à la transcriptomique spatiale, les chercheurs ont observé que les myofibroblastes riches en tenascine C se regroupaient près des fibres nerveuses en bourgeonnement et des cellules immunitaires appelées macrophages dans la couche externe du vaisseau. Les artères lésées présentaient des nerfs sensoriels denses et emmêlés et davantage de structures de type synaptique que la normale, tant chez la souris que dans des échantillons d’artères humaines atteintes d’hyperplasie néointimale. Les macrophages dans ces zones affichaient une signature inflammatoire, produisant des molécules telles que IL‑1β et TGF‑β1, qui peuvent alimenter davantage la cicatrisation. Ensemble, les données dessinaient le portrait d’un microenvironnement réorganisé dans lequel cellules formatrices de cicatrice, nerfs et macrophages s’entremêlent physiquement et s’influencent mutuellement.
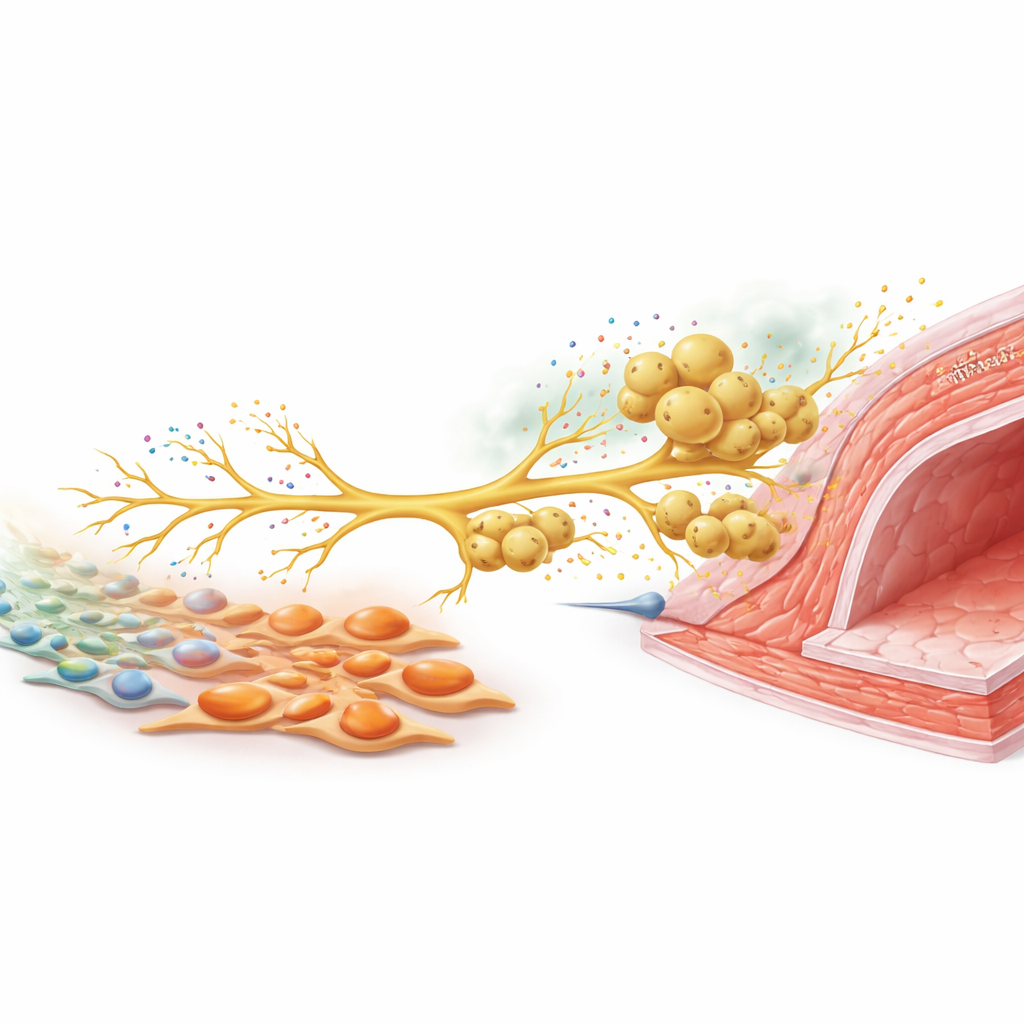
Un signal nerveux qui appelle davantage de défenseurs
Pour comprendre comment ces types cellulaires communiquent, l’équipe s’est concentrée sur les nerfs sensoriels qui détectent les stimuli dommageables. En culture, les myofibroblastes riches en tenascine C ont favorisé la croissance des fibres nerveuses issues de ganglions spinaux dorsaux. Chez les souris blessées, ces neurones sensoriels augmentaient la production de CCL2, un signal chimique bien connu pour attirer les macrophages. Lorsque neurones et macrophages étaient cultivés ensemble, les macrophages migraient le long des fibres nerveuses en croissance, comme ils le faisaient autour des artères in vivo. Silencer CCL2 dans les neurones réduisait fortement le recrutement des macrophages. Chez l’animal, diminuer l’activité des nerfs sensoriels par une toxine, ou supprimer sélectivement la tenascine C uniquement dans les fibroblastes, abaissait toutes deux la densité nerveuse, les niveaux de CCL2, l’accumulation de macrophages et, in fine, l’épaississement de la paroi vasculaire. Combiner les deux interventions n’apportait pas de bénéfice supplémentaire, suggérant qu’elles agissent dans la même voie.
Pourquoi cette nouvelle voie est importante
Pris ensemble, les résultats révèlent un cercle vicieux : la lésion incite les fibroblastes à devenir des myofibroblastes producteurs de tenascine C ; ces cellules remodelent la matrice et stimulent les nerfs sensoriels ; les nerfs activés libèrent CCL2, qui attire les macrophages ; et les macrophages sécrètent des facteurs inflammatoires et fibrosants qui aggravent la cicatrisation et rétrécissent l’artère. En identifiant la tenascine C et son axe nerveux–macrophage en aval comme moteurs centraux de cette boucle, ce travail suggère que des traitements ciblant cette molécule ou ses partenaires de signalisation pourraient aider à maintenir les artères réparées ouvertes plus longtemps, offrant aux patients une protection plus durable après des procédures cardiovasculaires.
Citation: Tong, X., Shi, G., Fang, Z. et al. Tenascin C+ myofibroblasts exacerbate vascular neointimal hyperplasia by propagation of nerve-macrophage interactions in mice. Nat Commun 17, 2199 (2026). https://doi.org/10.1038/s41467-026-69062-3
Mots-clés: hyperplasie néointimale, tenascine C, remodelage vasculaire, nerfs sensoriels, inflammation macrophagique