Clear Sky Science · fr
Le paclitaxel favorise l’expansion des macrophages TREM2+ expliquant son efficacité thérapeutique inférieure par rapport au nab‑paclitaxel
Pourquoi cette étude est importante
De nombreuses femmes atteintes d’un cancer du sein reçoivent des chimiothérapies appelées taxanes, le plus souvent le paclitaxel ou une version plus récente liée à de petites particules d’albumine, appelée nab‑paclitaxel. Les cliniciens soupçonnaient depuis longtemps que le médicament plus récent fonctionne souvent mieux, sans que les raisons soient claires. Cette étude explore des données de patientes et des expériences animales pour montrer que le paclitaxel standard peut, de façon involontaire, favoriser la dissémination du cancer vers les poumons en remodelant les cellules immunitaires de l’organisme, et elle identifie une voie pour bloquer cet effet indésirable.
Deux médicaments semblables, deux issues différentes
Les chercheurs ont d’abord comparé l’efficacité réelle du paclitaxel et du nab‑paclitaxel chez des milliers de femmes atteintes d’un cancer du sein. En regroupant les résultats de 17 études cliniques portant sur 6 486 patientes, ils ont constaté que le nab‑paclitaxel entraînait des taux de réduction tumorale plus élevés et plus de disparitions complètes de la tumeur dans le sein et les ganglions voisins avant la chirurgie. Cet avantage était particulièrement marqué chez les patientes traitées après l’échec de thérapies antérieures. Pourtant, les deux médicaments étaient administrés à des doses similaires et sont conçus pour cibler les cellules cancéreuses en division de façon comparable, ce qui suggère qu’un mécanisme autre que la simple destruction tumorale directe explique la différence.
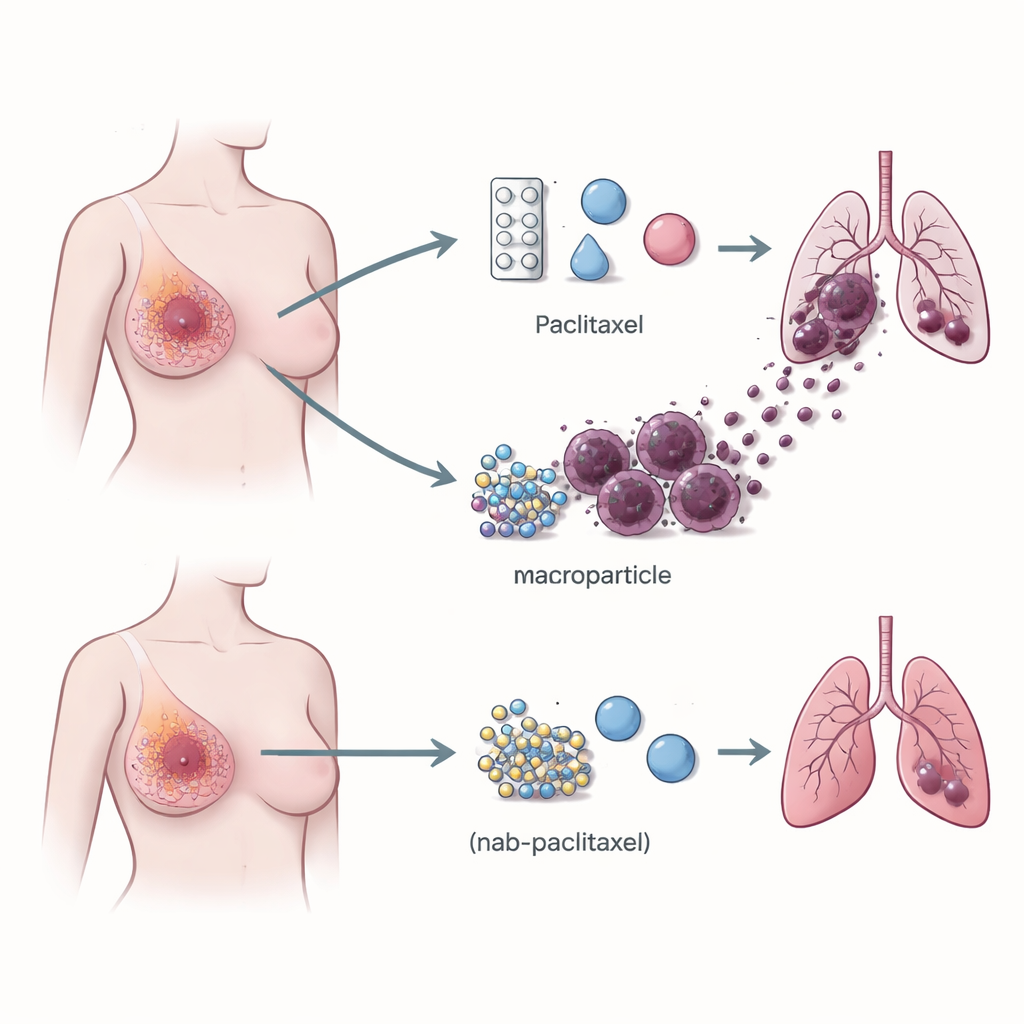
Des cellules immunitaires qui favorisent la dissémination
L’attention s’est portée sur le microenvironnement immunitaire de la tumeur — l’ensemble des globules blancs qui peuvent soit combattre le cancer soit, assez souvent, contribuer à sa progression. À l’aide du séquençage d’ARN unicellulaire, qui mesure l’activité des gènes dans des milliers de cellules individuelles, l’équipe a comparé des tumeurs de patientes traitées par paclitaxel ou par nab‑paclitaxel. Ils ont observé que les tumeurs traitées par paclitaxel contenaient beaucoup plus de macrophages portant à leur surface un récepteur appelé TREM2. Ces macrophages TREM2‑positifs se concentraient aux bords des tumeurs et étaient beaucoup plus abondants chez les patientes qui ont ensuite développé des métastases pulmonaires que chez celles dont le cancer est resté localisé. Ce schéma a été confirmé dans des cohortes plus larges et dans des modèles murins, établissant un lien solide entre ce type de macrophages et le risque de dissémination.
Quand le traitement réduit la tumeur mais favorise la propagation
Chez la souris porteuse de tumeurs mammaires, le paclitaxel a fait ce qu’on attend : il a ralenti ou réduit la tumeur primaire. Mais en même temps, il a augmenté le nombre de foyers tumoraux dans les poumons et a accru la proportion de macrophages TREM2‑positifs dans les tumeurs et la circulation sanguine. Le nab‑paclitaxel, en revanche, réduisait la taille tumorale sans favoriser les métastases pulmonaires ni l’expansion de ces macrophages, alors même qu’il était tout aussi efficace pour diminuer la tumeur principale. Lorsque le gène codant TREM2 était supprimé chez la souris, ou lorsque TREM2 était diminué par des oligonucléotides antisens (courtes séquences d’ADN qui silencient des gènes spécifiques), le paclitaxel conservait son effet réducteur sur la tumeur primaire mais perdait en grande partie sa capacité à favoriser la dissémination pulmonaire. Cela montre que les macrophages porteurs de TREM2 ne sont pas de simples témoins ; ils sont des acteurs nécessaires de la promotion des métastases induite par le paclitaxel.
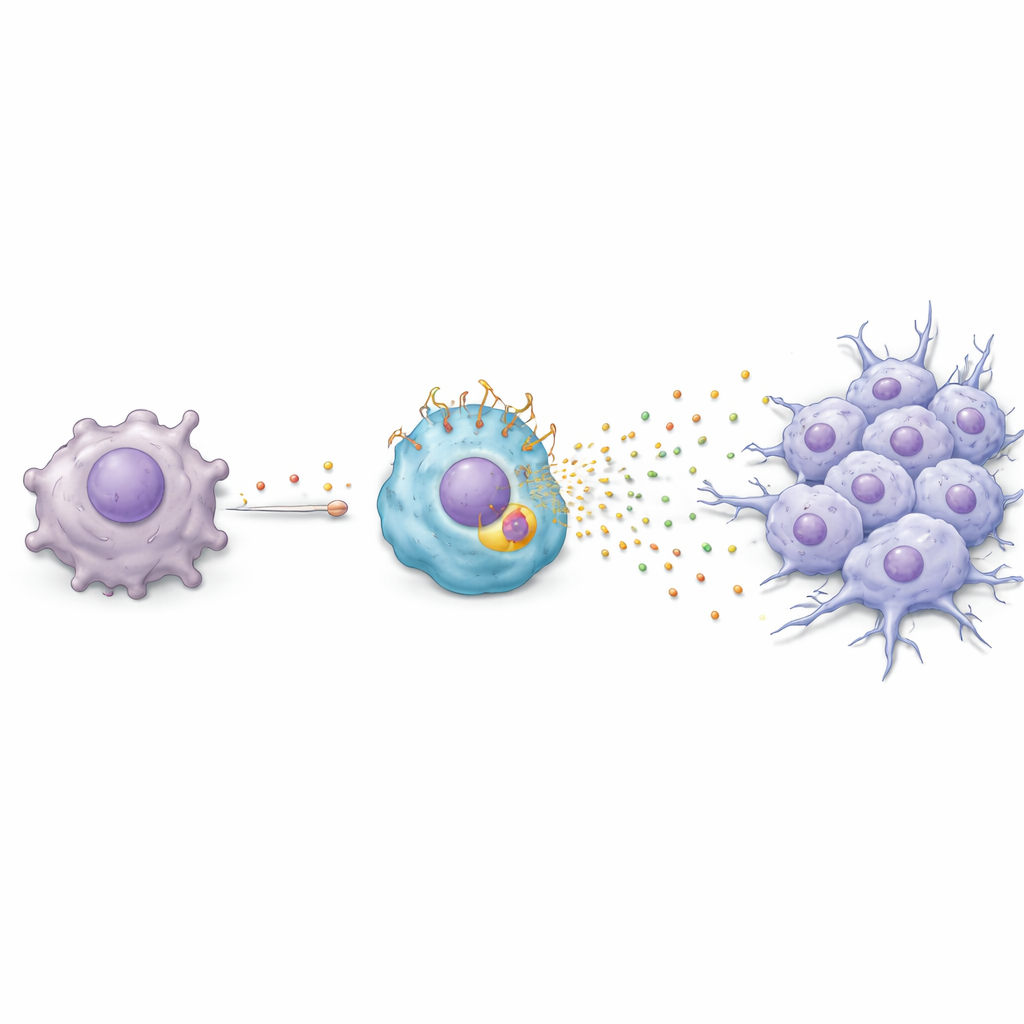
Une réaction en chaîne chimique de la tumeur à la cellule immunitaire
L’équipe a ensuite cherché comment le paclitaxel pousse les macrophages à adopter cet état riche en TREM2 néfaste. Ils ont découvert une chaîne d’événements : le paclitaxel incite les cellules cancéreuses à activer un gène de réponse au stress appelé ATF3, qui augmente ensuite la production d’un facteur de croissance nommé FGF2. Les cellules cancéreuses libèrent alors FGF2 dans leur environnement, où il agit sur les macrophages voisins. Dans ces macrophages, FGF2 active un autre régulateur, EGR1, qui élève les niveaux de TREM2. Une fois TREM2 élevé, les macrophages commencent à sécréter un mélange de protéines — notamment Serpin E1, HGF, CCL3 et CXCL2 — qui poussent les cellules cancéreuses vers un état plus mobile et invasif, appelé transition épithélio‑mésenchymateuse. In vitro et chez la souris, ce dialogue chimique rendait les cellules tumorales plus susceptibles de migrer et d’envahir, des étapes clés sur la voie des métastases.
Transformer une arme à double tranchant en outil plus sûr
En termes compréhensibles, le message principal est que le paclitaxel peut agir comme une arme à double tranchant : s’il attaque les tumeurs, il ordonne aussi à certaines cellules immunitaires d’aider le cancer à s’échapper vers des organes distants. Le nab‑paclitaxel semble éviter de déclencher cette dérive immunitaire particulière. La bonne nouvelle est que bloquer TREM2 — ou des maillons de la chaîne de signalisation FGF2–EGR1–TREM2 — permet de séparer les bénéfices antitumoraux du paclitaxel de ses risques de promotion des métastases dans des modèles animaux. Si des stratégies similaires se révèlent sûres et efficaces chez l’humain, les cliniciens pourraient continuer d’utiliser un médicament de chimiothérapie familier et largement disponible tout en réduisant sa tendance à favoriser la dissémination du cancer, ce qui améliorerait les résultats à long terme pour les patientes.
Citation: Xing, Y., Zhong, R., Li, Q. et al. Paclitaxel drives TREM2+ macrophage expansion underlying its inferior therapeutic efficacy compared to Nab-paclitaxel. Nat Commun 17, 2272 (2026). https://doi.org/10.1038/s41467-026-69060-5
Mots-clés: cancer du sein, paclitaxel, microenvironnement tumoral, macrophages, métastase