Clear Sky Science · fr
Réutilisation fiable de l’interactome des anticorps à l’intérieur de la cellule
Transformer les anticorps en petits outils à l’intérieur de nos cellules
Les anticorps sont connus comme les armes de précision du sang, ciblant virus et autres menaces. Mais l’essentiel de l’activité dans de nombreuses maladies, y compris Alzheimer, Parkinson et certains cancers, se déroule à l’intérieur des cellules, où les anticorps classiques atteignent rarement leur cible ou ne fonctionnent pas bien. Cette étude montre comment reconstruire systématiquement des anticorps existants en « intrabodies » plus petits qui fonctionnent de manière fiable à l’intérieur de cellules humaines vivantes, ouvrant la voie à de nouveaux diagnostics, outils de recherche et potentiellement à des thérapies futures opérant directement au cœur des processus pathologiques.
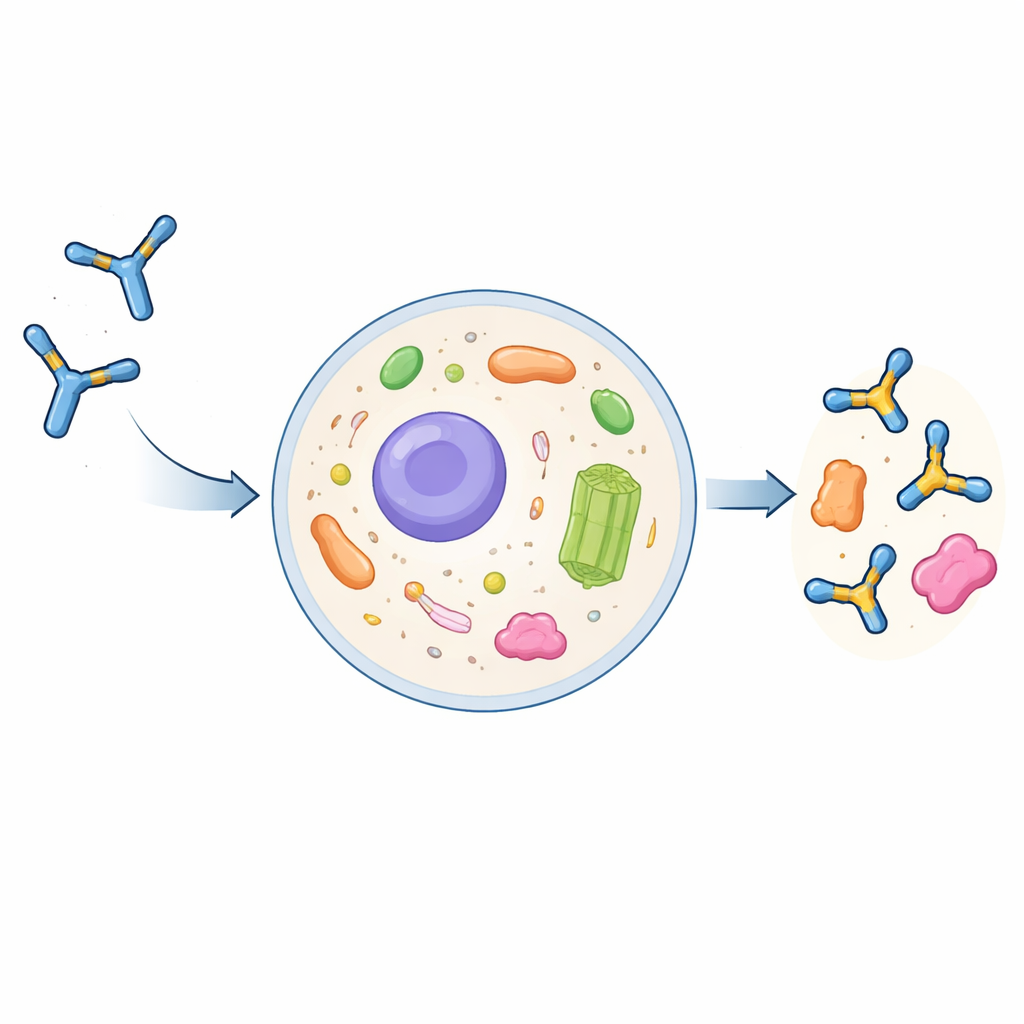
Pourquoi les anticorps classiques peinent à l’intérieur des cellules
Les anticorps de taille complète sont de grandes protéines en forme de Y, évoluées pour agir à l’extérieur des cellules. Ils sont assemblés et modifiés chimiquement dans la voie sécrétoire de la cellule puis relâchés dans la circulation. S’ils sont repris par les cellules, ils sont généralement envoyés vers des compartiments de dégradation plutôt que dans le liquide intérieur de la cellule, le cytoplasme. Les scientifiques peuvent réduire les anticorps à leurs parties de reconnaissance essentielles, appelées fragments variables monocaténaires (scFv), et exprimer ces fragments comme intrabodies à l’intérieur des cellules. Cependant, ces intrabodies s’agrègent souvent, deviennent insolubles et perdent leur capacité à reconnaître leur cible. Jusqu’à présent, il n’existait pas de recette générale et fiable pour transformer un anticorps conventionnel en un intrabody bien comporté.
Déterminer les règles de conception pour des intrabodies solubles
Les chercheurs ont commencé par mesurer la capacité de 45 intrabodies différents à rester dissous lorsqu’ils sont produits dans des cellules humaines. Ils ont comparé de manière systématique de nombreuses caractéristiques protéiques — telles que l’hydrophobicité globale, la qualité de structure prédite et les propriétés des boucles de liaison — pour déterminer lesquelles expliquaient le mieux si un intrabody restait soluble. Un facteur simple s’est distingué : la charge électrique nette à un pH proche de la physiologie. Les intrabodies à charge nette fortement négative étaient beaucoup plus susceptibles de rester solubles, alors que ceux à charge neutre ou positive avaient tendance à s’agréger. D’autres prédicteurs sophistiqués, y compris les scores de confiance structurelle issus d’AlphaFold, ne corrélaient pas avec la solubilité. Cela a permis à l’équipe de construire un modèle pratique basé sur la charge capable d’estimer quelle fraction d’un intrabody se trouvera dans la fraction soluble d’un extrait cellulaire.
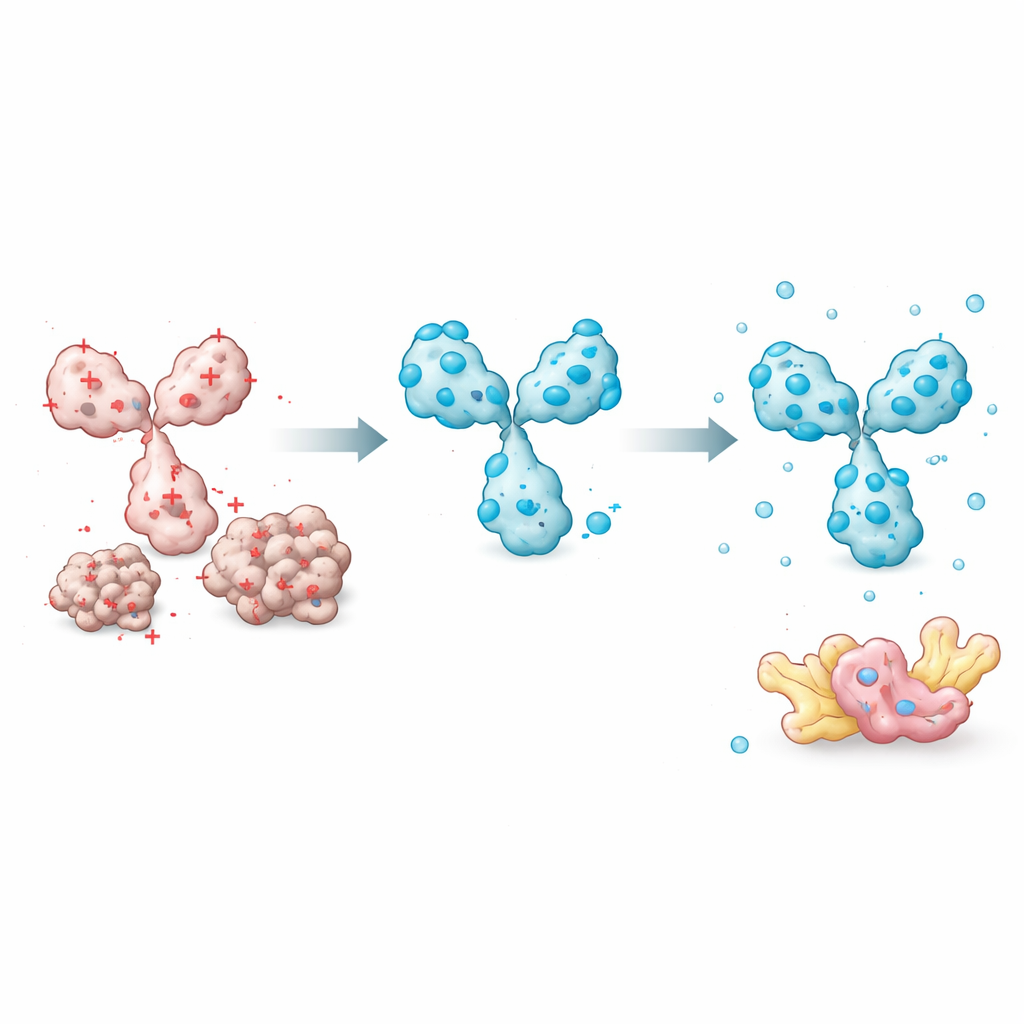
Réingénierie des linkers et domaines pour un meilleur comportement
Armés de cette connaissance, les auteurs se sont concentrés sur des éléments qu’ils pouvaient facilement ajuster sans perturber la reconnaissance de la cible par l’intrabody. Un élément clé est le court peptide « linker » qui relie les deux domaines variables. La plupart des conceptions existantes utilisent des linkers neutres qui n’altèrent pas la charge. En remplaçant ces positions par des acides aminés chargés négativement, les chercheurs ont pu abaisser la charge globale de l’intrabody, améliorant drastiquement la solubilité tout en préservant la reconnaissance de la cible. Ils ont aussi découvert que l’ordre des domaines variables (si la partie lourde ou la partie légère vient en premier) et des positions spécifiques du cadre en dehors des boucles de liaison influencent la facilité de repliement et la solubilité de la protéine. Choisir un ordre de domaines qui protège les régions les plus fragiles et introduire des mutations d’échange de charge placées avec soin a encore renforcé les performances.
Utiliser l’intelligence artificielle pour concevoir des intrabodies à grande échelle
Pour dépasser l’approche tâtonnante d’un échantillon à la fois, les auteurs ont combiné leurs règles simples de charge avec des logiciels avancés de conception protéique basés sur l’apprentissage profond. À partir d’architectures d’anticorps connues, ils ont utilisé une approche d’« inverse folding » pour proposer de nouvelles séquences qui adopteraient toujours la forme désirée mais porteraient des caractéristiques de surface — en particulier des motifs de charge — favorisant la stabilité et la solubilité. Ils ont limité les changements au niveau des boucles de liaison clés pour préserver la reconnaissance, tout en laissant l’algorithme redesigner les surfaces environnantes. Les tests ont montré que beaucoup de ces intrabodies guidés par l’IA étaient non seulement hautement solubles mais aussi plus stables thermiquement que des variantes conçues manuellement, tout en conservant la capacité à se lier à des cibles pertinentes pour la maladie comme le SOD1 mal replié, p53, α‑synucléine et d’autres protéines impliquées dans la neurodégénérescence.
Constituer une bibliothèque d’attrape‑protéines intracellulaires
En appliquant ces règles et outils à grande échelle, l’équipe a reformaté informatiquement 672 anticorps en intrabodies prédits comme efficaces à l’intérieur des cellules. Ces molécules ingénierées couvrent plus de 60 cibles intracellulaires différentes, y compris des protéines impliquées dans les maladies d’Alzheimer, de Parkinson et de Huntington, ainsi que des facteurs liés au cancer et des modifications post‑traductionnelles comme la phosphorylation et l’acétylation. Dans des expériences, des intrabodies sélectionnés ont réussi à « pêcher » des formes protéiques spécifiques liées à la maladie, telles que le SOD1 mutant ou certaines conformations d’α‑synucléine, tout en ignorant les formes normales. Toutes les séquences sont mises à disposition ouvertement, et les auteurs fournissent un outil web permettant à d’autres d’estimer la solubilité des intrabodies à partir de la séquence en utilisant le même modèle fondé sur la charge.
Ce que cela signifie pour la recherche et les médicaments futurs
Concrètement, ce travail transforme la vaste collection d’anticorps existants — dont beaucoup sont déjà étudiés en clinique — en une boîte à outils pouvant être adaptée de façon fiable pour une utilisation intracellulaire. En suivant un ensemble simple de règles de conception, les chercheurs peuvent désormais créer des intrabodies susceptibles de fonctionner dès la première tentative, économisant temps et coûts. Pour un lecteur non spécialiste, le message clé est que les scientifiques ont trouvé un moyen simple de « reconfigurer » nos meilleurs dispositifs détecteurs protéiques afin qu’ils fonctionnent dans l’intérieur encombré des cellules vivantes, où nombre de maladies prennent naissance. Cela pourrait accélérer le développement de nouvelles façons de suivre, d’étudier et éventuellement de traiter des affections causées par des protéines mal repliées ou dysfonctionnelles.
Citation: O’Shea, C.M., Shahzad, R., Aghasoleimani, K. et al. Reliable repurposing of the antibody interactome inside the cell. Nat Commun 17, 2222 (2026). https://doi.org/10.1038/s41467-026-69057-0
Mots-clés: intrabodies, ingénierie des anticorps, solubilité des protéines, maladie neurodégénérative, intelligence artificielle en biologie