Clear Sky Science · fr
Régulation de l’eau interfaciale pour le transfert d’oxygène vers des liaisons benzyliques C(sp3)–H via la covalence tungstène–oxygène activée par le nickel
Transformer l’eau et l’huile en produits chimiques utiles
Les chimistes cherchent depuis longtemps une méthode plus propre pour convertir des molécules d’origine pétrolière simples en ingrédients de plus grande valeur pour les plastiques, les médicaments et les produits du quotidien. Cette étude montre comment « régler » avec précision la mince couche d’eau en contact avec une électrode permet à l’eau ordinaire de fournir de l’oxygène à des hydrocarbures récalcitrants, réduisant ainsi les déchets et la consommation d’énergie.
Pourquoi l’oxygène provenant de l’eau est important
De nombreux produits industriels sont obtenus en ajoutant de l’oxygène à des hydrocarbures — des molécules essentiellement constituées de carbone et d’hydrogène. Aujourd’hui, cela implique souvent des oxydants puissants et des températures élevées, consommant beaucoup d’énergie et générant des émissions contribuant au réchauffement climatique. L’eau est une source d’oxygène bon marché, sûre et abondante, mais la convaincre de partager directement son oxygène avec des liaisons carbone–hydrogène robustes nécessite généralement des tensions très élevées. Dans ces conditions sévères, la plupart de l’électricité est perdue à produire du gaz oxygène par séparation de l’eau plutôt qu’à fabriquer des produits utiles.
Une électrode intelligente qui réorganise l’eau
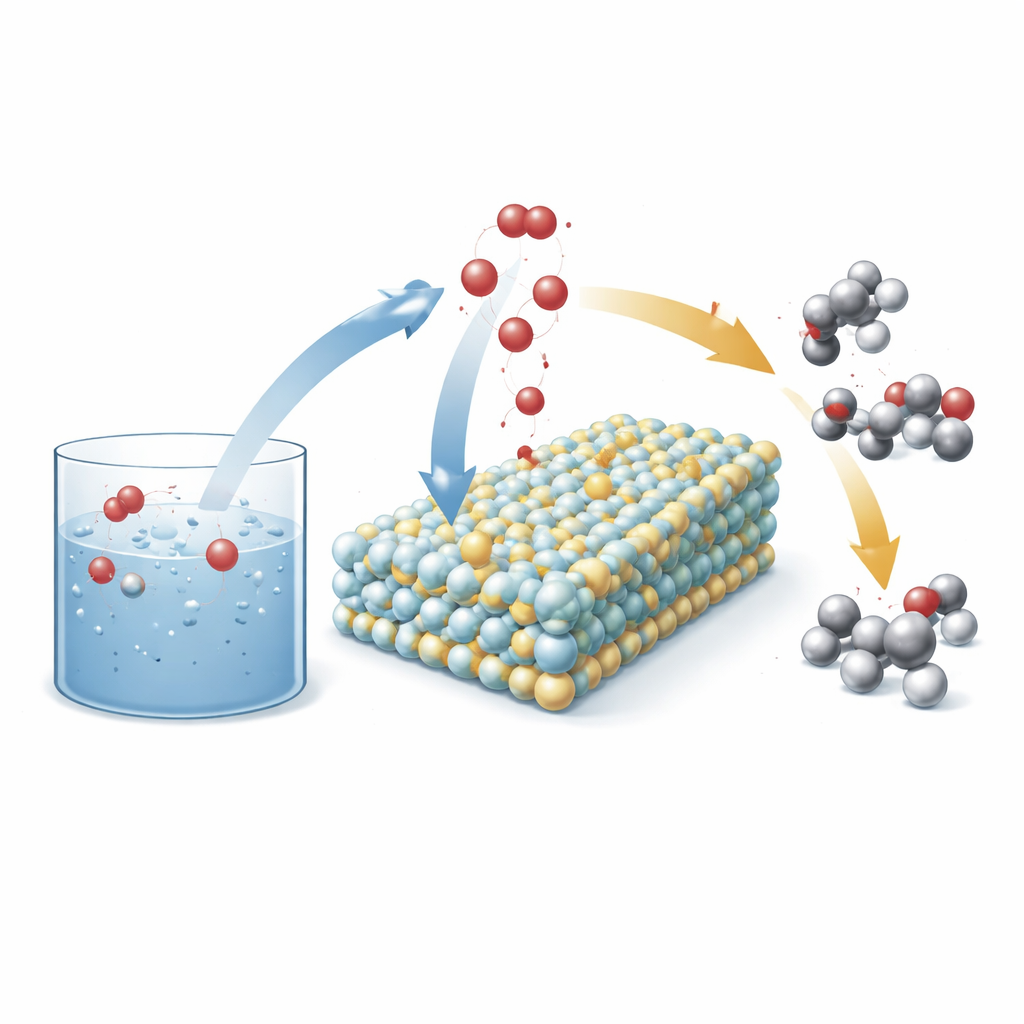
Les chercheurs ont conçu un nouveau type d’anode (l’électrode positive d’une cellule électrochimique) constitué de particules nanométriques de carbure de tungstène qui se transforment en cours d’opération en un matériau amorphe tungstène–oxygène. Dans ce réseau, ils dispersent des atomes de nickel individuels. En conditions de réaction, l’oxygène de l’eau migre dans le solide, le convertissant en une surface d’oxyde de tungstène activée par le nickel avec de nombreux sites réactifs exposés. Cette surface reconstruite sert alors de plateforme où l’eau et les molécules d’hydrocarbure se rencontrent et échangent de l’oxygène de manière contrôlée, favorisant des produits de valeur tels que des alcools et des cétones plutôt que des acides sur-oxydés et autres sous-produits.
Desserrement de la « cage » d’eau à la surface
Une découverte clé est que les atomes de nickel perturbent subtilement la façon dont les molécules d’eau s’arrangent contre l’électrode. Normalement, l’eau à la surface chargée forme un réseau dense de liaisons hydrogène, comme une maille serrée qui ralentit le mouvement. Des simulations informatiques et des mesures infrarouges sensibles montrent que près des régions dopées au nickel ce réseau devient plus lâche, avec moins de liaisons hydrogène et davantage de molécules d’eau « libres ». Cela ouvre des canaux par lesquels l’eau peut diffuser plus facilement vers les sites réactifs tungstène–oxygène. En conséquence, des fragments porteurs d’oxygène issus de l’eau peuvent atteindre la surface plus rapidement et plus souvent, alimentant la réaction au lieu de s’échapper sous forme de gaz oxygène.
Diriger l’oxygène vers les bonnes liaisons
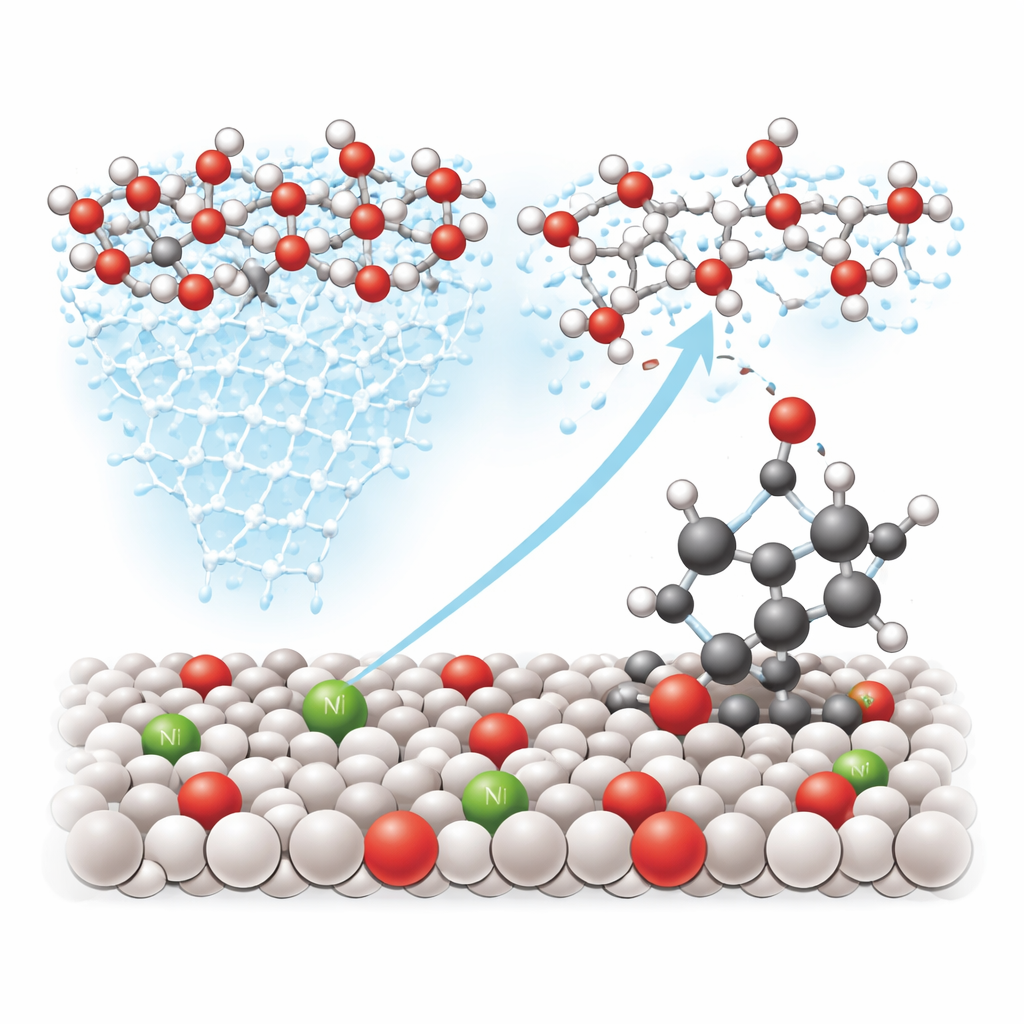
Au-delà d’améliorer la circulation à la surface, le nickel module aussi la structure électronique des atomes de tungstène voisins, rendant certains sites particulièrement aptes à capter et activer l’eau. Les expériences du groupe utilisant des isotopes — des versions marquées de l’oxygène et de l’hydrogène qui peuvent être suivies — montrent que l’oxygène actif provient d’eau fraîchement dissociée plutôt que de la matrice de l’oxyde elle‑même. Des « instantanés » spectroscopiques capturent un pont transitoire entre le tungstène, l’oxygène et le carbone benzylique sur des molécules comme l’éthylbenzène. Des calculs théoriques confirment que, sur la surface modifiée au nickel, il est plus facile pour un atome d’oxygène d’attaquer ce site carbone–hydrogène que de suivre la voie habituelle de séparation de l’eau produisant du gaz oxygène, orientant ainsi la réaction vers des produits oxygénés utiles.
Efficace, sélectif et durable
Dans les essais, l’électrode activée par le nickel convertit une gamme de liaisons carbone–hydrogène benzyliques en alcools et cétones avec des efficacités faradiques — la part de la charge électrique consacrée à la chimie désirée — typiquement supérieures à 50 %, atteignant plus de 56 % dans les cas optimisés. Le système fonctionne sur de nombreux cycles sans perte d’activité, tout en conservant sa structure nickel–tungstène. Parce qu’il utilise l’eau comme seule source d’oxygène et évite les oxydants chimiques ajoutés, il offre une efficacité énergétique compétitive et des coûts de matériaux réduits par rapport à d’autres méthodes avancées. Bien que l’application actuelle se concentre sur des sites benzyliques, le principe sous-jacent — l’usage d’additifs atomiques pour remodeler l’eau interfaciale et rediriger les voies réactionnelles — ouvre la voie à une boîte d’outils plus large pour l’oxydation plus verte, électriquement pilotée, de liaisons carbone–hydrogène autrement inertes.
Ce que cela signifie pour une chimie plus propre
Ce travail montre que de petites modifications à l’échelle atomique peuvent avoir des effets majeurs sur le comportement de l’eau à une électrode et sur la destination de son oxygène. En utilisant des atomes de nickel pour à la fois assouplir la structure de l’eau interfaciale et affiner les sites réactifs, les auteurs transforment l’eau en un donneur d’oxygène efficace pour des liaisons hydrocarbonées difficiles à activer, tout en supprimant la formation indésirable de gaz oxygène. À long terme, des stratégies de ce type pourraient contribuer à repenser la chimie d’oxydation dans l’industrie chimique, la rendant plus économe en énergie et plus respectueuse du climat en utilisant l’électricité et l’eau au lieu d’oxydants agressifs et de réactifs d’origine fossile.
Citation: Leng, BL., Lin, X., Dong, HY. et al. Regulating interfacial water for oxygen transfer to benzylic C(sp3)–H bonds via Ni-activated tungsten-oxygen covalency. Nat Commun 17, 2355 (2026). https://doi.org/10.1038/s41467-026-69054-3
Mots-clés: électrocatalyse, oxydation de l’eau, activation de C–H benzylique, oxyde de tungstène dopé au nickel, chimie verte