Clear Sky Science · fr
RNA‑Seq double in vivo révèle des effecteurs clés de la perturbation de la barrière épithéliale par un pathogène extracellulaire
Comment certains microbes contournent nos barrières cellulaires
Nos organes sont tapissés de cellules étroitement serrées qui font office de murs, retenant le sang, les microbes et les toxines là où ils doivent rester. Pourtant, certains agents pathogènes se glissent entre ces cellules et se propagent dans l’organisme. Cette étude décrit de manière détaillée comment la bactérie responsable de la leptospirose, une maladie grave et répandue dans le monde, gagne silencieusement des organes comme le foie et les reins, puis utilise une ruse impliquant le calcium intracellulaire pour forcer l’ouverture de ces barrières protectrices.
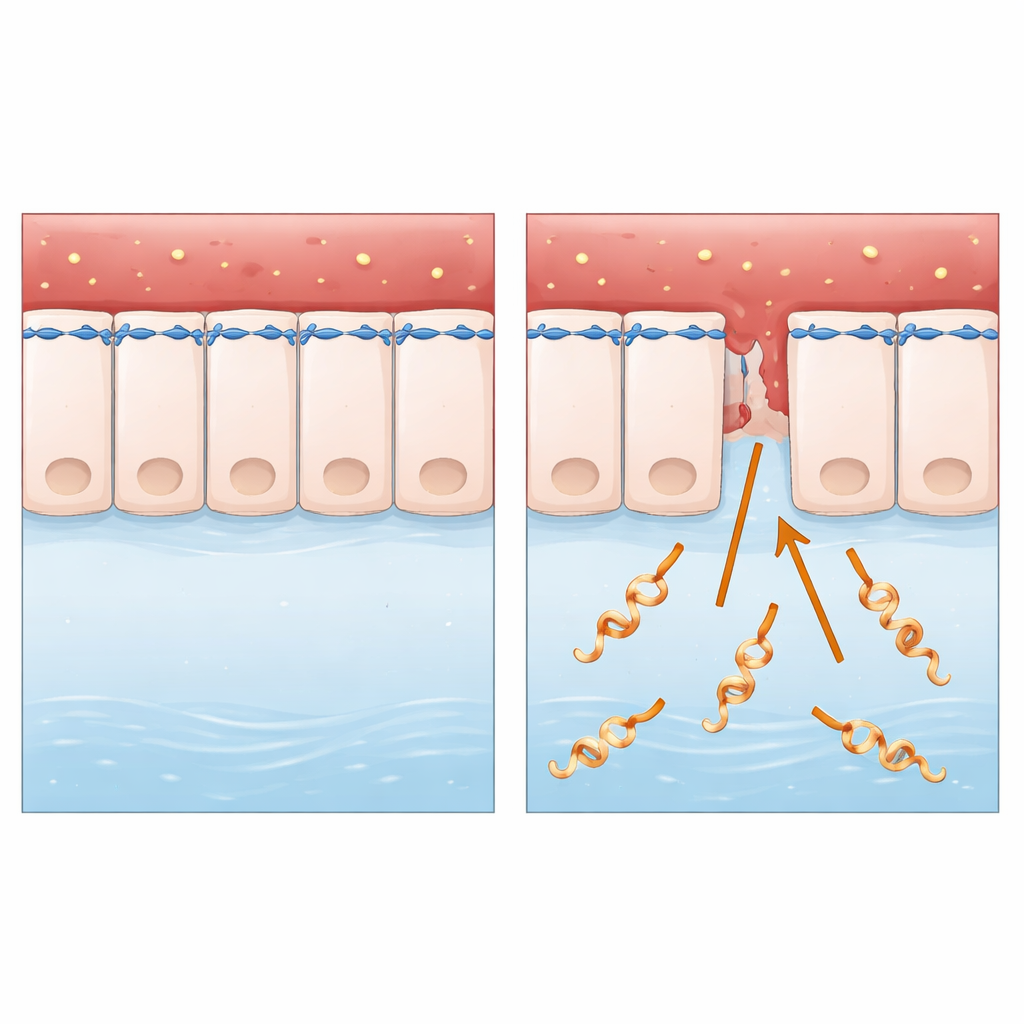
Un envahisseur discret des tissus animaux et humains
Les chercheurs se sont intéressés à Leptospira interrogans, une bactérie en forme de spirale principalement transmise des animaux à l’homme via de l’eau ou un sol contaminés. Après pénétration par de petites lésions cutanées ou les muqueuses, elle circule dans le sang et peut déclencher des formes sévères, incluant une insuffisance hépatique et rénale ainsi que des hémorragies internes. Contrairement à de nombreux microbes bien étudiés, Leptospira vit à l’extérieur des cellules et lui manquent certains « armes moléculaires » classiques que les scientifiques recherchent habituellement. Cela en faisait un modèle idéal pour poser une question fondamentale : comment une bactérie apparemment simple et extracellulaire traverse-t‑elle des couches cellulaires intactes avec autant d’efficacité ?
Observer simultanément les réponses génétiques de l’hôte et du microbe
Pour saisir le processus d’infection dans un animal vivant, l’équipe a utilisé le séquençage double d’ARN (dual RNA‑Seq) chez le hamster, modèle de leptospirose aiguë. Cette méthode permet de lire, en même temps, quels gènes de l’hôte et du pathogène sont activés ou réprimés. Les scientifiques ont infecté des hamsters et prélevé des tissus hépatiques et rénaux un et trois jours après. Au début, malgré un grand nombre de bactéries, les cellules de l’animal modifiaient à peine leur activité génique, suggérant que Leptospira échappe initialement à la détection immunitaire. Au jour 3, toutefois, les deux organes présentaient une réaction marquée, particulièrement le foie : des gènes liés à l’inflammation, aux jonctions intercellulaires et au cytosquelette étaient fortement modifiés, indiquant une restructuration active des barrières tissulaires.
Démonter la fermeture cellulaire de l’extérieur vers l’intérieur
Les couches cellulaires sont scellées par des jonctions serrées et des jonctions d’adhérence, qui relient les cellules voisines et les ancrent à un anneau d’actine et de myosine, la même paire de protéines qui permet la contraction musculaire. La microscopie sur des cellules épithéliales humaines infectées par Leptospira a montré des changements de forme, l’ouverture d’espaces entre les cellules et l’affaiblissement ou le mauvais positionnement de protéines clés des jonctions. Il est important de noter que les cellules ne mouraient pas, ce qui indique que la barrière était démantelée, non détruite. Les chercheurs ont aussi observé des signes de stress au niveau des usines de repliement des protéines des cellules, mais le blocage de ce stress ne restaura pas les jonctions, orientant les investigations vers un autre mécanisme.
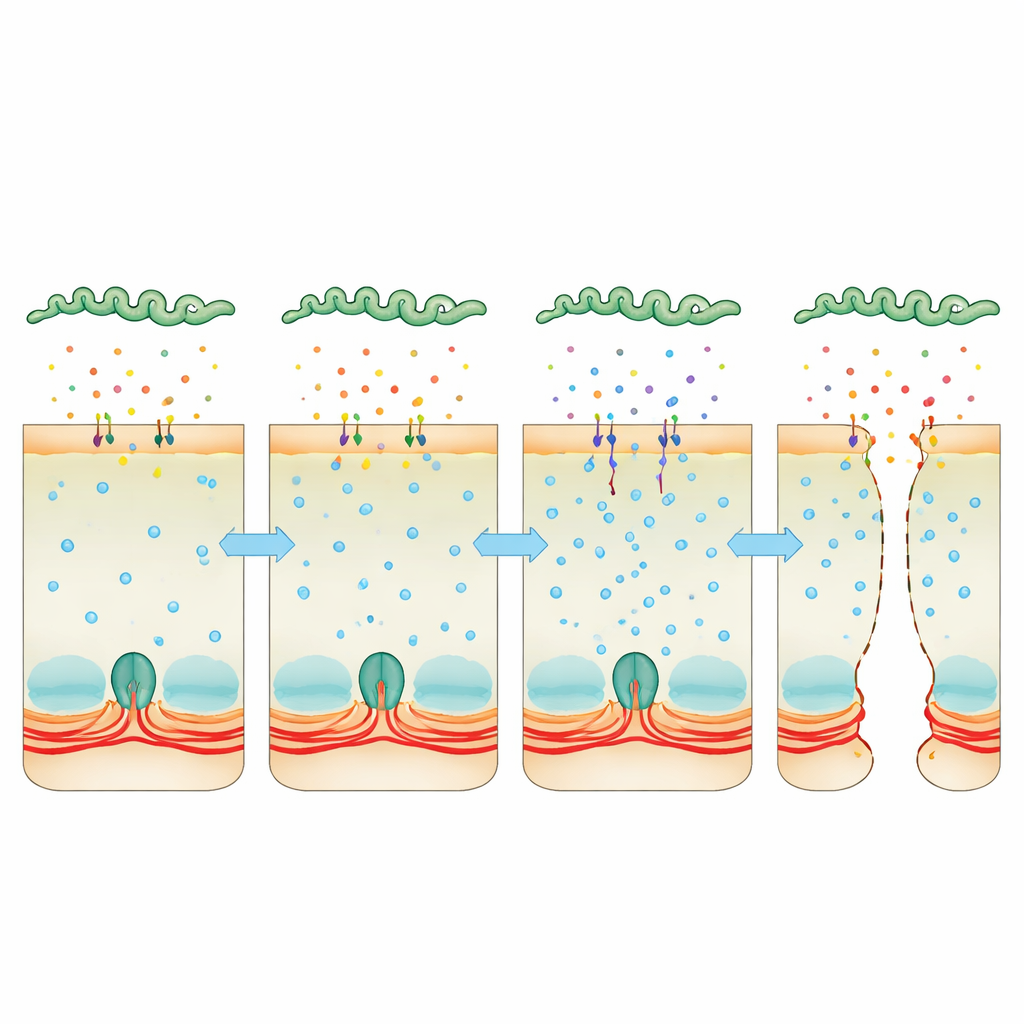
Détourner le calcium comme levier caché
L’attention s’est portée sur le calcium, signal universel intracellulaire qui peut resserrer ou relâcher l’anneau actine–myosine. Les cellules infectées accumulaient davantage de calcium, ce qui était associé à une activité augmentée de la myosine light chain kinase, une enzyme qui fait contracter l’anneau et tirer sur les jonctions. Lorsque l’équipe utilisa un composé chélatant le calcium, ou des médicaments inhibant la calmoduline ou cette kinase, les couches cellulaires restaient mieux préservées et les bactéries avaient plus de difficulté à se faufiler. Parallèlement, le séquençage profond de l’ARN bactérien révéla qu’à l’intérieur de l’hôte, Leptospira augmentait fortement la production de deux protéines « modulatrices de virulence » ressemblant à des toxines. Ces protéines sont sécrétées dans le milieu, se fixent aux cellules hôtes et sont retrouvées à l’intérieur d’elles. Lorsque les bactéries étaient dépourvues d’une ou des deux protéines, leur capacité à traverser les couches cellulaires ou à provoquer une maladie mortelle chutait fortement, et leur milieu secreté n’augmentait plus les niveaux calciques ni ne démantelait les jonctions aussi efficacement.
Conséquences pour la maladie et pistes pour la prévention
Pris ensemble, les résultats racontent une histoire cohérente. Après s’être infiltrée presque à l’insu de la surveillance, Leptospira commence à sécréter des protéines modifiant la virulence, ressemblant à des toxines. Ces protéines se lient aux cellules épithéliales et perturbent l’équilibre calcique intracellulaire, ce qui active une voie contractile qui éloigne le « zip » cellulaire maintenant les cellules voisines ensemble. À mesure que les jonctions serrées et d’adhérence se relâchent, des micro‑passages apparaissent, permettant aux bactéries de passer entre les cellules, de coloniser les organes et de déclencher des formes graves de la maladie. En identifiant ce mécanisme piloté par le calcium et les protéines bactériennes responsables, l’étude ouvre la voie à de nouvelles stratégies — par exemple bloquer ces protéines ou leur voie de signalisation — pour renforcer nos barrières cellulaires et limiter la propagation de la leptospirose et peut‑être d’autres infections exploitant des tactiques similaires.
Citation: Giraud-Gatineau, A., Haustant, G., Monot, M. et al. In vivo dual RNA-Seq uncovers key effectors of epithelial barrier disruption by an extracellular pathogen. Nat Commun 17, 2274 (2026). https://doi.org/10.1038/s41467-026-69033-8
Mots-clés: leptospirose, barrière épithéliale, signalisation calcique, toxines bactériennes, interactions hôte–pathogène