Clear Sky Science · fr
La nDIA-MS optimisée par superchargement permet le profilage global des variations de solubilité du protéome induites par des médicaments
Pourquoi le comportement des protéines compte au-delà des simples quantités
Les médicaments peuvent modifier non seulement la quantité d’une protéine produite par une cellule, mais aussi sa localisation et son état — qu’elle soit libre ou agrégée sur des structures cellulaires. Ces changements de « où » et « comment » les protéines existent dans la cellule sont étroitement liés à des maladies comme le cancer ou les pathologies neurodégénératives, mais ils sont difficiles à mesurer à grande échelle. Cette étude présente une méthode rapide et puissante pour analyser des milliers de protéines humaines simultanément afin d’observer comment leur solubilité — qu’elles soient dans un état libre ou plus fixé — évolue lorsque les cellules sont exposées à deux médicaments expérimentaux largement utilisés.
Une manière plus rapide et plus nette d’observer les protéines
Les auteurs s’appuient sur une technologie centrale de la biologie moderne : la spectrométrie de masse, une technique qui pèse et quantifie des fragments protéiques. Les méthodes standard excellent déjà pour mesurer la quantité de chaque protéine présente, mais peinent à révéler des changements d’état protéique, par exemple le passage sur l’ADN ou l’intégration dans des assemblages denses. Ici, les chercheurs affinent une version appelée acquisition indépendante des données à fenêtre étroite (nDIA-MS). En ajoutant de petits auxiliaires chimiques, dits agents de superchargement, au liquide qui transporte les peptides dans l’appareil, ils augmentent les charges électriques de ces fragments et renforcent considérablement le signal.
Après avoir testé deux additifs de superchargement courants, le diméthylsulfoxyde (DMSO) et l’alcool m-nitrobenzyl (mNBA), ils constatent que 3 % de DMSO procure l’augmentation de signal globale la plus importante et le plus grand nombre de protéines détectées, tandis que le mNBA est meilleur pour accroître le nombre et la charge des fragments peptidiques individuels. Avec le protocole optimisé, l’équipe peut identifier environ 9 600 protéines humaines à partir d’un seul microgramme d’un digest cellulaire standard en une course de 15 minutes — une combinaison remarquable de rapidité et de profondeur pour des expériences de routine. Cette performance prépare le terrain pour utiliser la nDIA-MS non seulement pour compter les protéines, mais aussi pour sonder comment leur état physique réagit au stress.
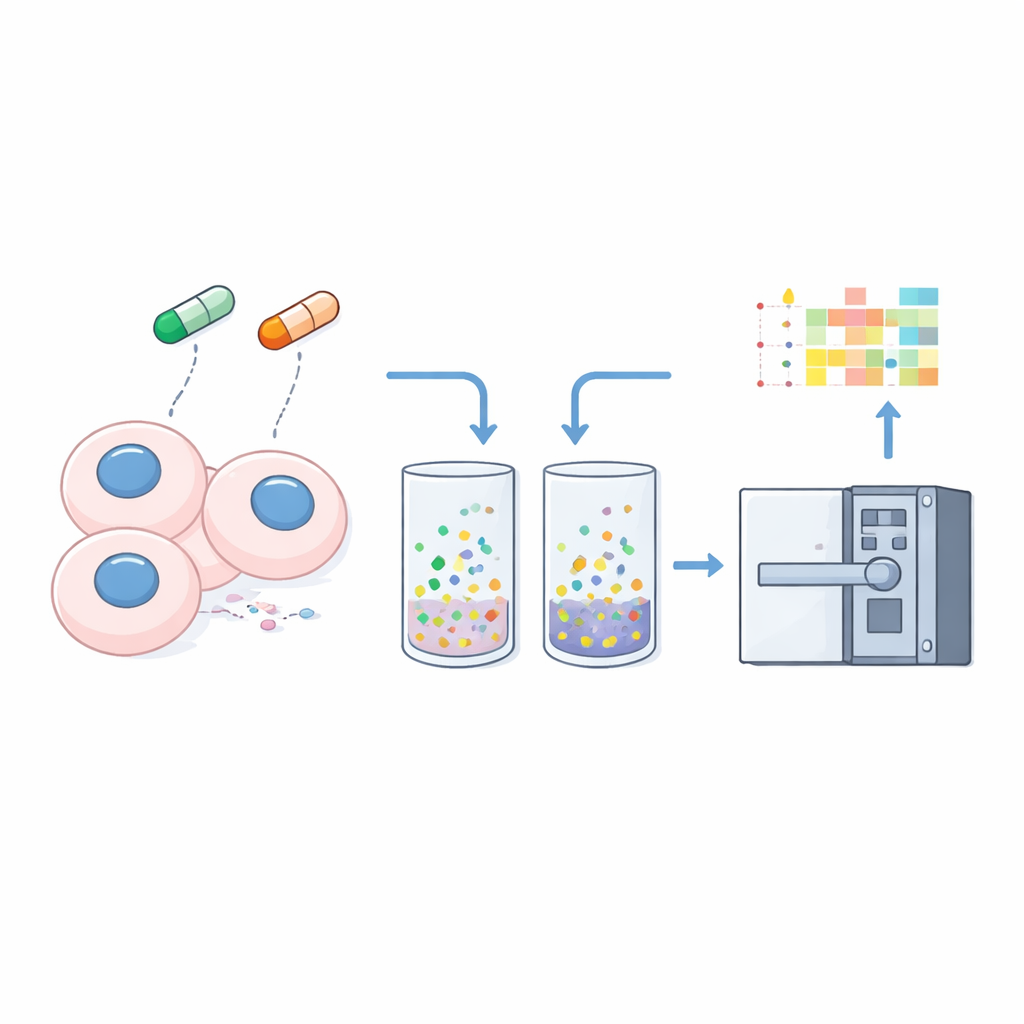
Transformer la solubilité en indicateur de changement cellulaire
Pour transformer la solubilité en signal mesurable, les chercheurs prétraitent doucement les cellules avec un détergent léger qui extrait les protéines librement solubles, laissant un matériel lié de manière serrée à l’ADN, aux membranes ou à d’autres structures. Ils analysent à la fois le lysat total et ce culot « insoluble » provenant de trois lignées cellulaires cancéreuses en utilisant la méthode nDIA-MS optimisée. En comparant l’abondance de chaque protéine dans le culot par rapport à l’échantillon total, ils calculent un simple « ratio d’insolubilité » — des valeurs plus élevées suggèrent une association plus forte aux structures cellulaires, des valeurs plus faibles indiquent un état plus soluble et libre.
L’équipe expose ensuite les cellules pendant seulement une heure à deux médicaments : le MG132, un bloqueur du protéasome qui empêche la dégradation des protéines indésirables, et le ML‑792, un inhibiteur de l’activation de la SUMO qui interfère avec un système clé d’étiquetage des protéines. Cette exposition courte est volontaire ; elle vise à capturer des déplacements rapides et précoces du comportement protéique avant que les changements d’expression génique ne prennent pleinement effet. Même dans cette fenêtre brève, ils peuvent quantifier les variations de solubilité et d’abondance pour 8 694 protéines et confirmer que leur fractionnement sépare nettement les protéines classiquement solubles, comme la tubuline, des protéines liées à la chromatine, comme les histones.
Des médicaments qui remodèlent le paysage protéique cellulaire
MG132 et ML‑792 entraînent un remodelage étendu mais distinct de la solubilité des protéines. MG132 rend plus de mille protéines plus insolubles et plus de six cents plus solubles à travers les trois lignées cellulaires. De nombreuses protéines affectées se situent au carrefour du contrôle de qualité protéique, de la réponse aux dommages de l’ADN, de la régulation génique et de l’autophagie — le système d’auto-nettoyage de la cellule. Par exemple, des composants du complexe activateur du protéasome et des adaptateurs aidant à marquer les protéines défectueuses deviennent moins solubles, ce qui suggère que lorsque la dégradation est bloquée, des facteurs clés du contrôle qualité se retrouvent eux-mêmes piégés sur des structures telles que la chromatine ou les membranes cellulaires. Les protéines d’autophagie et les acteurs de la réponse aux dommages, y compris le régulateur du stress HSF1, se déplacent aussi vers des états plus insolubles, de type condensat, cohérents avec la formation de corps de stress nucléaires.
ML‑792, en revanche, cible fortement les protéines impliquées dans la transcription et le système SUMO lui‑même. Des centaines de protéines deviennent soit plus insolubles soit plus solubles lorsque l’activation de la SUMO est bloquée, et les protéines SUMO centrales migrent vers le pool soluble, comme attendu. L’étude met en évidence des comportements marquants : des sous‑unités de l’ARN polymérase III deviennent plus insolubles, suggérant un changement d’import nucléaire ou d’attachement à la chromatine ; des répresseurs clés associés aux corps nucléaires, tels que SP100 et DAXX, deviennent plus solubles, indiquant que les marques SUMO contribuent à les séquestrer dans ces compartiments. Lorsque les deux médicaments sont appliqués seuls ou en séquence, certaines protéines, dont NAB2, SMAD2 et RB1, montrent des variations de solubilité coordonnées voire opposées, révélant une interaction nuancée entre les systèmes d’étiquetage ubiquitine et SUMO dans le contrôle de la localisation protéique.
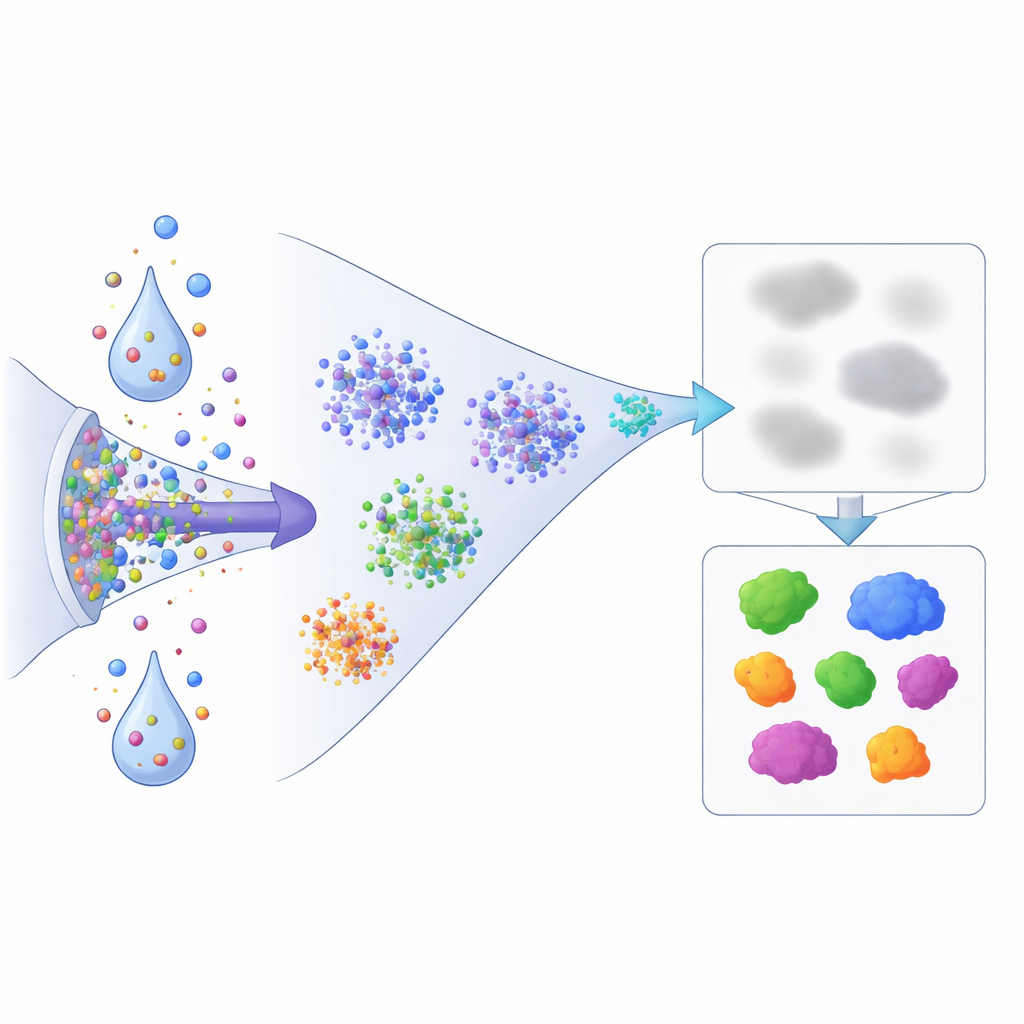
Ce que cela signifie pour la découverte de médicaments à venir
Pour un public non spécialiste, le message central est que les protéines ne se contentent pas d’augmenter ou de diminuer en quantité lorsque les cellules sont stressées ou traitées par des médicaments ; elles se déplacent, se condensent et modifient leur degré d’attachement aux structures cellulaires. Ce travail fournit une méthode à haute vitesse et à l’échelle du protéome pour observer ces changements. En combinant un protocole de spectrométrie de masse ajusté avec une comparaison simple soluble‑contre‑insoluble, les auteurs montrent que des médicaments expérimentaux courants réorganisent rapidement le paysage protéique interne de façons que des mesures d’abondance standard ne détecteraient pas. L’approche ouvre la voie au cartographie de la manière dont des candidats-médicaments remodelent les états protéiques dans toute la cellule, aidant les chercheurs à découvrir des cibles inattendues, des voies de stress et des points de défaillance qui pourraient être cruciaux pour comprendre à la fois l’action thérapeutique et les effets secondaires.
Citation: Xiong, Y., Zhang, H., Tan, L. et al. Supercharging-enhanced nDIA-MS enables global profiling of drug-induced proteome solubility shifts. Nat Commun 17, 2350 (2026). https://doi.org/10.1038/s41467-026-69025-8
Mots-clés: solubilité du protéome, spectrométrie de masse, inhibiteur du protéasome MG132, inhibiteur de la SUMOylation ML-792, transitions d'état des protéines