Clear Sky Science · fr
Architecture interne conçue des nanoparticules lipidiques cœur-coquille favorise une libération endosomale efficace de l’ARNm
Pourquoi cette nouvelle astuce de livraison est importante
Beaucoup des médicaments les plus prometteurs, des vaccins contre la COVID-19 aux traitements expérimentaux contre le cancer, sont basés sur l’ARN messager, ou ARNm. Mais un problème tenace subsiste : une fois ces brins fragiles entrés dans nos cellules, la plupart se retrouvent piégés et détruits dans de petites cavités internes appelées endosomes. Cette étude présente une réinvention ingénieuse des minuscules bulles graisseuses, les nanoparticules lipidiques, qui transportent l’ARNm. En réorganisant leur structure interne autour d’un cœur solide en or, les chercheurs améliorent de façon spectaculaire la quantité d’ARNm qui parvient à s’échapper dans le compartiment de travail de la cellule, où il peut réellement produire des protéines utiles.
Donner aux petits coursiers un meilleur plan corporel
Les vaccins et thérapies à ARNm actuels reposent principalement sur des particules souples et amorphes composées d’un mélange de lipides qui enveloppent l’ARNm. En théorie, des lipides « ionisables » présents dans ces particules devraient devenir positivement chargés dans l’intérieur acide des endosomes et perforer la membrane endosomale, libérant ainsi l’ARNm. En pratique, la charge négative de l’ARNm annule une grande partie de cet effet, de sorte qu’environ seulement 2 % de l’ARNm délivré atteint la machinerie de production de protéines de la cellule. Les auteurs posent une question simple mais puissante : au lieu de changer uniquement la chimie des lipides, et si l’on réingéniait l’architecture interne de la particule pour contrôler la position relative de l’ARNm et des lipides ?
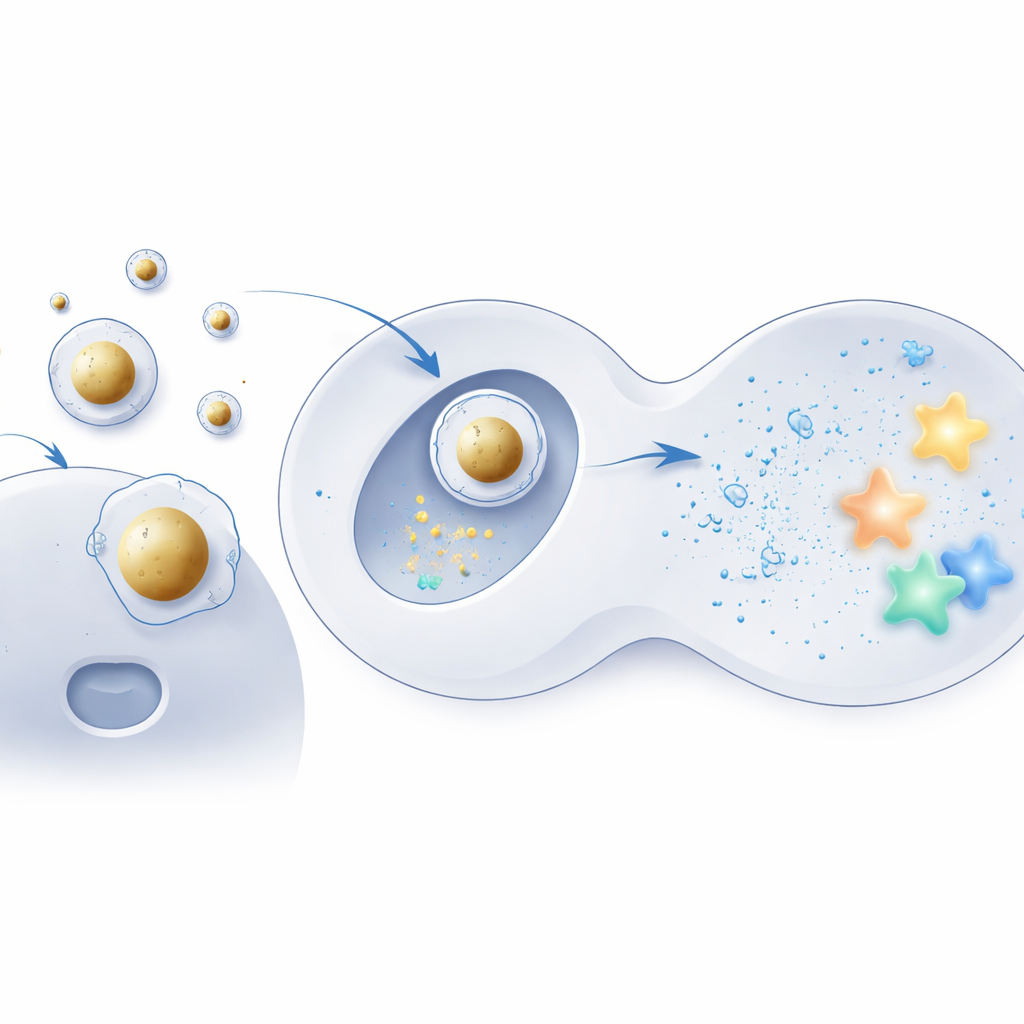
Construire une coque de livraison centrée sur l’or
Pour tester cette idée, l’équipe a utilisé de petites sphères d’or comme cœurs rigides et les a recouvertes des mêmes lipides ionisables employés dans les formulations conventionnelles. L’ARNm, chargé négativement, a d’abord été condensé sur ces cœurs, puis l’assemblage a été enveloppé dans un mélange familier de lipides auxiliaires et de molécules stabilisantes, créant une structure organisée cœur–coquille. La microscopie électronique et les simulations informatiques ont montré que ces « Au‑LNP » étaient très uniformes, thermodynamiquement stables et conservaient bien leur forme dans des conditions aqueuses et proches du milieu corporel. Surtout, leur composition lipidique globale restait la même que celle des particules standard, isolant la structure interne — et non les ingrédients — comme changement clé.
Comment un intérieur réarrangé favorise l’évasion
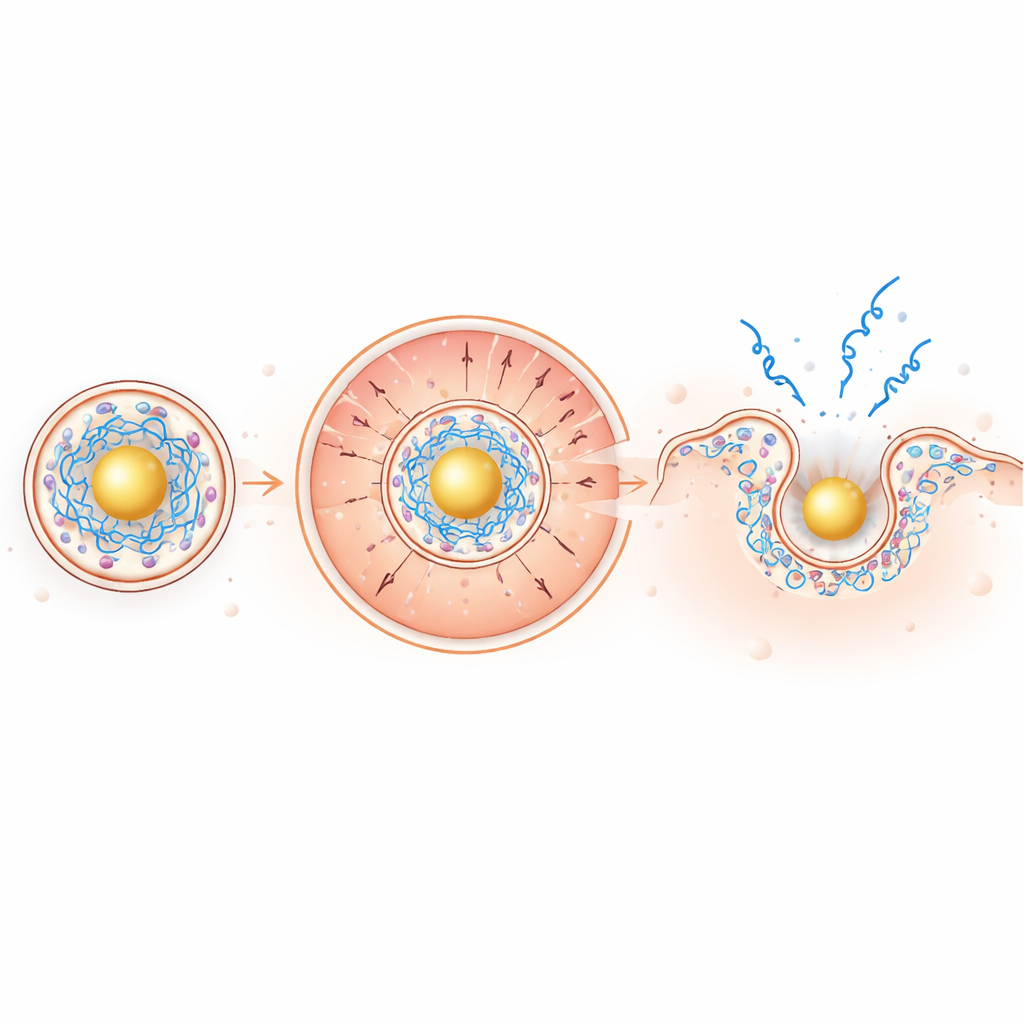
Dans l’environnement endosomal légèrement acide, le cœur à base d’or devient fortement positif, attirant l’ARNm chargé négativement vers l’intérieur tout en repoussant les lipides ionisables chargés positivement vers la membrane environnante. Cette ségrégation pilotée par des charges concentre les lipides perturbateurs de membrane précisément là où ils sont nécessaires. Dans des tests sur membranes modèles et sur des globules rouges, les nouvelles particules étaient plus efficaces pour perforer les membranes à faible pH tout en restant inactives à pH neutre, une caractéristique de sécurité souhaitable. Dans des cellules vivantes, l’imagerie d’ARNm fluorescent a révélé environ un doublement de l’évasion endosomale et une augmentation étonnante d’environ 100 fois de la dispersion de l’ARNm dans le cytoplasme comparé aux particules conventionnelles.
Des boîtes de culture aux souris : signaux plus forts et meilleure protection
Ces avantages physiques se sont traduits par des gains biologiques réels. Dans plusieurs types cellulaires, les particules à noyau d’or ont entraîné une production beaucoup plus élevée de protéines rapporteurs que les formulations standard, notamment à faibles doses. Chez la souris, elles ont augmenté la production de protéines dirigée par l’ARNm jusqu’à cinq à sept fois après des injections intramusculaires ou intraveineuses, sans modifier la distribution corporelle habituelle des particules. Utilisées pour délivrer un ARNm codant la protéine Spike du SARS‑CoV‑2, les particules repensées ont à peu près doublé les taux d’anticorps après la première injection et les ont encore accrus après un rappel, tout en produisant des anticorps neutralisants du virus plus puissants. Dans un modèle difficile de cancer du sein triple négatif, les vaccins à ARNm véhiculés par les nouvelles particules ont réduit les tumeurs de manière plus efficace, abaissé les signaux d’activité tumorale et prolongé de façon notable la survie.
Sécurité et voie vers des médicaments futurs
Malgré l’utilisation de l’or en leur cœur, les particules ont semblé bien tolérées chez la souris. Le poids corporel, les marqueurs inflammatoires et les examens tissulaires n’ont montré aucune toxicité majeure, et les niveaux d’or dans les organes sont revenus vers la ligne de base en l’espace de deux jours. Les auteurs insistent sur le fait que l’or sert principalement de support conceptuel : le même principe de conception interne pourrait être appliqué à d’autres matériaux sûrs ou biodégradables. Le message central pour les non-spécialistes est que la façon dont nous empaquetons l’ARNm à l’intérieur de son minuscule vecteur peut importer autant que ce avec quoi nous l’empactons. En offrant aux nanoparticules lipidiques une organisation interne plus disciplinée, ce travail propose une nouvelle manière de franchir un goulot d’étranglement ancien de la délivrance d’ARNm — débloquant des vaccins et des thérapies plus efficaces contre les maladies infectieuses, le cancer et au-delà.
Citation: Li, T., Zhang, J., Guo, J. et al. Engineered internal architecture of core-shell lipid nanoparticles promotes efficient mRNA endosomal release. Nat Commun 17, 2187 (2026). https://doi.org/10.1038/s41467-026-69017-8
Mots-clés: administration d’ARNm, nanoparticules lipidiques, évasion endosomale, nanomédecine, vaccins à ARN