Clear Sky Science · fr
Une thérapie combinée ciblée et épigénétique renforce l’immunité antitumorale en stabilisant l’expression du CMH I dépendante de GATA6 dans l’adénocarcinome canalaire pancréatique
Pourquoi cette recherche est importante pour le cancer du pancréas
L’adénocarcinome canalaire pancréatique est l’un des cancers les plus mortels, en grande partie parce qu’il se dissimule au système immunitaire et résiste à la plupart des médicaments. Cette étude met au jour un état cellulaire tumoral particulier, gouverné par un gène appelé GATA6, qui rend les cellules du cancer pancréatique plus visibles aux attaques immunitaires. Les auteurs montrent aussi comment la combinaison de deux types de médicaments peut préserver cet état vulnérable et améliorer la capacité des lymphocytes T cytotoxiques à attaquer les tumeurs dans des modèles expérimentaux.
Un état cellulaire tumoral qui invite le système immunitaire
Toutes les cellules du cancer du pancréas ne se comportent pas de la même façon. Certaines conservent une identité plus ordonnée, de type épithélial, tandis que d’autres dérivent vers un état plus mobile et agressif, de type mésenchymateux. le facteur de transcription GATA6 aide à maintenir l’identité épithéliale et est associé à de meilleurs résultats chez les patients. Dans de larges cohortes, les tumeurs présentant des niveaux élevés de GATA6 contenaient davantage de cellules immunitaires, y compris des lymphocytes T CD8 « tueurs », que les tumeurs avec peu ou pas de GATA6. À l’aide d’imageries spatiales avancées sur des échantillons humains, les chercheurs ont observé que les cellules cancéreuses GATA6-positives étaient plus souvent adjacentes aux T CD8 et présentaient des niveaux plus élevés d’une molécule appelée CMH I, qui agit comme un drapeau montrant aux T ce que contient la cellule. Ces observations suggèrent que GATA6 identifie une population tumorale naturellement plus visible pour le système immunitaire. 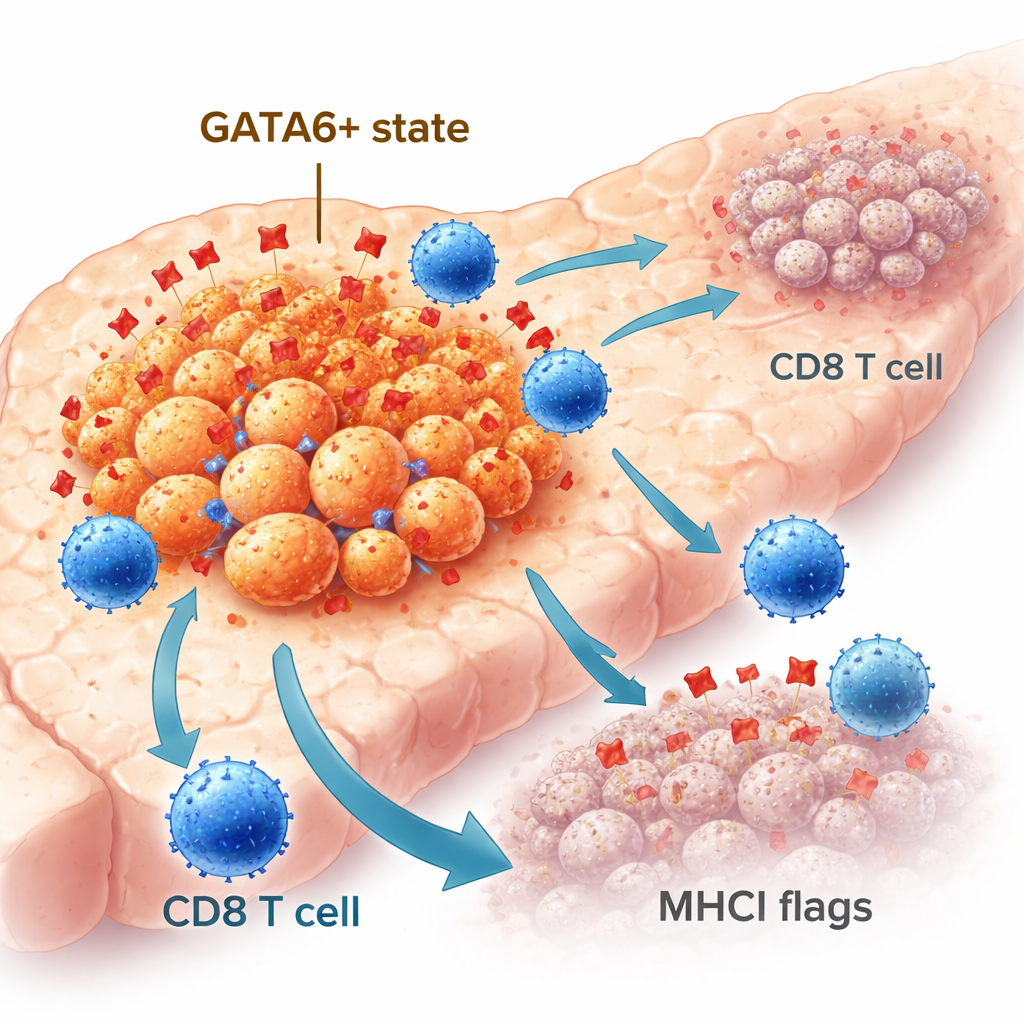
Une thérapie ciblée qui augmente la visibilité tumorale — mais à quel prix
L’équipe s’est ensuite demandé si des médicaments ciblés pouvaient encore augmenter cette visibilité. Ils se sont concentrés sur les inhibiteurs de MEK, une classe de médicaments qui bloquent une voie de signalisation de croissance fréquemment active dans le cancer du pancréas. Dans des lignées cellulaires pancréatiques murines et dans des tumeurs développées chez la souris et dans des xénogreffes dérivées de patients, l’inhibition de MEK augmentait le CMH I à la surface des cellules tumorales à forte expression de GATA6, les rendant potentiellement de meilleurs cibles pour les T. Lorsque des tumeurs riches en GATA6 étaient traitées par inhibiteurs de MEK chez la souris, la croissance tumorale ralentissait, le CMH I augmentait et davantage de T CD8 portant des molécules cytotoxiques envahissaient les tumeurs. Bloquer directement GATA6, soit par suppression génique soit par dégradation rapide de la protéine, annulait cette augmentation du CMH I induite par l’inhibiteur de MEK et le contrôle tumoral qui en résultait, démontrant que GATA6 est essentiel pour cet effet bénéfique.
Comment les tumeurs s’adaptent : glissement vers un état plus difficile à éliminer
Cependant, l’histoire a une tournure. Un traitement prolongé par inhibiteurs de MEK poussait de nombreuses cellules tumorales à basculer de l’état épithélial GATA6-positif vers un état plus mésenchymateux, à faible GATA6, associé à la résistance au traitement. Tant dans les modèles murins que dans les xénogreffes dérivées de patients, les tumeurs traitées par inhibiteurs de MEK montraient à terme moins de cellules GATA6-positives, davantage de marqueurs de transition épithélio-mésenchymateuse et un bénéfice global moins durable. Bien que des cellules GATA6-positives individuelles augmentent encore leur CMH I en réponse au médicament, la réduction de la taille de cette population limitait l’amélioration globale de la présentation des antigènes tumoraux, ce qui aide à expliquer pourquoi les inhibiteurs de MEK seuls ont déçu dans les essais cliniques contre le cancer du pancréas.
Des médicaments épigénétiques qui maintiennent les tumeurs dans l’état vulnérable
Pour contrer cette échappée adaptative, les chercheurs se sont tournés vers les inhibiteurs des histones désacétylases, ou inhibiteurs de HDAC, une classe de médicaments épigénétiques connus pour influencer l’identité cellulaire et la visibilité immunitaire. en culture cellulaire et dans des modèles murins, la combinaison d’inhibiteurs de MEK avec des inhibiteurs de HDAC de classe I tels que la domatinostat a restauré l’expression de GATA6 supprimée par l’inhibition de MEK, inversé les signes de transition épithélio-mésenchymateuse et encore renforcé les niveaux de CMH I à la surface des cellules tumorales. Fait important, cette thérapie combinée a entraîné une infiltration et une activation plus fortes des T CD8 et davantage de mort cellulaire tumorale dans des tumeurs orthotopiques murines et dans un modèle murin génétiquement modifié qui imite de près le cancer pancréatique humain. L’épuisement des T CD8 éliminait une grande partie du bénéfice, confirmant que la combinaison agit en grande partie en renforçant l’action des lymphocytes T tueurs.
Vers des thérapies combinées plus intelligentes pour un cancer difficile
En rassemblant ces résultats, l’étude propose une stratégie selon laquelle l’inhibition ciblée de MEK et l’inhibition épigénétique de HDAC sont utilisées ensemble pour stabiliser un état cellulaire tumoral dirigé par GATA6, riche en CMH I et donc hautement reconnaissable par le système immunitaire. En augmentant à la fois le nombre de cellules GATA6-positives et en renforçant leurs « drapeaux » CMH I, la combinaison favorise une infiltration plus profonde des T CD8, une activité cytotoxique plus forte et une survie prolongée dans des modèles murins agressifs du cancer du pancréas. Bien que les inhibiteurs de HDAC puissent provoquer des effets secondaires importants et que ces travaux restent précliniques, cette recherche ouvre la voie à des approches thérapeutiques futures associant des médicaments ciblant des voies et des modificateurs épigénétiques soigneusement choisis pour rendre les tumeurs pancréatiques plus vulnérables aux défenses immunitaires de l’organisme. 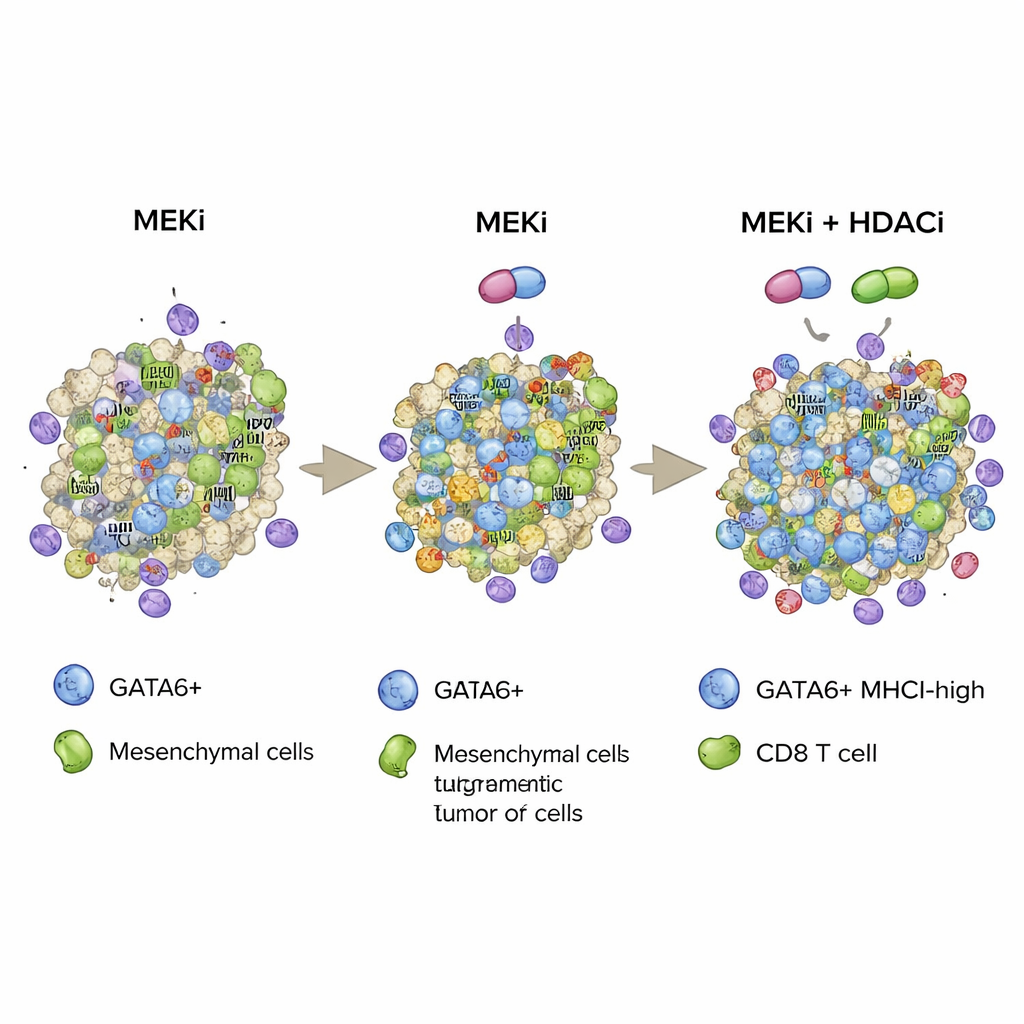
Citation: Peng, J., Yang, J., Antonopoulou, G. et al. Combined targeted and epigenetic-based therapy enhances antitumor immunity by stabilizing GATA6-dependent MHCI expression in pancreatic ductal adenocarcinoma. Nat Commun 17, 1476 (2026). https://doi.org/10.1038/s41467-026-69013-y
Mots-clés: cancer du pancréas, immunité tumorale, GATA6, inhibiteur de MEK, inhibiteur de HDAC