Clear Sky Science · fr
Immobilisation synergique multicomposante via des stratégies d’échange in situ et dynamique pour la construction de biopharmaceutiques hiérarchiques
Pourquoi il est important de concevoir des médicaments plus intelligents
Beaucoup des médicaments les plus puissants d’aujourd’hui sont de grandes et fragiles molécules biologiques, comme des protéines et des enzymes. Elles peuvent combattre le cancer, éliminer des bactéries nuisibles et accélérer la cicatrisation, mais elles sont faciles à détériorer et difficiles à délivrer au bon endroit dans l’organisme. Cet article décrit une nouvelle manière de « conditionner » plusieurs de ces composants délicats à l’intérieur d’un matériau protecteur et spongieux, afin qu’ils agissent en séquence avec plus d’efficacité et moins d’effets secondaires.
Transformer un cristal en immeuble moléculaire
Les chercheurs partent d’un matériau poreux spécial composé d’ions métalliques et de petits éléments organiques. Il se comporte un peu comme un minuscule immeuble flexible rempli de pièces et de couloirs. Ils montrent que ce réseau, appelé structure pyrimidine zéolitique, peut se former autour des protéines de sorte que celles-ci se retrouvent protégées à l’intérieur du cristal. Cet emprisonnement « in situ » n’écrase ni n’inactive les protéines, et des images précises confirment qu’elles sont réparties de manière homogène à l’intérieur, un peu comme des locataires présents à chaque étage d’un immeuble.
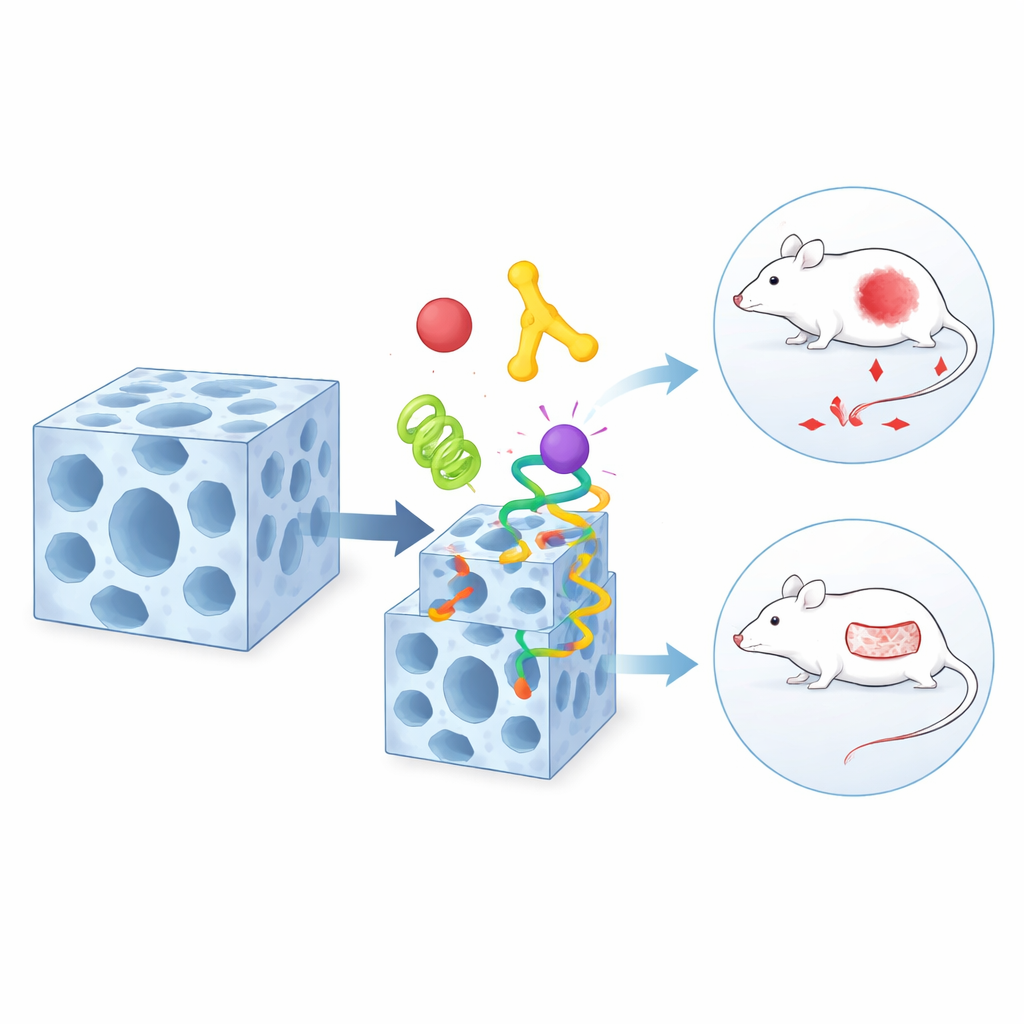
Un hôte métamorphe pour la décoration de surface
Le même matériau a un second tour étonnant : il peut modifier réversiblement sa structure interne lorsqu’il est exposé à certains solvants ou à l’eau. Au cours de cette transformation douce, certaines liaisons chimiques du réseau se relâchent puis se reforment. L’équipe a découvert que des groupes chimiques présents à la surface des protéines — comme ceux de certains acides aminés — peuvent profiter de ce moment de faiblesse. Ils rivalisent temporairement avec les éléments constitutifs originaux du réseau et s’insèrent dans des « défauts » nouvellement créés près de la surface. En conséquence, une couche de protéines se retrouve principalement ancrée à l’extérieur du cristal, tandis que celles de l’intérieur restent en place. Ce processus d’échange dynamique permet aux scientifiques de décider quels composants vivent au cœur et lesquels ornent l’enveloppe extérieure.
Concevoir des chaînes de montage enzymatiques
Avec le contrôle des espaces intérieur et extérieur, les auteurs construisent de minuscules « lignes d’assemblage » enzymatiques. Dans un exemple, une enzyme qui transforme le sucre en un produit intermédiaire agressif est enfermée à l’intérieur du réseau, tandis qu’une seconde enzyme qui dégrade ce produit de façon sûre est fixée près de la surface. Cet agencement intérieur–extérieur rend la réaction plus rapide et plus efficace que des conceptions classiques cœur–enveloppe ou des mélanges aléatoires d’enzymes. Parce que les enzymes extérieures sont plus accessibles aux molécules et que l’intermédiaire nocif est rapidement éliminé, le système reste actif sur de nombreux cycles et tolère mieux la chaleur, les conditions difficiles et les usages répétés.
Des emballages intelligents anti-cancer et antibactériens
La vraie portée de cette approche apparaît lorsqu’elle est appliquée à la médecine. L’équipe combine une protéine ciblant les tumeurs, une enzyme consommant le glucose et un médicament de chimiothérapie classique dans une seule particule stratifiée. Le composant de ciblage à la surface guide la particule vers les cellules cancéreuses, l’enzyme épuise leur réserve d’énergie en consommant le sucre local, et la petite molécule médicamenteuse porte un coup létal supplémentaire. Chez des souris porteuses de greffes tumorales humaines, ce paquet tripartite réduit les tumeurs bien plus efficacement que l’un quelconque des composants pris isolément ou des mélanges plus simples. Dans une autre conception, les auteurs adaptent le réseau pour des plaies cutanées infectées en plaçant un peptide antibactérien et une enzyme remodelant les tissus dans des régions distinctes du même vecteur. Chez des rats, ces particules réduisent fortement l’infection et accélèrent la fermeture de plaies difficiles par rapport aux traitements conventionnels.

Comment ce travail fait progresser la médecine
Pour un non-spécialiste, le message principal est que cette étude transforme un cristal poreux unique en un habitat programmable pour de nombreux types de molécules thérapeutiques. En décidant qui vit à l’intérieur, qui réside à la surface et selon quel ratio, les chercheurs peuvent orchestrer des traitements par étapes — d’abord cibler, puis attaquer, puis réparer — au sein d’un seul et même objet minuscule. Cette stratégie non seulement protège des médicaments biologiques fragiles, mais leur permet aussi de se soutenir mutuellement, conduisant à des thérapies anticancéreuses et antibactériennes plus puissantes et plus précises. Les mêmes principes de conception pourraient être adaptés à de futurs « médicaments intelligents » nécessitant la coopération de plusieurs composants au bon endroit et au bon moment.
Citation: Yang, M., Meng, X., Shi, R. et al. Multicomponent synergistic immobilization via in-situ and dynamic exchange strategies for constructing hierarchical biopharmaceuticals. Nat Commun 17, 2208 (2026). https://doi.org/10.1038/s41467-026-69009-8
Mots-clés: structures métal-organiques, immobilisation d’enzymes, nanomédecine anticancéreuse, cicatrisation des plaies, libération de biopharmaceutiques