Clear Sky Science · fr
Les kinases des adhésions focales régulent l’action de la leptine et l’effet amaigrissant de l’inhibition de HDAC6
Pourquoi cette recherche importe pour le contrôle du poids
De nombreuses personnes vivant avec l’obésité ont des niveaux élevés de l’hormone leptine, qui est censée informer le cerveau que l’organisme possède suffisamment de graisse et qu’il doit manger moins. Pourtant, leur cerveau ignore souvent ce signal, état appelé résistance à la leptine. Cette étude met en lumière deux enzymes peu connues dans le cerveau qui jouent le rôle d’« amplificateurs » clés du signal de la leptine, et montre comment des médicaments expérimentaux ciblant une autre enzyme, HDAC6, exploitent cette voie pour restaurer la capacité de la leptine à réduire l’appétit et le poids corporel chez la souris obèse.
Le signal de l’appétit et pourquoi il échoue
La leptine est produite par les cellules adipeuses en proportion de la quantité de graisse que nous portons. Quand la leptine atteint le cerveau, en particulier des régions de l’hypothalamus, elle active normalement une protéine appelée STAT3 qui induit l’expression de gènes limitant la faim et augmentant la dépense énergétique. Dans l’obésité, les taux sanguins de leptine sont élevés mais le signal leptinique dans le cerveau est faible, si bien que l’appétit reste élevé. Des travaux antérieurs ont montré que bloquer l’enzyme HDAC6 en dehors du cerveau peut, de façon inattendue, rendre le cerveau de nouveau sensible à la leptine et provoquer une perte de poids, mais les étapes cruciales à l’intérieur des cellules cérébrales qui traduisent ce signal en réponse étaient peu claires.
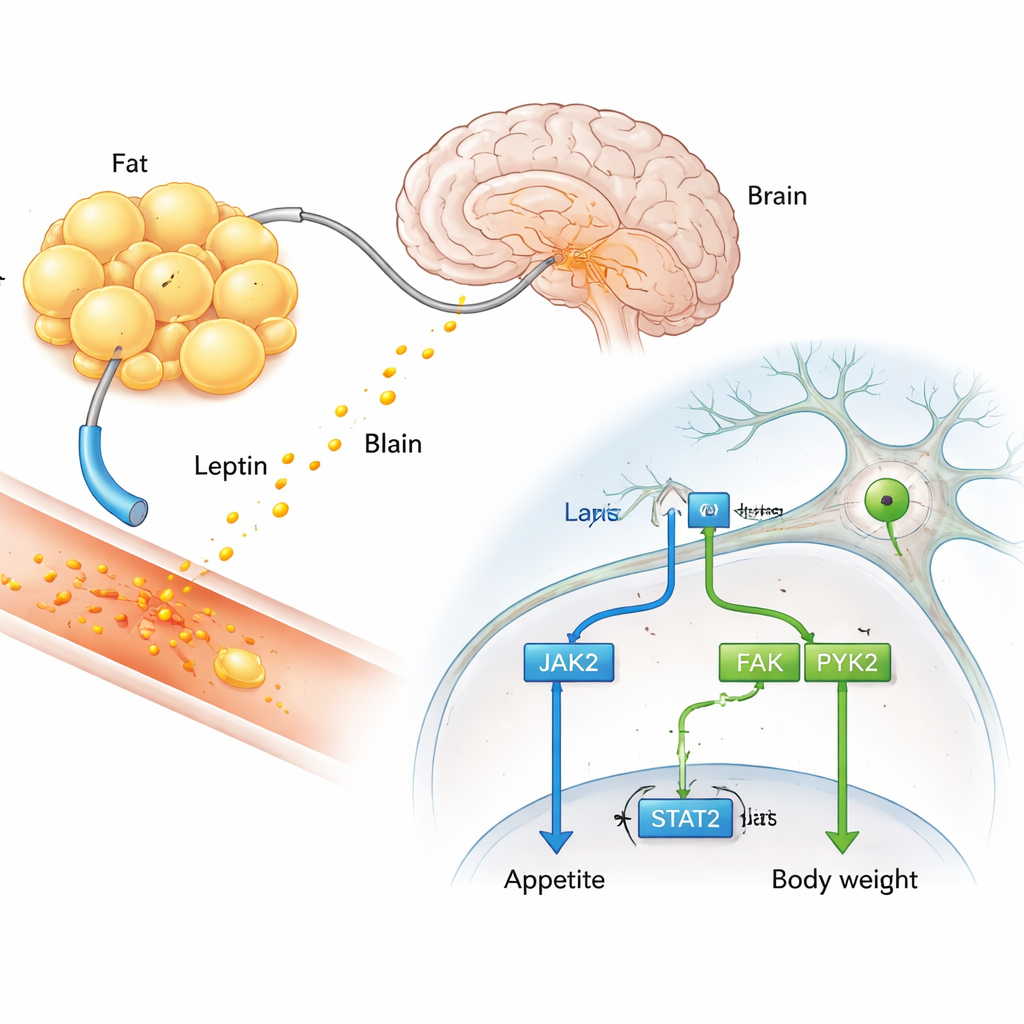
De nouveaux acteurs dans le message de la leptine au cerveau
Les auteurs ont utilisé de vastes bases de données d’expression génique pour comparer les changements cérébraux induits par la leptine et par un médicament bloquant HDAC6, la Tubastatine A, chez des souris obèses. Ils ont recherché des molécules dont le profil d’activité était fortement lié au rétablissement de la sensibilité à la leptine. Cette recherche a mis en évidence une paire de kinases appelées kinases des adhésions focales, FAK et PYK2, mieux connues pour aider les cellules à percevoir leur environnement physique. L’équipe a constaté que ces kinases sont largement présentes dans les neurones répondant à la leptine dans les centres hypothalamiques clés de l’appétit, suggérant qu’elles pourraient contribuer à transmettre le message de la leptine à l’intérieur de la cellule.
Comment FAK et PYK2 renforcent le signal de la leptine
Dans des expériences cellulaires, les chercheurs ont montré que FAK et PYK2 se lient physiquement à STAT3 et peuvent y ajouter un groupement phosphate agissant comme un « interrupteur » d’activation, une étape habituellement attribuée à une autre enzyme, JAK2. Même dans des cellules dépourvues de JAK2, la leptine pouvait encore activer STAT3 lorsque FAK et PYK2 étaient présents. Lorsque les scientifiques ont réduit les niveaux de FAK ou de PYK2, ou bloqué leur activité avec un médicament, la capacité de la leptine à activer STAT3 et ses gènes cibles a fortement diminué. Cela indique que FAK et PYK2 agissent comme des partenaires importants qui aident la leptine à activer pleinement STAT3, en travaillant aux côtés de JAK2 ou en le remplaçant.
De la chimie cérébrale au comportement alimentaire
Pour tester l’impact chez l’animal vivant, l’équipe a bloqué FAK et PYK2 dans le cerveau des souris. Les souris maigres recevant de la leptine mangent normalement moins après un jeûne, mais lorsque les kinases des adhésions focales ont été inhibées, cet effet suppressif sur l’appétit a été atténué et l’activation de STAT3 dans le cerveau a été plus faible. Des souris génétiquement dépourvues de PYK2 ont montré une résistance partielle similaire à la leptine et à la perte de poids induite par la Tubastatine A. Lorsque FAK et PYK2 ont été réduits de façon ciblée dans l’hypothalamus de souris adultes, les animaux sont devenus hyperphagiques — ils ont mangé davantage, pris de la graisse et développé une glycémie plus élevée — même avec un régime standard. Ces souris ont également perdu la réponse habituelle de perte de poids aux inhibiteurs de HDAC6, montrant que les kinases des adhésions focales sont nécessaires pour que ces médicaments fonctionnent.
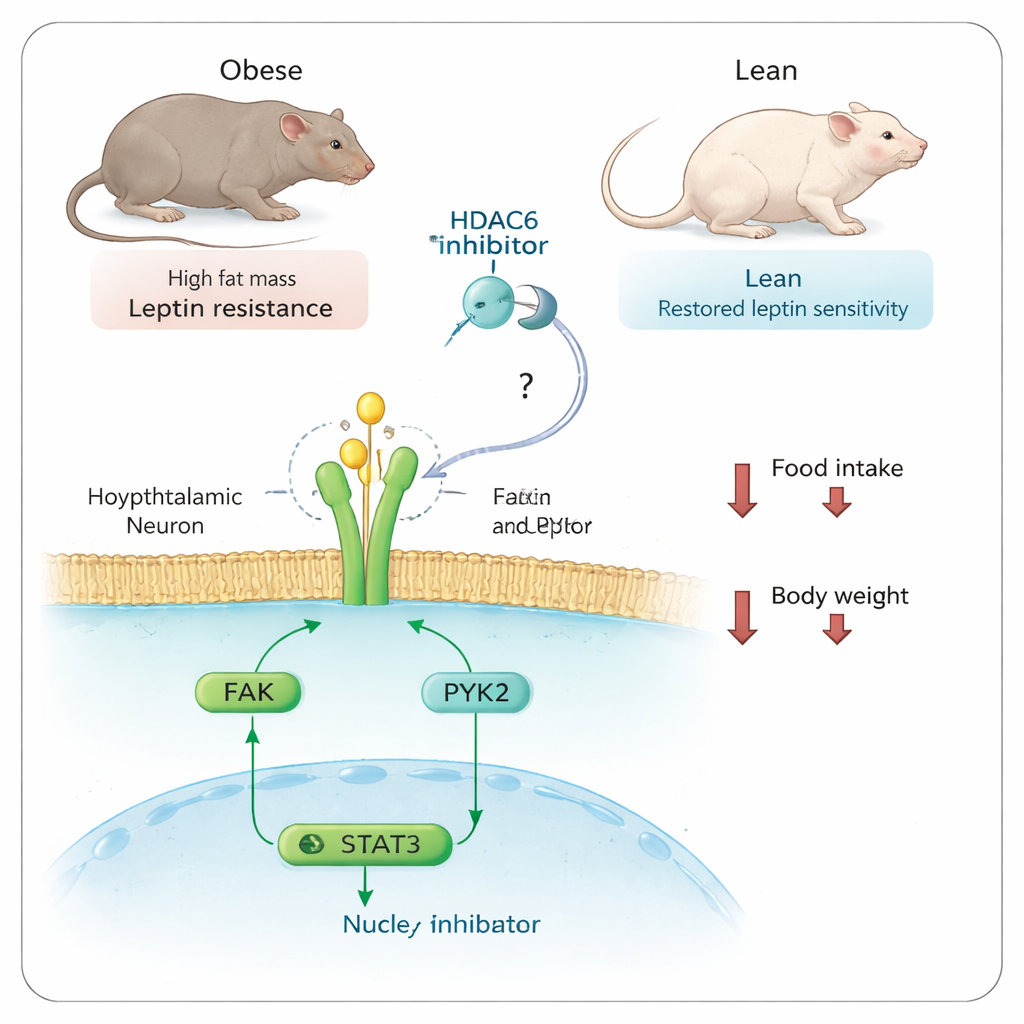
Relier la graisse corporelle, le sang et le cerveau
Les résultats soutiennent un modèle en deux étapes. D’abord, le blocage de HDAC6 dans les tissus périphériques, en particulier dans la graisse, conduit à la libération d’un facteur non encore identifié dans le sang. Ensuite, ce facteur atteint le cerveau et augmente l’expression et l’activité de FAK et PYK2 dans les neurones sensibles à la leptine. Avec ces kinases engagées, la leptine peut mieux activer STAT3, ce qui réduit l’apport alimentaire et favorise la perte de poids. Lorsque FAK et PYK2 sont absents ou inhibés dans l’hypothalamus, les médicaments bloquant HDAC6 n’aident plus, car le signal de la leptine ne peut pas être pleinement amplifié.
Ce que cela signifie pour les thérapies futures contre l’obésité
Pour un public non spécialiste, le message principal est que ce travail identifie un « circuit amplificateur » crucial pour l’hormone naturelle de contrôle de l’appétit. FAK et PYK2 agissent comme des aides moléculaires qui permettent à la leptine de dire efficacement au cerveau : « Tu en as assez ; tu peux arrêter de manger maintenant. » Des médicaments qui moduleraient en toute sécurité cette voie — en ciblant HDAC6 dans le corps et les kinases des adhésions focales dans le cerveau — pourraient un jour compléter le régime et l’exercice pour traiter l’obésité en restaurant, plutôt qu’en remplaçant, le système naturel de contrôle du poids de l’organisme.
Citation: Hadley, C.K., Galgano, L., Gui, Y. et al. The focal adhesion kinases regulate leptin action and the weight reducing effect of HDAC6 inhibition. Nat Commun 17, 1212 (2026). https://doi.org/10.1038/s41467-026-69008-9
Mots-clés: résistance à la leptine, obésité, hypothalamus, signalisation STAT3, inhibiteurs de HDAC6