Clear Sky Science · fr
La matrice extracellulaire favorise l’agrégation des cellules tumorales circulantes dans les métastases du cancer du sein triple négatif
Comment des cellules cancéreuses du sein se regroupent dans la circulation sanguine
Lorsque le cancer du sein se propage, c’est souvent parce que des cellules tumorales isolées s’échappent dans la circulation sanguine et colonisent des organes éloignés. Cette étude pose une question apparemment simple mais aux implications majeures : comment les cellules de cancer du sein les plus agressives, qui ont perdu leur « Velcro » habituel pour rester ensemble, réussissent-elles néanmoins à voyager en grappes serrées — et pourquoi cela les rend-il si mortelles ?
Un manteau sucré collant qui remplace la colle cellulaire classique
Les auteurs se concentrent sur le cancer du sein triple négatif (CSTN), une forme particulièrement agressive qui libère souvent des cellules tumorales circulantes (CTC) dans le sang. Dans de nombreux cancers, les grappes de CTC sont bien plus susceptibles de provoquer des métastases que les cellules isolées. Typiquement, ces grappes sont maintenues par des jonctions adhérentes épithéliales — des complexes protéiques spéciaux qui agissent comme des rivets moléculaires entre cellules voisines. Mais les cellules de CSTN perdent fréquemment ces protéines de jonction, ce qui pose un paradoxe : sans la colle habituelle, qu’est-ce qui maintient l’intégrité de leurs grappes ? En explorant de larges bases de données génomiques tumorales, les chercheurs ont découvert que les tumeurs de CSTN sont enrichies en gènes impliqués dans l’armature externe de la cellule, appelée matrice extracellulaire. Un gène se distingue, HAS2, qui code pour une enzyme synthétisant l’hyaluronane (HA), un long polymère sucré qui enrobe les cellules. Des niveaux élevés de HAS2 et d’HA étaient fortement corrélés à des caractéristiques tumorales agressives et métastatiques.
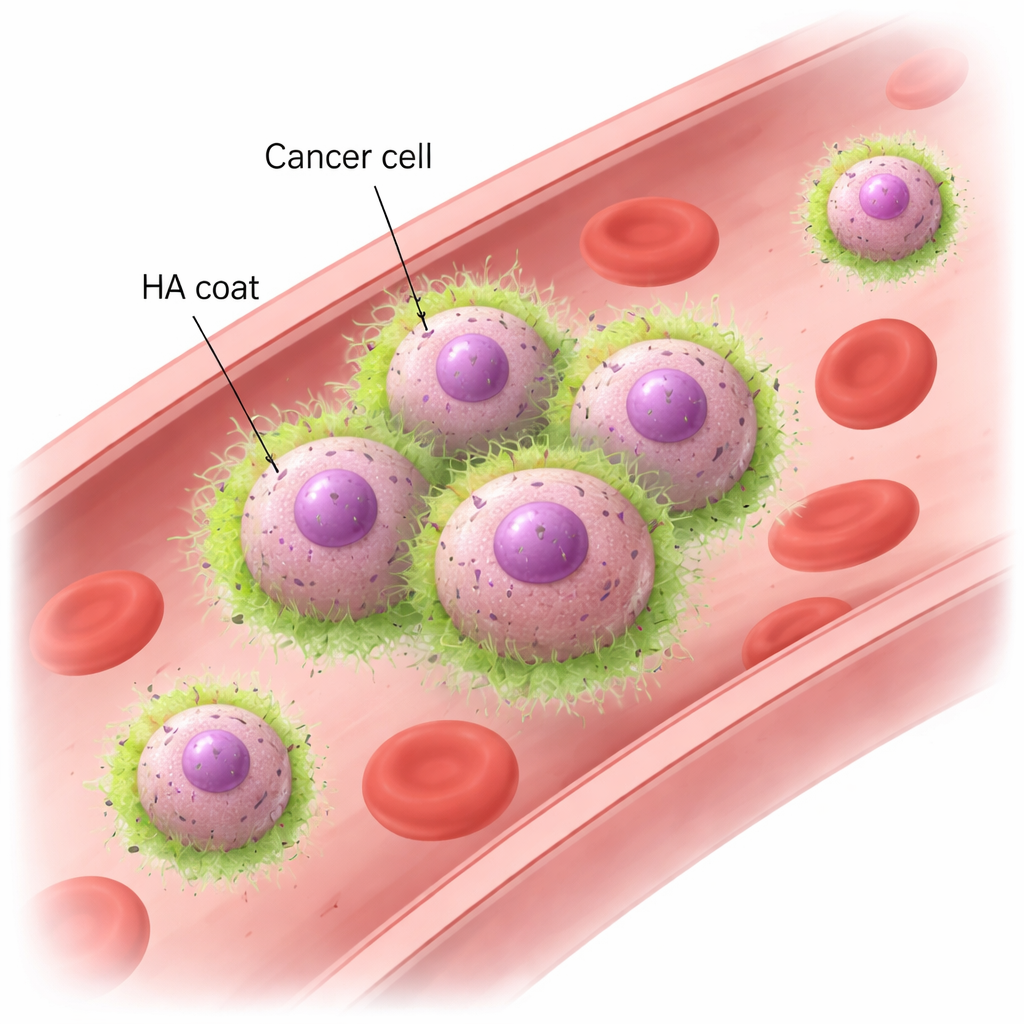
Hyaluronane et CD44 : une nouvelle façon pour les cellules de se tenir la main
À l’aide de modèles murins et de lignées de cellules mammaires humaines, l’équipe a montré que les cellules métastatiques de CSTN forment rapidement des grappes lorsqu’elles sont exposées à un flux tourbillonnant simulant la circulation sanguine. Ces grappes restent intactes même sous des forces comparables à celles des vaisseaux sanguins réels, alors que les cellules moins agressives se disloquent et dérivent seules. La microscopie a révélé que les cellules métastatiques sont enveloppées d’un « manteau » d’HA, qui devient concentré précisément aux endroits de contact entre cellules. L’élimination de l’HA par des enzymes, ou la réduction de HAS2, empêchait les cellules de s’agréger sous flux, bien qu’elles puissent encore sédimenter ensemble lorsqu’elles étaient laissées au repos. Le partenaire clé du côté cellulaire est CD44, un récepteur de surface courant qui se lie à l’HA. Les cellules dépourvues de CD44 ne pouvaient plus retenir l’HA à leur surface ni former de grappes. Inversement, des cellules non-agrégantes modifiées pour produire à la fois HAS2 et CD44 ont acquis une capacité robuste à s’agréger. Ces expériences montrent que l’interaction HA–CD44 est à la fois nécessaire et suffisante pour faire adhérer des cellules cancéreuses dans un flux sanguin rapide.
De petites protrusions et des verrous mécaniques construisent des grappes solides
Une imagerie à haute résolution a dévoilé la chorégraphie physique de la formation des grappes. Les cellules isolées de CSTN étendent de nombreuses fines protrusions membranaires à base d’actine — comme des antennes — ponctuées de CD44 et coiffées d’HA. Quand deux cellules se rapprochent, ces antennes se rencontrent d’abord, formant des ponts initiaux HA–CD44. Au fil du temps, les protrusions glissent l’une le long de l’autre, rapprochant les corps cellulaires jusqu’à ce que de larges zones membranaires soient presque côte à côte. Ce processus rappelle la manière dont les cellules épithéliales normales forment des jonctions adhérentes, mais ici il est porté par un manteau sucré flexible plutôt que par des chaînes protéiques rigides. À mesure que la zone de contact mûrit, un autre ensemble de structures intervient : les desmosomes, des jonctions robustes reliant la membrane aux structures internes. Les protéines desmosomales s’accumulent seulement après l’établissement du contact basé sur l’HA et agissent comme des « verrous » mécaniques aidant les grappes à résister aux forces de cisaillement du flux sanguin. Lorsque les composants des desmosomes étaient réduits, les grappes se formaient mais se déchiraient à des contraintes de cisaillement plus élevées.
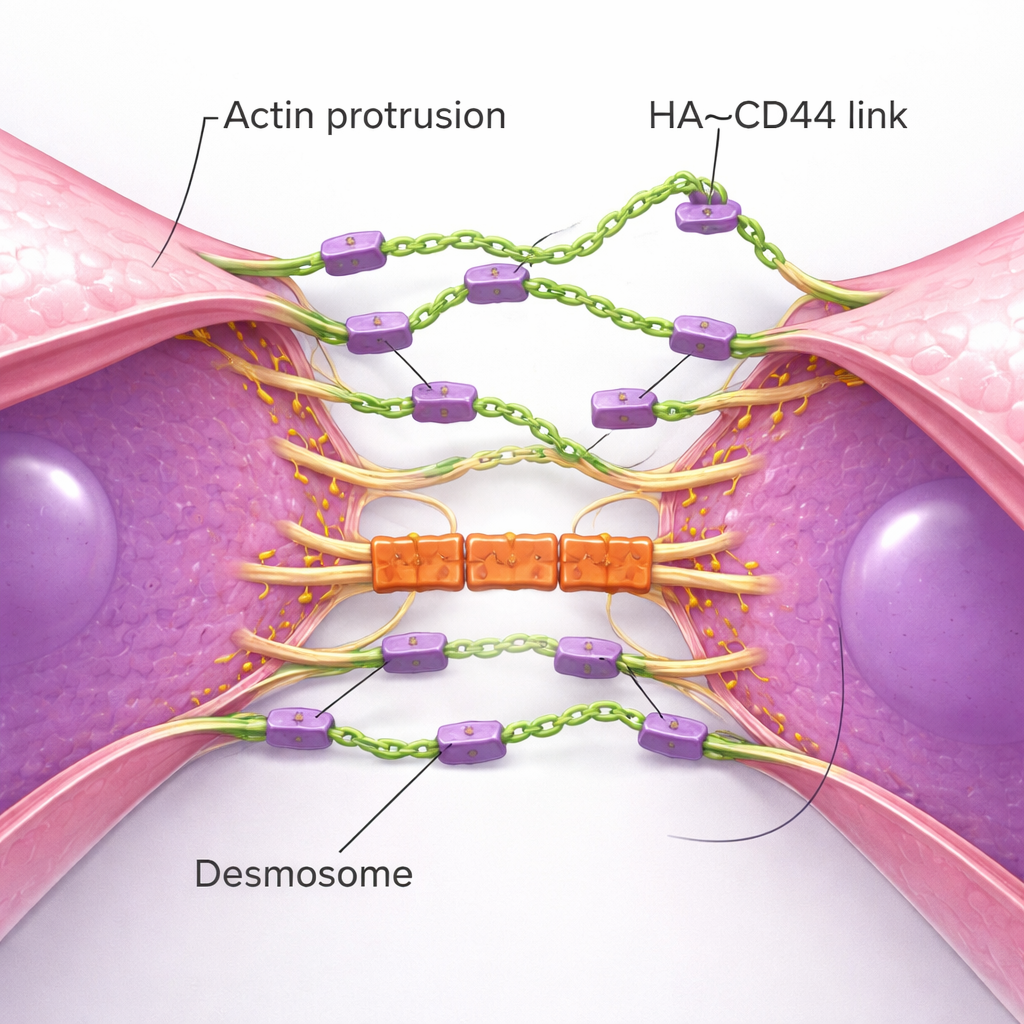
Pourquoi l’agrégation compte pour la survie et la métastase
Le système d’agrégation basé sur l’HA s’est avéré être plus qu’un simple moyen de rester ensemble : il augmentait directement la survie. Sous un flux sanguin simulé prolongé, les grappes riches en HA présentaient des niveaux beaucoup plus faibles d’espèces réactives de l’oxygène nocives et bien moins de mort cellulaire que les cellules isolées appauvries en HA. Dans des modèles murins, les cellules de CSTN dépourvues de HAS2 produisaient beaucoup moins de CTC, formaient uniquement de petites grappes et donnaient nettement moins de métastases pulmonaires — alors que leurs tumeurs primaires croissaient tout aussi bien. Lorsque des grappes préformées de cellules témoins et de cellules déficientes en HAS2 ont été injectées chez la souris, les cellules pauvres en HA colonisaient beaucoup moins efficacement les poumons. De plus, les CTC enveloppées d’HA pouvaient « recruter » d’autres cellules — aussi bien des cellules cancéreuses dépourvues d’HA que des cellules immunitaires normales comme des neutrophiles — dans des grappes mixtes, à condition que ces partenaires expriment CD44. Des prélèvements sanguins de patientes atteintes d’un CSTN métastatique montraient le même schéma : les CTC portaient souvent un manteau d’HA, avec une concentration d’HA aux points de contact entre cellules tumorales et entre cellules tumorales et non tumorales.
Ce que cela signifie pour les patientes et les thérapeutiques futures
Pour un non-spécialiste, l’idée principale est que certaines des cellules de cancer du sein les plus mortelles ne voyagent pas en solitaires mais en petites équipes coopératives maintenues par un manteau sucré externe et son récepteur, plutôt que par les « rivets » classiques entre cellules présents dans les tissus normaux. Ce mécanisme HA–CD44 aide les cellules tumorales à survivre au flux sanguin hostile, à s’unir entre elles et avec des cellules sanguines auxiliaires, et à ensemencer plus efficacement de nouveaux foyers tumoraux dans des organes distants. Cibler la production d’HA (par exemple en inhibant HAS2) ou bloquer son interaction avec CD44 pourrait, en théorie, affaiblir ces grappes et rendre la métastase du CSTN plus difficile, offrant un nouvel angle pour de futures approches anti-métastatiques.
Citation: Bobkov, G.O., Patel, K.J., Lege, B.M. et al. Extracellular matrix mediates circulating tumor cell clustering in triple-negative breast cancer metastasis. Nat Commun 17, 1352 (2026). https://doi.org/10.1038/s41467-026-69007-w
Mots-clés: cancer du sein triple négatif, cellules tumorales circulantes, hyaluronane, CD44, métastase