Clear Sky Science · fr
Cristaux organiques hydrophobes non poreux pour la capture du dioxyde de carbone via une transition de phase par fusion des chaînes
Pourquoi c’est important pour la vie quotidienne
Réduire les émissions de dioxyde de carbone (CO₂) est essentiel pour ralentir le changement climatique, mais les technologies de capture actuelles sont souvent énergivores, coûteuses et complexes. Cette étude présente un matériau solide étonnamment simple qui peut absorber le CO₂ des cheminées industrielles dans des conditions réalistes puis le relâcher à nouveau après une étape de chauffage douce. Agissant presque comme une « éponge solide » réversible fonctionnant même en air humide, ces cristaux ouvrent la voie à des systèmes de dépollution des gaz d’échappement industriels plus abordables et pratiques.
Un nouveau type d’éponge solide pour le CO₂
Les chercheurs se sont concentrés sur une famille de petites molécules organiques dérivées d’un composé courant, la monoéthanolamine, largement utilisée aujourd’hui dans les laveurs liquides de CO₂. En greffant une chaîne huileuse de longueur moyenne — dix atomes de carbone — ils ont obtenu un composé appelé C10‑MEA qui forme des cristaux souples en forme d’aiguilles. Contrairement aux matériaux de capture classiques qui reposent sur des pores permanents et de grandes surfaces internes, ces cristaux sont initialement non poreux et répulsifs à l’eau. Pourtant, exposés au CO₂, ils subissent une transformation solide‑solide rapide qui permet au gaz de pénétrer et de réagir, capturant le CO₂ sans que le matériau ne se liquéfie jamais.
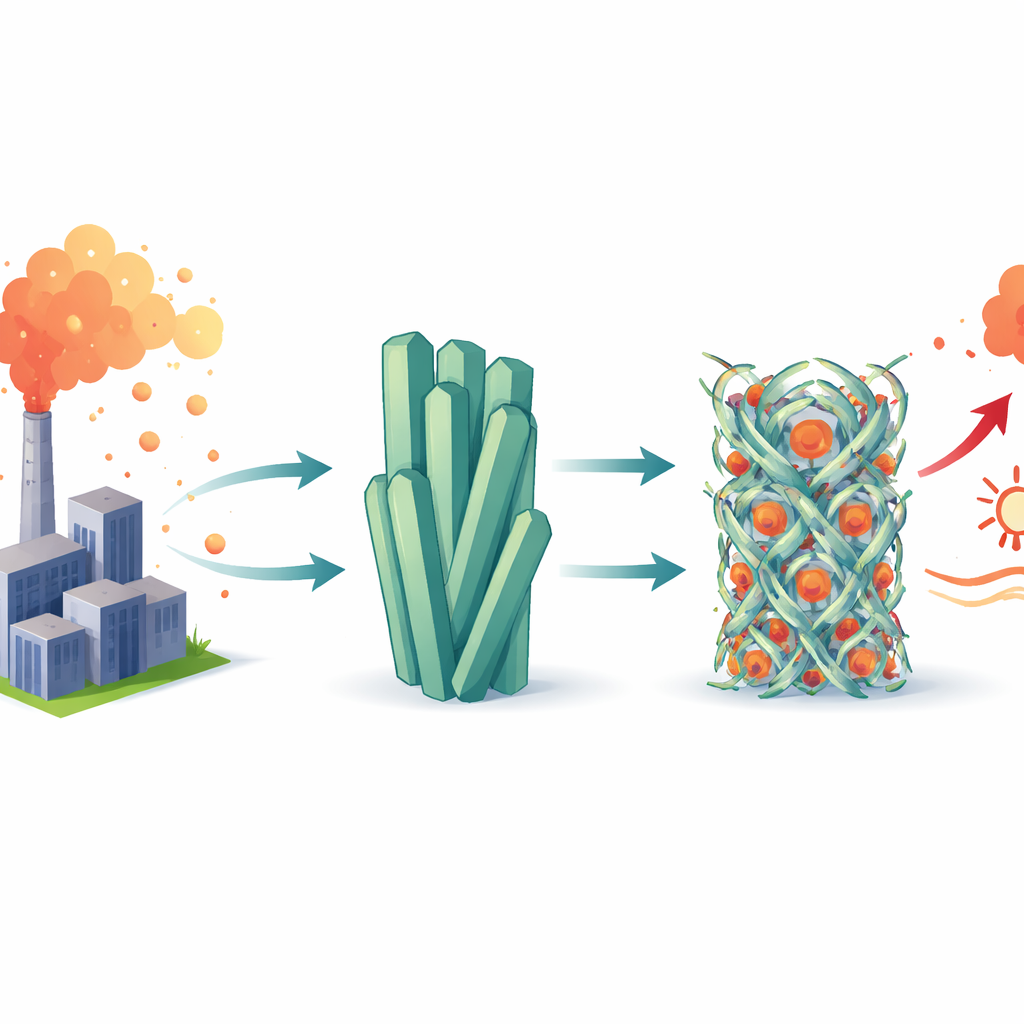
Comment le CO₂ reconfigure le solide
Quand les cristaux de C10‑MEA rencontrent le CO₂, la chaleur libérée par la réaction chimique assouplit localement et « fait fondre » les longues chaînes latérales, un phénomène appelé fusion des chaînes. Cet assouplissement temporaire laisse le CO₂ diffuser dans le solide et former une structure fortement liée nommée carbamate d’ammonium, dans laquelle chaque molécule de CO₂ est associée à deux groupes amine de la matrice hôte. Des techniques avancées — diffraction de poudre aux rayons X, diffraction électronique, spectroscopies infrarouge et Raman, et RMN solide — montrent que les cristaux se réorganisent d’un empilement en couches simple vers un réseau plus complexe en tissage. Dans cette nouvelle organisation, un dense réseau de liaisons hydrogène et des interactions coopératives entre les chaînes huileuses stabilisent le solide riche en CO₂, verrouillant une capacité de capture élevée d’environ 2,5 millimoles de CO₂ par gramme de matériau.
Capture efficace, libération douce
Lors des tests de performance, le C10‑MEA s’est démarqué parmi des composés apparentés aux chaînes légèrement plus courtes ou plus longues. Il a capté le CO₂ rapidement, atteignant une saturation complète en quelques minutes même à de faibles concentrations de gaz et à des températures modestes. Le processus se comporte comme une chimadsorption — formation de liaisons chimiques réelles — mais l’énergie nécessaire pour l’inverser est étonnamment faible, comparable à celle de matériaux qui retiennent les gaz physiquement. Une fois le cristal riche en CO₂ formé, une augmentation de température modeste d’environ 30 °C suffit à déclencher la désorption. Fait remarquable, les auteurs montrent que le CO₂ pur lui‑même peut servir de gaz d’épurage pour extraire le CO₂ capturé à environ 65 °C et à pression atmosphérique, fournissant un flux non dilué adapté à la compression et au stockage.
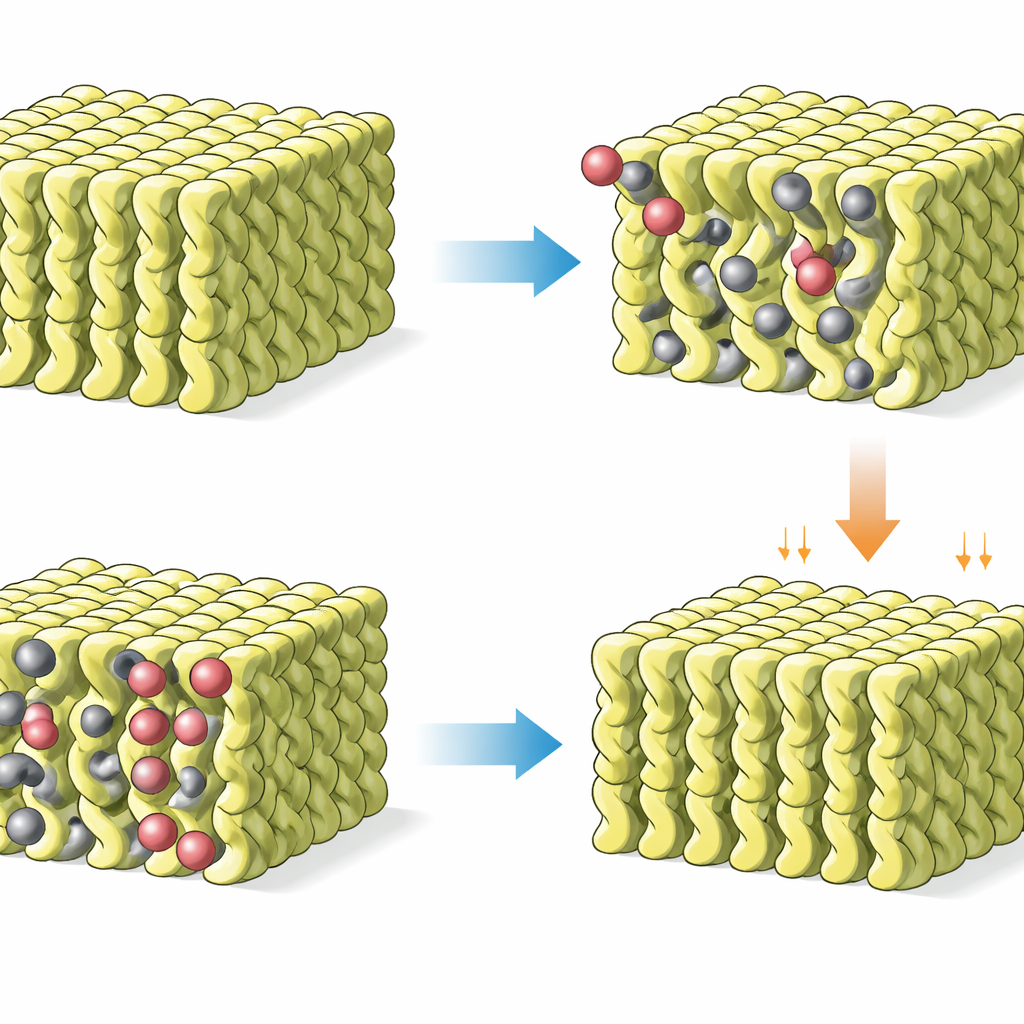
Robuste dans des conditions réelles
Pour qu’un milieu de capture soit pratique dans les centrales électriques ou les usines, il doit tolérer l’eau, l’oxygène et des cycles répétés. La nature hydrophobe des cristaux de C10‑MEA les rend résistants à l’absorption d’eau : sous CO₂ pleinement humide, ils forment toujours le même adduit solide au CO₂ au lieu de se transformer en gel imbibé d’eau. En revanche, sous azote humide, les cristaux initiaux absorbent l’eau et deviennent gélifiés, montrant que la présence de CO₂ protège effectivement la structure. Des études thermogravimétriques et spectroscopiques confirment que le CO₂ est l’espèce principale libérée lors du chauffage et que le matériau reste stable sous des mélanges similaires aux gaz de combustion contenant de l’air, des niveaux modérés de CO₂ et une humidité élevée. Dans des essais continus, les cristaux ont accompli des centaines de cycles absorption–désorption à température constante avec seulement environ un pour cent de perte de capacité, soulignant leur durabilité.
Ce que cela signifie pour l’avenir du captage du carbone
En combinant une forte capacité de capture du CO₂, une résistance à l’eau et une libération à faible énergie dans un solide organique simple à fabriquer, ce travail dessine un nouveau modèle pour les matériaux de capture. Plutôt que de compter sur des pores permanents ou des solvants liquides énergivores, les cristaux exploitent un changement de phase réversible — fusion des chaînes et recristallisation — pour passer d’états sans CO₂ à des états riches en CO₂. Comme ces matériaux peuvent fournir des flux de CO₂ concentrés avec un chauffage relativement doux, leur coût énergétique estimé est inférieur à celui de nombreuses options existantes. Si leur mise à l’échelle réussit, de tels solides réactifs pourraient rendre le captage industriel du carbone plus économique et flexible, aidant à décarboner les grandes sources d’émissions sans exiger de changements radicaux dans le fonctionnement des centrales électriques et des usines.
Citation: Petrović, A., Lima, R.J.d.S., Hadaf, G.B. et al. Nonporous hydrophobic organic crystals for carbon dioxide capture via chain-melting phase transition. Nat Commun 17, 2293 (2026). https://doi.org/10.1038/s41467-026-69006-x
Mots-clés: captage du carbone, adsorbants solides, matériaux à changement de phase, chimadsorption, cristaux hydrophobes